2019-10-29 京都大学
水野桂 医学研究科博士課程学生、赤松秀輔 同助教、小川修 同教授、藤本明洋 同特定准教授(現・東京大学教授)、中川英刀 理化学研究所チームリーダーらの研究グループは、分子バーコード法と呼ばれる手法と情報解析法を組み合わせて、血中遊離DNA(cfDNA:cell-free DNA)のシークエンスデータから、がん細胞に由来する微量の突然変異(cfDNAの0.2%程度)を高精度に検出する解析手法(eVIDENCE ソフトウェア)を開発しました。
がん罹患者の血液中には、白血球などの正常細胞から遊離したDNAのほかに、がん細胞から遊離したDNAが存在することが知られていますが、がん細胞由来のDNAが微量であるために、次世代シークエンサーを用いたcfDNAの解析では、がん細胞に存在する突然変異を正確に検出することが困難な場合があるという問題点がありました。
本研究成果は、血液中に存在するがんの変異を検出することで、リキッドバイオプシーによるがんゲノム医療の実現に貢献するものと期待できます。
本研究成果は、2019年10月22日に、国際学術誌「Scientific Reports」に掲載されました。
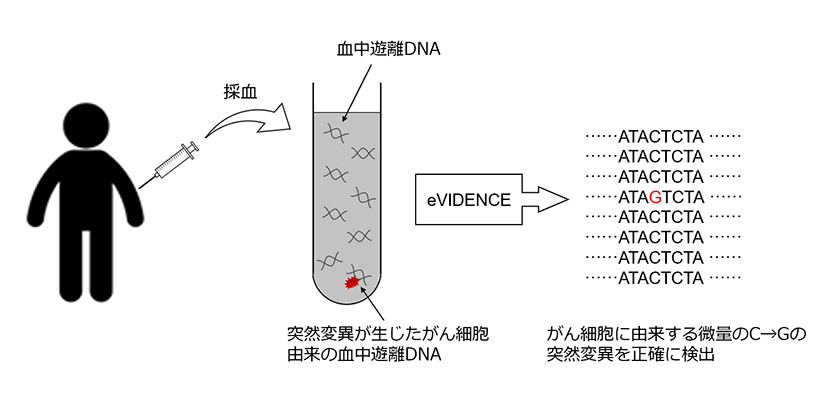
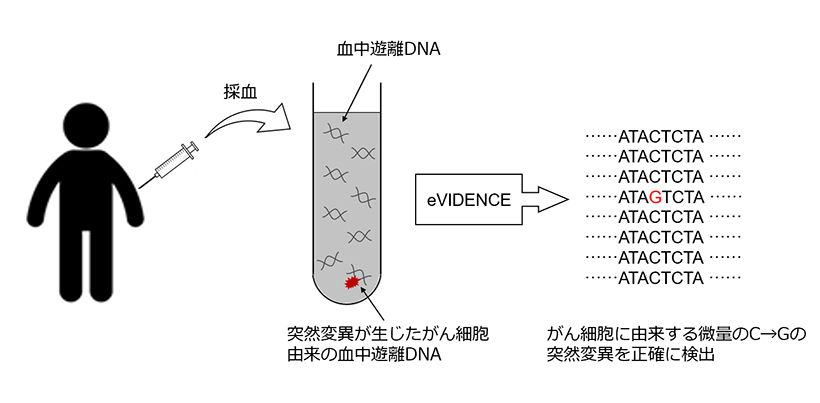
図:本研究の概要図
書誌情報
【DOI】https://doi.org/10.1038/s41598-019-51459-4
【KURENAIアクセスURL】http://hdl.handle.net/2433/244393
Kei Mizuno, Shusuke Akamatsu, Takayuki Sumiyoshi, Jing Hao Wong, Masashi Fujita, Kazuaki Maejima, Kaoru Nakano, Atushi Ono, Hiroshi Aikata, Masaki Ueno, Shinya Hayami, Hiroki Yamaue, Kazuaki Chayama, Takahiro Inoue, Osamu Ogawa, Hidewaki Nakagawa and Akihiro Fujimoto (2019). eVIDENCE: a practical variant filtering for low-frequency variants detection in cell-free DNA. Scientific Reports, 9:15017.
詳しい研究内容について
血中遊離 DNA の高精度解析手法を開発
―リキッドバイオプシーによるゲノム医療へ―
概要
京都大学大学院医学研究科の水野桂博士課程学生、赤松秀輔助教、小川修教授、理化学研究所生命医科学研 究センターがんゲノム研究チームの中川英刀チームリーダー、京都大学大学院医学研究科の藤本明洋特定准教 授( 研究当時、現( 東京大学大学院医学系研究科教授)らの共同研究グループは、分子バーコード法と呼ばれ る手法と情報解析法を組み合わせて、血中遊離 DNA cfDNA cell-free(DNA)のシークエンスデータから、 がん細胞に由来する微量の突然変異( cfDNA の 0.2%程度)を高精度に検出する解析手法( eVIDENCE ソフト ウェア)を開発しました。
がん罹患者の血液中には、白血球などの正常細胞から遊離した DNA のほかに、がん細胞から遊離した DNA が存在することが知られていますが、がん細胞由来の DNA が微量であるために、次世代シークエンサーを用 いた cfDNA の解析では、がん細胞に存在する突然変異を正確に検出することが困難な場合があるという問題 点がありました。本研究成果は、血液中に存在するがんの変異を検出することで、リキッドバイオプシー[1]に よるがんゲノム医療の実現に貢献するものと期待できます。
本成果は、2019 年 10 月 22 日に英国の科学雑誌「Scientific(Reports」に掲載されました。
1.背景
近年、がん細胞に生じた突然変異を検出し、突然変異の種類に応じて投与する抗がん剤を検討するがんゲノ ム医療が広まりつつあります。通常は、手術や生検でがん組織を採取して検査を行いますが、がんの種類によ っては組織採取が困難な場合があります。
がん罹患者の血液中には、がん細胞から遊離した DNA が存在していることが知られており、がん由来の血 中遊離 DNA cfDNA cell-free(DNA)を検出することができれば、採血を行うだけでがんゲノム医療を実践 することが可能となります。
一方で、cfDNA の大部分が白血球などの正常細胞由来の DNA で占められており、がん由来の DNA が微量 である場合がしばしばあります。このような場合、次世代シークエンサーを用いて DNA の配列決定を行う際 に、微量ながん細胞由来の突然変異と配列決定時のエラーとの判別が困難となります。
cfDNA に存在する微量な突然変異を検出する手法はこれまでも開発されてきましたが、調べられる遺伝子 に制約があることや、手法間で検出される突然変異の一致率が低いことなどの問題点がありました。
2.研究手法・成果
共同研究グループは、分子バーコード法と呼ばれる手法を用いました。この方法では、調べたい DNA 分子 一つ一つに異なる配列を持った DNA 分子 分子バーコード)を付加することで、シークエンサーの配列決定 時のエラーと、真の突然変異を判別することが可能となります。この手法と情報解析法を組み合わせることで、 cfDNA に存在する微量のがん由来突然変異を高精度に検出する解析手法 eVIDENCE ソフトウェア)を開発 しました。
肝臓がん患者から採取した 27 個の cfDNA サンプルを eVIDENCE で解析したところ、全部で 77 個の突然 変異を検出しました。25 個の突然変異を選んでそれらが本当に cfDNA に存在するのか確認したところ、全て 真の変異であることが分かりました( 図 1)。さらに、cfDNA に 0.2-1.0%だけ存在するわずかな突然変異も正 確に検出できることが示されました。
また、cfDNA とがん組織の両方の解析を行うことのできた症例が 6 例あり、cfDNA とがん組織で検出され た突然変異を比較しました。cfDNA で 26 個、がん組織で 16 個の突然変異を検出し、がん組織で検出された 16 個の変異のうち、12 個は cfDNA でも検出しました 図 2)。cfDNA だけで検出された変異は 14 個あり、 この中には肝臓がんのドライバー遺伝子[2]である ARID1A、NFE2L2、PIK3CA の変異が含まれていました。こ のことは、eVIDENCE を用いた cfDNA の解析は、がん組織を用いた検査よりも重要な遺伝子異常をより多く 捉えることが可能であることを示唆します。
3.波及効果、今後の予定
本研究で開発した cfDNA の解析手法は、がんの種類や調べたい遺伝子の種類に制約なく応用することがで き、現在、進行前立腺がん患者から採取した cfDNA の解析研究を進めています。今後、本研究成果がリキド バイオプシーによるがんゲノム医療の実現に貢献することが期待されます。
4.研究プロジェクトについて
本研究は、日本学術振興会 科学研究費補助金 研究課題番号 JP18H04049)および武田科学振興財団の 研究助成を受けて行われました。
*共同研究グループ
京都大学大学院医学研究科
泌尿器科学教室
博士課程学生 水野 桂
助教 赤松 秀輔
博士課程学生 (研究当時) 住吉 崇幸
准教授 井上 貴博
教授 小川 修
創薬医学講座
特定准教授 (研究当時) 藤本 明洋
(現:東京大学大学院医学系研究科 人類遺伝学教室 教授)
理化学研究所
生命医科学研究センター
がんゲノム研究チーム
チームリーダー 中川 英刀
上級研究員 藤田 征志
広島大学大学院医系科学研究科
消化器・代謝内科学
診療講師 大野 敦司
診療准教授 相方 浩
教授 茶山 一彰
和歌山県立医科大学
外科学第 2 講座
講師 上野 昌樹
講師 速水 晋也
教授 山上 裕機
<用語解説>
[1] リキッドバイオプシー
内視鏡や針などでがん組織を採取する従来の生検( バイオプシー)に代えて、血液などの体液サンプル( リキ ッド)を用いて、遺伝子解析などにより診断や治療効果予測などを行う方法。
[2] ドライバー遺伝子
がんの発生・進展に重要な役割を果たす遺伝子。
<研究者のコメント>
リキッドバイオプシーは従来の生検と比較して患者さんの身体的負担が少なく、また、何度も繰り返し行うこ とが可能なため、今後、がんゲノム医療で果たす役割が期待されています。本研究開発が精度の高い cfDNA 解 析に寄与し、リキッドバイオプシーによるがんゲノム医療の実現に貢献する可能性があるものと考えています。
<論文タイトルと著者>
タイトル: eVIDENCE: a practical variant filtering or low-frequency variants detection in cell-free DNA eVIDENCE (血中遊離 DNA における低頻度変異検出手法)
著 者: Kei Mizuno, Shusuke Akamatsu, Takayuki Sumiyoshi, Jing Hao Wong, Masashi Fujita, Kazuaki Maejima, Kaoru Nakano, Atushi Ono, Hiroshi Aikata, Masaki Ueno, Shinya Hayami, Hiroki Yamaue, Kazuaki Chayama, Takahiro Inoue, Osamu Ogawa, Hidewaki Nakagawa and Akihiro Fujimoto
掲 載 誌: Scientific Reports DOI 未定
<参考図表>
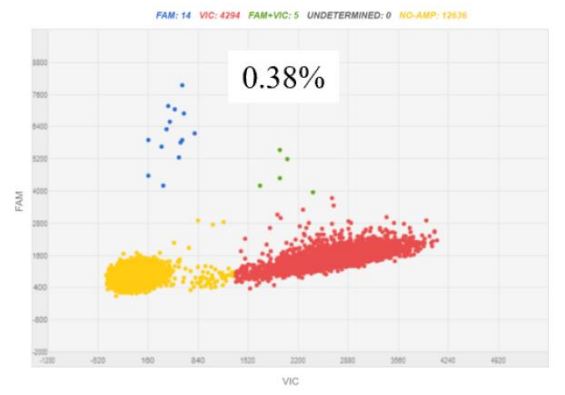
図 1:肝臓がん患者由来の cfDNA を解析したところ、TP53 の突然変異 S269G)が全体の 0.25%に認められるという結 果が得られました。上図は、その変異が cfDNA 中に実際に存在するかどうかを digital(PCR という手法を用いて確認した ものです。青色の点が変異タイプの蛍光を検出したもの、赤色の点が正常タイプの蛍光を検出したものを表しており、変 異タイプが全体の 0.38%で確かに存在することが示されました。黄色の点は変異タイプ・正常タイプのいずれの蛍光も検 出されなかったもの、緑色の点はそのどちらの蛍光も検出されたものを表しています。 がん組織 DNA で cfDNA で認められた変異 認められた変異
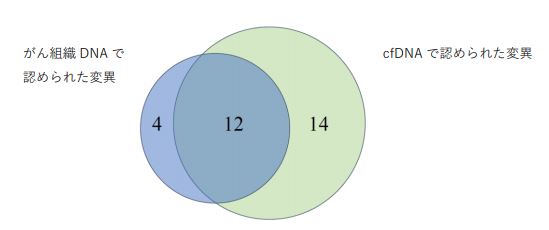
図 2:がん組織で検出された 16 個の変異のうち、12 個 75%)は cfDNA 中にも存在しました。cfDNA だけで検出され た 14 個の変異の中には、ARID1A S1976F)、NFE2L2 E79G)、PIK3CA P449A)のドライバー遺伝子変異が含まれ ていました。