肝がんの再発予防薬剤の反応性予測・予後予測バイオマーカーの開発に期待
2018-04-24 理化学研究所
理化学研究所(理研)生命医科学研究センター肝がん予防研究ユニットの小嶋聡一ユニットリーダー、秦咸陽研究員らの共同研究グループ※は、肝がん治療後の再発を予防する世界初の薬として治験が進められている「非環式レチノイド[1](一般名:ペレチノイン)」が、がん遺伝子「MYCN[2]」を発現する肝がん幹細胞[3]を選択的に排除していることを突き止め、MYCNが肝がん再発に対する創薬標的であることを明らかにしました。
今後、肝がん患者のMYCNの発現量を検査することで、肝がんの再発リスクの予測や、非環式レチノイドが効くと予想される患者を予め選び出すコンパニオン診断[4]が可能になると期待できます。
肝がんは、外科的切除などで治療した後も再発する確率が高く、極めて予後不良の疾患です。高い再発率の原因として、まだがん化していない肝臓組織に存在するがん幹細胞から新たながんが生じる可能性が考えられています。今回、共同研究グループは、非環式レチノイドがMYCN陽性肝がん幹細胞を標的とし、肝がんの再発を抑制していることを突き止めました。臨床研究の結果、非環式レチノイドを高濃度に投与したグループ(600mg/日)の約7割の被験者で、MYCN遺伝子の発現が抑制されました。また、臨床検体の解析により、MYCNの発現は肝がんの再発率と正に相関することも分かりました。
本研究は、米国アカデミー紀要『Proceedings of the National Academy of Sciences of the United States of America』の掲載に先立ち、オンライン版(4月23日付け:日本時間4月24日)に掲載されます。
※共同研究グループ
理化学研究所 生命医科学研究センター
肝がん予防研究ユニット
ユニットリーダー 小嶋 聡一(こじま そういち)
(旧ライフサイエンス技術基盤研究センター 生命機能動的イメージング部門 イメージング基盤・応用研究グループ 微量シグナル制御技術開発特別ユニット 特別ユニットリーダー)
研究員 秦 咸陽(しん せんよう)
(旧ライフサイエンス技術基盤研究センター 生命機能動的イメージング部門 イメージング基盤・応用研究グループ 微量シグナル制御技術開発特別ユニット 特別研究員)
トランスクリプトーム研究チーム
チームリーダー ピエロ・カルニンチ(Piero Carninci)
(旧ライフサイエンス技術基盤研究センター 機能性ゲノム解析部門 LSA要素技術研究グループ トランスクリプトーム研究チーム チームリーダー)
専任研究員 橋本 浩介(はしもと こうすけ)
(旧ライフサイエンス技術基盤研究センター 機能性ゲノム解析部門 LSA要素技術研究グループ トランスクリプトーム研究チーム 専任研究員) 細胞機能変換技術研究チーム
チームリーダー 鈴木 治和(すずき はるかず)
(旧ライフサイエンス技術基盤研究センター 機能性ゲノム解析部門 オミックス応用技術研究グループ 細胞機能変換技術研究チーム チームリーダー)
金沢大学大学院先進予防医学研究科 保健学科 病態検査学講座
教授 本多 政夫(ほんだ まさお)
東京慈恵会医科大学 臨床検査医学講座
教授 松浦 知和(まつうら ともかず)
東京医科歯科大学 生体材料工学研究所 薬化学分野
教授 影近 弘之(かげちか ひろゆき)
鳥取大学大学院医学系研究科 機能性再生医科学専攻 遺伝子医療学部門
教授 汐田 剛史(しおた ごうし)
岐阜大学大学院医学系研究科 消化器病態学分野
教授 清水 雅仁(ひみず まさひと)
※研究支援
本研究は、日本学術振興会(JSPS)科学研究費補助金 若手研究(B)「肝癌幹細胞から成熟癌細胞への分化に伴う代謝リプログラミングのシステム解析」、Core-to-Coreプログラム「難治疾患に対する分子標的薬創製のための国際共同研究拠点の構築」及び日本医療研究開発機構(AMED)肝炎等克服実用化研究事業(B型肝炎創薬実用化等研究事業)の支援を受けて行われました。
背景
肝がん(肝臓がん)は予後が悪いがんの一つで、日本では年間の死亡者数が3万人を超えており、世界的にも肝がんは全がん種の中で死因の第2位です注1)。肝がんの再発率が高い原因として、外科的切除などでがんを除去しても、残された肝臓組織に残存するがん幹細胞から新たながんが生じる可能性が考えられています。
「非環式レチノイド(一般名:ペレチノイン)」は、岐阜大学の武藤泰敏教授(当時)が1981年に発表した合成レチノイドで注2)、肝がん治療後の患者を対象に1年間投与したところ、投与終了後約4年にわたり肝がんの再発が抑制されたことから、世界初の肝がん再発予防薬として期待されています注3)。これまで小嶋ユニットリーダーらは、非環式レチノイドが正常肝細胞には影響を与えず、肝がん細胞を選択的に死滅させる仕組みを明らかにしてきました注4)。しかし、非環式レチノイドが肝がん幹細胞に作用するかどうかは分かっていませんでした。
注1)日本肝臓学会「肝がん白書 平成27年版」
注2)Muto Y, et al. Jpn J Cancer Res [Gann] 1981;72:974-977
注3)Muto Y, et al. N Engl J Med 1996; 334:1561-1567
注4)2016年1月8日プレスリリース「肝がん再発予防薬の作用メカニズムを解明」
研究手法と成果
共同研究グループはまず、非環式レチノイドが作用する遺伝子を網羅的に調べるため、正常肝細胞株と肝がん細胞株をそれぞれ非環式レチノイドで処理し、発現が変化した遺伝子をCAGE法[5]を用いたトランスクリプト-ム(細胞内の全転写産物)解析を行いました。その結果、肝がん細胞株での「MYCN遺伝子」の発現が、非環式レチノイド処理により一過的に強く抑制されることが分かりました。
さらに、非環式レチノイドの臨床試験に参加した患者の肝がん組織を用いてMYCNの遺伝子発現を解析したところ、非環式レチノイドの低濃度投与群(300mg/day:6名)ではMYCNの発現に影響がみられなかったのに対し、高濃度投与群(600mg/day:6名)では約7割(4名)の患者においてMYCNの発現抑制が確認され、MYCNが非環式レチノイドの薬剤反応マーカーであることが示されました。
次に、肝がん細胞におけるMYCNの役割を調べるため、発現解析と機能解析を行いました。免疫染色法[6]およびFACS[7]解析により、MYCNタンパク質は細胞周期[8]G2期の肝がん細胞で有意に高いことが分かりました。さらに、siRNA法[9]を用いて肝がん細胞のMYCNの機能阻害実験を行ったところ、細胞増殖が抑制され、アポトーシス[10]の誘導が観察されました。これらの結果から、MYCN遺伝子は肝がん細胞においてがん遺伝子として働き、細胞増殖を制御することが示されました。
非環式レチノイドの肝がん再発予防効果は、肝がん幹細胞がMYCNを発現し、非環式レチノイドの標的となっている可能性が考えられます。公開されている遺伝子発現データベースを用いて、肝がん患者の臨床データを解析したところ、肝がん組織中のMYCN遺伝子発現は、EpCAM遺伝子をはじめとするがん幹細胞マーカーの発現と有意に相関していました。また、肝がん細胞株を培養した細胞集団を免疫染色法で観察したところ、MYCNとEpCAMの両方のタンパク質を発現する二重陽性肝がん幹細胞の存在が確認されました(図1)。これら二重陽性細胞は、非環式レチノイド処理によって濃度依存的に排除されました。
最後に、MYCNの発現と肝がんの再発の関係を調べました。日本およびヨーロッパの肝がん患者の臨床検体を用いた解析では、MYCNの発現は、肝がん非がん部より肝がん組織において有意に高いことが分かりました。さらに、日本で行われた肝がん患者の追跡調査から、MYCNの発現が高いと、術後の肝がん再発率も高くなる正の相関がみられました(図2)。これは、MYCNが肝がんの再発予測バイオマーカーとして有用であることを示しています。
今後の期待
MYCN遺伝子陽性の肝がん患者に対して、早期段階におけるMYCN遺伝子発現の抑制が予後の改善につながる可能性が考えられます。今後、肝がん患者のMYCNの発現量を検査することで、肝がんの再発リスクの予測や、非環式レチノイドが効くと予想される患者を予め選び出すコンパニオン診断が可能になると期待できます。
原論文情報
Xian-Yang Qin, Harukazu Suzuki, Masao Honda, Hikari Okada, Shuichi Kaneko, Ikuyo Inoue, Etsuko Ebisui, Kosuke Hashimoto, Piero Carninci, Keita Kanki, Hideki Tatsukawa, Naoto Ishibashi, Takahiro Masaki, Tomokazu Matsuura, Hiroyuki Kagechika, Kan Toriguchi, Etsuro Hatano, Yohei Shirakami, Goshi Shiota, Masahito Shimizu, Hisataka Moriwaki, Soichi Kojima, “Prevention of hepatocellular carcinoma by targeting MYCN-positive liver cancer stem cells with acyclic retinoid”, Proceedings of the National Academy of Sciences of the United States of America, 10.1073/pnas.1802279115
補足説明
-
- 非環式レチノイド
- 一般名:ペレチノイン、英語名:acyclic retinoid(略称:ACR)。興和株式会社が現在、第Ⅲ相臨床試験を実施している世界初の肝がん再発化学予防候補薬(開発コード名はNIK-333)。
-
- MYCN
- 特定のDNA配列に結合して標的遺伝子の発現を制御する転写因子MYCファミリーの一つをコードする遺伝子。神経芽腫の発生に関わるなど、がん遺伝子として知られる。ミックエヌと読む。
-
- がん幹細胞
- 幹細胞は、体のさまざまな細胞に分化する能力と、自分と同じ幹細胞を作る能力の両方を持つ細胞を指す。近年、がんの形成においても少数の幹細胞が大量のがん細胞を作り出す例が見つかり、がん幹細胞と呼ばれるようになった。
-
- コンパニオン診断
- 抗体医薬など特定の分子に作用する薬剤を用いる場合、その分子の発現を投与前に検査し、患者個人の薬剤反応性を治療前に予測して最適な治療計画を立てることができる。このように、特定の治療薬の患者適合性を調べることをコンパニオン診断と呼ぶ。
-
- CAGE法
- 理研が独自に開発した手法で、耐熱性逆転写酵素やmRNAのCap構造を捕捉する技術を組み合わせて転写産物の5’末端の塩基配列を決定・定量する実験手法。この塩基配列を読み取ってゲノム配列と照らし合わせて、どこから、どれだけの転写が始まっているかを調べることができる。遺伝子の転写開始点をゲノムワイドに同定できる。CAGEはCap Analysis Gene Expressionの略
-
- 免疫染色法
- 観察したい分子に対する抗体を培養細胞や組織切片に反応させ、抗原抗体反応によりその分子を可視化する手法。免疫組織化学染色法とも呼ばれる。
-
- FACS技術
- 本研究では、細胞に核染色剤を導入したものを対象に、細胞のDNA量を統計的に解析するのに用いた。FACSはFluorescent activated cell sorterの略。
-
- 細胞周期
- 細胞は、分裂を繰り返して増殖するが、この細胞分裂のサイクルを細胞周期と呼ぶ。細胞周期は、間期とM期に分けられる。分裂が起こるM(Mitosis)期と、DNAの複製が起こるS(Synthesis)期、それぞれの間をつなぐG1(Gap1)期、G2(Gap2)期からなり、サイクルはG1→S→G2→M→G1→…の順に進む。
-
- siRNA法
- 短い2本鎖RNA(siRNA、small interference RNA)を細胞に導入し、任意の遺伝子の阻害をする実験手法。2本鎖RNAによって配列特異的にRNAが分解されるRNA 干渉(RNAi、RNA interference)の原理に基づく。
-
- アポトーシス
- 多細胞生物の体を構成する細胞に見られる、遺伝的にプログラムされた細胞死。
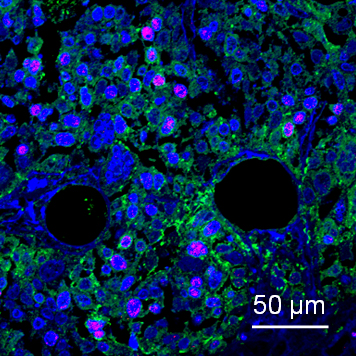
図1 がん遺伝子MYCNを発現する肝がん幹細胞の蛍光免疫染色像
肝がん組織の蛍光免疫染色像。細胞の核をDAPI(青)で、MYCNタンパク質をピンク色で、肝がん幹細胞をそのマーカーであるEpCAM(緑)の蛍光染色でそれぞれ観察した。MYCNとEpCAMの両方のタンパク質を発現する二重陽性肝がん幹細胞の存在が確認されたことが分かる。丸い黒に見える部分は、血管(中心静脈)の断面。
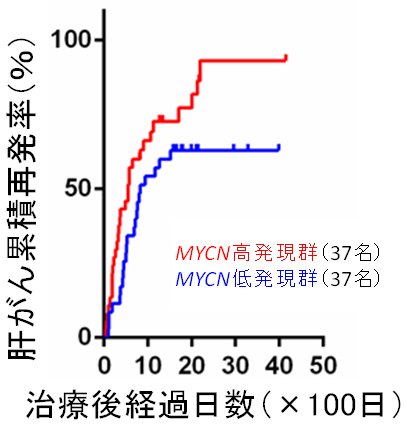
図2 MYCN遺伝子の発現量と肝がん再発率の関係
日本で行われた肝がん患者の治療後10年以上にわたる追跡調査の結果と、切除した肝がん組織でのMYCNの発現量の解析をグラフにしたもの。MYCNの発現が高い患者は、再発率も高いことが分かる。なおこの解析では、転移性の肝がんを除外している。
発表者
理化学研究所
生命医科学研究センター 肝がん予防研究ユニット
ユニットリーダー 小嶋 聡一(こじま そういち)
(旧ライフサイエンス技術基盤研究センター 生命機能動的イメージング部門 イメージング基盤・応用研究グループ 微量シグナル制御技術開発特別ユニット 特別ユニットリーダー)
研究員 秦 咸陽(しん せんよう)
(旧ライフサイエンス技術基盤研究センター 生命機能動的イメージング部門 イメージング基盤・応用研究グループ 微量シグナル制御技術開発特別ユニット 特別研究員)
報道担当
理化学研究所 広報室 報道担当