2020-07-14 名古屋大学,日本医療研究開発機構
名古屋大学大学院医学系研究科神経遺伝情報学の大野欽司教授、医学系研究科医療技術学専攻病態解析学の平山正昭准教授、神経内科学の勝野雅央教授、博士課程大学院生の西脇寛、岩手医科大学脳神経内科・老年科の前田哲也教授、岡山脳神経内科クリニックの柏原健一院長、福岡大学医学部脳神経内科の坪井義夫教授らの研究グループは、日本・アメリカ・フィンランド・ロシア・ドイツのパーキンソン病患者の腸内細菌叢*1のメタ解析を行い、ムチン*2分解菌であるAkkermansiaが共通して増加し、短鎖脂肪酸*3産生菌であるFaecalibacteriumとRoseburiaが減少していることを明らかにしました。
これまでにパーキンソン病患者の腸内細菌叢解析が17報の論文に報告されてきました。しかし、健常人においても腸内細菌叢は国ごとに大きく異なることから国を超えてパーキンソン病と関連のある腸内細菌を同定することは困難でした。本研究チームは、過去最多のパーキンソン病患者の協力を得て腸内細菌叢解析を行いました。次に、国を超えて腸内細菌叢を統合解析するメタ解析手法を開発し、過去に報告されたアメリカ・フィンランド・ロシア・ドイツの4か国のパーキンソン病患者の腸内細菌叢と合わせてメタ解析を行いました。また、腸内細菌叢の代謝パスウェイ(代謝経路)を解析する手法として、KOSEA(KEGG orthology set enrichment analysis)手法*4を開発しました。メタ解析の結果、パーキンソン病患者の腸内細菌叢では、Akkermansiaの増加とFaecalibacteriumとRoseburiaの減少を認めました。Akkermansiaの増加によってムチン層が分解され腸管壁の透過性が上昇し、腸管神経叢が酸化ストレスに晒されることが予想されます。腸管壁透過性の上昇が、パーキンソンの原因物質であるα-シヌクレイン*5の腸管神経叢*6への蓄積を促進し、パーキンソン病の発症や進行につながる可能性が示唆されました。また、短鎖脂肪酸産生菌(FaecalibacteriumとRoseburia)の減少により中枢神経の炎症を抑制できなくなることが予想されます。
本研究の成果は、パーキンソン病の病態の解明と新規治療法開発につながることが期待されます。
ポイント
- 国ごとに大きく異なる腸内細菌叢を、国を超えて統合解析するメタ解析の手法を構築した。
- 日本・アメリカ・フィンランド・ロシア・ドイツの5か国のパーキンソン病患者の腸内細菌叢のメタ解析を行った。
- 5か国のパーキンソン病患者においてムチン分解菌であるAkkermansiaの増加と短鎖脂肪酸産生菌であるFaecalibacteriumとRoseburiaの減少を認めた。
- 腸管壁ムチン分解による腸管壁透過性の上昇が、α-シヌクレイン凝集体の腸管神経叢への蓄積を促進し、パーキンソン病の発症や進行につながる可能性が示唆された。
- 短鎖脂肪酸の低下により中枢神経の炎症を抑制できなくなりパーキンソン病を進行させる可能性が示唆された。
背景
パーキンソン病は、中脳の黒質にあるドパミン産生細胞にレビー小体と呼ばれるα-シヌクレイン凝集体が異常凝集することによって引き起こされます。α-シヌクレイン凝集体は、腸管神経叢から始まり中脳黒質まで上行する可能性が示されてきました。α-シヌクレイン凝集体はプリオン*7のように正常のα-シヌクレインを異常凝集させて異常を伝播させることが明らかにされています。パーキンソン病患者ではα-シヌクレイン凝集体が迷走神経背側核*8から中脳黒質に向かって上行することが示されてきました。また、便秘、レム睡眠行動障害、鬱がパーキンソン病の運動症状が始まるそれぞれ20年、10年、5年前から起こることが知られており、これはα-シヌクレイン凝集体が迷走神経背側核から青斑核*9に向かって上行する現象と一致しています。加えて、パーキンソン病患者の腸管神経叢には高い頻度でα-シヌクレイン凝集体が蓄積していることが知られています。また、パーキンソン病患者では腸管透過性が上昇することを本研究チームとドイツのグループが以前に報告をしました。
いままでに17報のパーキンソン病患者の腸内細菌叢研究が報告されてきました。しかし、健常者においても国による腸内細菌叢の違いが大きく国を超えてパーキンソン病患者で共通で変わる菌を特定することは困難でした。そこで、本研究チームは、過去最多のパーキンソン病患者の協力を得て腸内細菌叢解析を行いました。次に、国を超えて腸内細菌叢を統合解析するメタ解析手法を構築し、過去に報告されたアメリカ・フィンランド・ロシア・ドイツの4か国のパーキンソン病患者の腸内細菌叢と合わせてメタ解析を行いました。
研究成果
腸内細菌叢に影響を与える因子(ボディマス指数(BMI)、便秘、性別、年齢、薬剤)の影響を排除したところ、5か国のパーキンソン病患者の腸内細菌叢で共通してAkkermansia、Catabacterが増加し、Roseburia、Faecalibacterium、Lachnospiraceae ND3007 group が減少していることを明らかにしました(図1)。メタ解析に含めることができなかった12報の研究結果を調べたところ、Akkermansiaの増加、Roseburia、Faecalibacteriumの減少が多くの研究で認められました。また、腸内細菌叢の代謝パスウェイを解析するKOSEA(KEGG orthology set enrichment analysis)法を開発し、パスウェイ解析を行ったところ、腸内細菌叢による短鎖脂肪酸代謝がパーキンソン病で変化していることがわかりました。これらの解析により、ムチン分解菌であるAkkermansiaの増加と短鎖脂肪酸産生菌であるRoseburiaとFaecalibacteriumの減少がパーキンソン病患者において国を超えて認められることを明らかにしました。
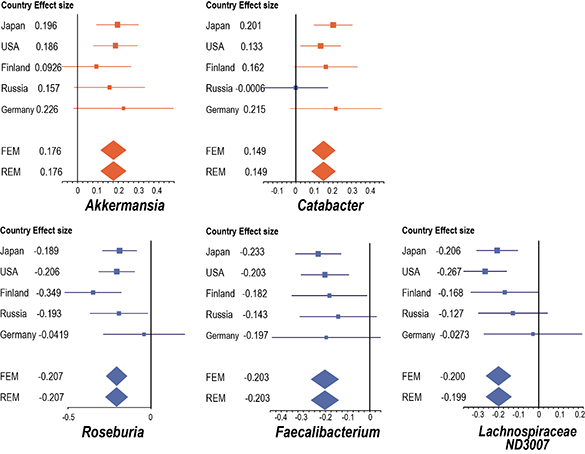
図 15か国のパーキンソン病患者で共通して変化が認められた5種類の腸内細菌。パーキンソン病で上昇する細菌を赤で、低下する細菌を青で示します。5か国のデータでは、平均値を箱で示し、95%信頼区間をヒゲで示します。FEM(fixed effect model)とREM(random effect model)は5か国の統合指標です。95%s信頼区間をダイアモンドで示します。
今後の展開
Akkermansiaの増加によってムチン層が分解され腸管の透過性が上昇することによって腸管神経叢にα-シヌクレインが異常凝集し、中脳黒質まで異常凝集したα-シヌクレインが上行する可能性が示されました。加えて、短鎖脂肪酸産生菌の減少によって中枢神経の炎症を制御しにくくなる可能性も示されました。また、今回開発した腸内細菌叢の代謝パスウェイを解析するKOSEA 法は今後広く腸内細菌叢の代謝パスウェイを解析に役立つことが期待されます。今回明らかにした腸内細菌叢の変化のパーキンソン病への関与を今後さらにモデル動物などを用いてパーキンソン病の病態分子機構の解明につなげます。
用語説明
- *1腸内細菌叢:
- 以前は腸内フローラとも呼ばれた。主に大腸に生息する細菌の集合体。
- *2ムチン(mucin):
- 動物の上皮細胞から分泌される粘液の主成分。糖タンパクの混合物である。腸管において杯細胞から分泌され粘膜表面を物理的に外的刺激から保護している。
- *3短鎖脂肪酸(short chain fatty acids):
- 腸内細菌が食物繊維を消化する際に、ヒトの場合、酢酸、プロピオン酸、酪酸が産生され、これらを短鎖脂肪酸と呼ぶ。短鎖脂肪酸はエネルギー源として利用されるとともに、異常な免疫応答を抑制するなどの生体調節機能を有している。
- *4KOSEA(KEGG orthology set enrichment analysis)法:
- 遺伝子発現のパスウェイ解析で定評があるGSEA(gene set enrichment analysis)を腸内細菌叢の解析に応用した手法。KEGG(Kyoto Encyclopedia of Genes and Genomes)は京都大学で開発維持しされているパスウェイデータベースである。
- *5α-シヌクレイン(α-synuclein):
- 神経組織中にみられる機能不明のタンパク質である。このタンパク質の細胞内異常蓄積がパーキンソン病をはじめとする神経変性疾患の原因とされている。
- *6腸管神経叢:
- 腸管壁の外側にある細い神経のネットワーク。
- *7プリオン:
- 感染するタンパク質とも呼ばれる。凝集体のように異常に形成されたタンパク質が正常なタンパク質を異常な形に変えることができる。
- *8迷走神経背側核:
- 内臓を支配する副交感神経である迷走神経の脳幹部にある神経核。
- *9青斑核:
- 脳幹にあるノルアドレナリン作動性ニューロンを含む神経核であり、鬱との関連が示されている。
発表雑誌
- 掲雑誌名
- Movement Disorderse(2020年6月18日付の電子版)
- 論文タイトル
- Meta-Analysis of Gut Dysbiosis in Parkinson’s Disease
- 著者
- Hiroshi Nishiwaki, MD1; Mikako Ito, PhD1; Tomohiro Ishida, MS2; Tomonari Hamaguchi, MD, PhD1; Tetsuya Maeda, MD, PhD3; Kenichi Kashihara, MD, PhD4; Yoshio Tsuboi, MD, PhD5; Jun Ueyama, PhD2; Teppei Shimamura, PhD6; Hiroshi Mori, PhD7; Ken Kurokawa, PhD7; Masahisa Katsuno, MD, PhD8; Masaaki Hirayama, MD, PhD2; Kinji Ohno, MD, PhD1
- 所属
- 1Division of Neurogenetics, Center for Neurological Diseases and Cancer, Nagoya University Graduate School of Medicine, Nagoya, Japan
- 2Department of Pathophysiological Laboratory Sciences, Nagoya University Graduate School of Medicine, Nagoya, Japan 3Division of Neurology and Gerontology, Department of Internal Medicine, School of Medicine, Iwate Medical University, Iwate, Japan
4Department of Neurology, Okayama Kyokuto Hospital, Okayama, Japan
5Department of Neurology, Fukuoka University, Fukuoka, Japan
6Division of Systems Biology, Center for Neurological Diseases and Cancer, Nagoya University Graduate School of Medicine, Nagoya, Japan
7Genome Evolution Laboratory, Department of Informatics, National Institute of Genetics, Mishima, Japan
8Department of Neurology, Nagoya University Graduate School of Medicine, Japan - DOI
- 10.1002/mds.28119
- URL
- https://onlinelibrary.wiley.com/doi/full/10.1002/mds.28119
研究支援
本研究は、国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業AMED-CREST「微生物叢と宿主の相互作用・共生の理解と、それに基づく疾患発症のメカニズム解明」領域における研究開発課題「パーキンソン病の起因となる腸管α-synuclein異常蓄積に対する腸内細菌叢の関与の解明」(研究開発代表者:大野欽司)の一環で行われました。
お問い合わせ先
名古屋大学医学部・医学系研究科
神経遺伝情報学 教授
大野欽司
平山正昭
広報担当
名古屋大学医学部・医学系研究科総務課総務係
AMED事業に関すること
日本医療研究開発機構(AMED)
シーズ開発・研究基盤事業部革新的先端研究開発課