2020-10-20 筑波大学,日本医療研究開発機構
あらゆる生物の体は、各々の役割に特化した細胞の集まりでできています。それらの細胞を生み出す元となるものが幹細胞であり、その働きは、幹細胞が局在する場所から伝達されるシグナルによって制御されています。ところが近年の研究により、そのシグナルが、ホルモンや神経伝達物質といった外部からのシグナルによって調節されることが明らかになってきました。ホルモンや神経伝達物質による幹細胞の制御は、傷害やストレスに対する応答、発生過程で見られ、需要に応じた幹細胞の増殖を可能にしています。
モデル動物であるキイロショウジョウバエにおいては、生殖幹細胞は交尾後に増加します。従って、交尾が生殖幹細胞の増殖を引き起こす外部シグナルであると考えられます。本研究では、キイロショウジョウバエの卵子の元となる生殖幹細胞が交尾刺激に応答して増殖するプロセスが、卵巣へと伸びる神経によって調節されていることを明らかにしました。この神経はオクトパミンと呼ばれる神経伝達物質を産生・放出し、卵巣に存在するオクトパミン受容体に受け取られることが、交尾に伴う生殖幹細胞の増殖に必須であることを解明しました。本研究は、動物の生殖を支える生殖幹細胞の調節に、卵巣へと伸びる神経による直接的な支配が関わることを示した初めての成果です。オクトパミンは哺乳動物のノルアドレナリンに相当し、進化的に幅広く保存された神経伝達物質であると考えられていることから、今回の成果は動物に共通した神経による幹細胞の制御メカニズムの解明に貢献することが期待されます。
研究代表者
筑波大学 生存ダイナミクス研究センター 丹羽 隆介 教授
研究の背景
あらゆる生物の体は、各々の役割に特化した細胞の集まりでできています。それらの細胞を生み出す元となるものが幹細胞であり、幹細胞の動態は幹細胞ニッチ注1)から伝達されるシグナルによって制御されています。ところが近年の研究により、その幹細胞ニッチから伝達されるシグナルが、ホルモンや神経伝達物質といった外部からのシグナルによって調節されることが明らかになってきました。それらホルモンや神経伝達物質による幹細胞の制御は、傷害やストレスに対する応答、発生過程で見られ、需要に応じた幹細胞の増殖を可能にしています。
このような外部からのシグナルによる幹細胞制御の一例として、2016年に本研究チームは、モデル生物であるキイロショウジョウバエを用いて、卵子をつくる元となる生殖幹細胞注2)が、交尾後に増加することを報告しています。しかし、産卵の需要に応えるために、どのようにして交尾という外部からのシグナルが生殖幹細胞の増殖を引き起こすのかは明らかではありませんでした。
研究内容と成果
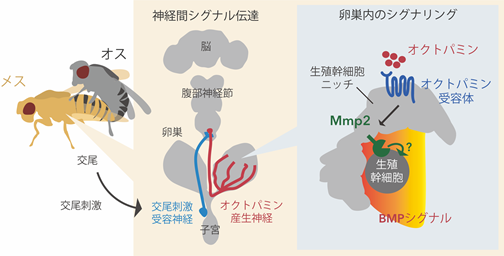
本研究グループは、様々な遺伝子を導入したショウジョウバエを用いた遺伝学的研究を出発点として、交尾によって引き起こされる生殖幹細胞の増殖に必要な生体分子および遺伝子を探索しました。その結果、候補因子として「オクトパミン注3)」と呼ばれる神経伝達物質と、その受容体であるオクトパミン受容体を同定しました。オクトパミンは神経系で産生されることが知られており、オクトパミン産生神経は、中枢神経系から卵巣へと軸索を伸ばしてシナプスを形成しています。そのオクトパミン産生神経を活性化したところ、未交尾のショウジョウバエにおいても生殖幹細胞の増殖を引き起こすことができました。一方で、オクトパミンの産生を阻害すると、交尾後の生殖幹細胞の増加は起こりませんでした。さらに、卵巣につながるオクトパミン産生神経は、子宮で交尾刺激を受容する神経と中枢神経系内で直接シナプスを形成しており、交尾刺激が、子宮―交尾刺激受容神経―オクトパミン産生神経―卵巣という経路で伝達されることが明らかになりました(図左)。
オクトパミン産生神経が卵巣へと伸びていることから、卵巣においてオクトパミン受容体が機能していると考えられます。そこで、卵巣の様々な細胞集団に対してオクトパミン受容体の機能阻害を行ったところ、交尾後の生殖幹細胞増加には、生殖幹細胞に接しているエスコート細胞(ニッチ細胞の一種)におけるオクトパミン受容体が必須であることが分かりました。さらに、オクトパミン受容体の下流で、タンパク質分解酵素のマトリックスメタロプロテアーゼ(Mmp2)注4)が機能することで、生殖幹細胞の増殖に重要なニッチシグナルである骨形成タンパク質(BMP)注5)シグナルが強くなりました。これらのことから、中枢神経系から卵巣へと伸びるオクトパミン産生神経が生殖幹細胞ニッチにおけるオクトパミン受容体を活性化し、細胞外プロテアーゼMmp2を介して生殖幹細胞ニッチからのBMPシグナルを増強させる、という一連のメカニズムが明らかになりました(図右)。
今後の展開
今回の研究で、卵巣につながる神経が生殖幹細胞ニッチを刺激して、産卵をもたらす生殖幹細胞の増殖に影響を及ぼすことが分かりました。しかしながら、細胞外プロテアーゼMmp2が生殖幹細胞ニッチのシグナルを調節する仕組みは未解明です。Mmp2には細胞外に存在するコラーゲンなどのタンパク質を切断する働きがあり、Mmp2が何らかのタンパク質を切断することでシグナルが伝えられると考えられます。今後、このシグナル伝達経路上でMmp2が作用するタンパク質の探索を行っていきます。
オクトパミンは、哺乳動物の神経伝達物質として有名なノルアドレナリンに似た物質であり、またMmp2もヒトを含むあらゆる動物が持っている分子です。よって、ノルアドレナリン産生神経を含む神経系やMmpが、ショウジョウバエ以外の生物での幹細胞の動態制御に与える影響が明らかになれば、幅広い動物において、神経系による幹細胞の調節メカニズムが解明されることが期待されます。
用語解説
- 注1)幹細胞ニッチ
- 幹細胞に接着し、幹細胞の増殖・分化を調節する細胞集団。
- 注2)生殖幹細胞
- 卵巣または精巣に存在し、配偶子へと分化する能力を持つ幹細胞。
- 注3)オクトパミン
- アミノ酸であるチロシンから生合成されるモノアミン神経伝達物質。ノルアドレナリンの類縁分子。
- 注4)マトリックスメタロプロテアーゼ(Mmp: Matrix metalloproteinase)
- 細胞内外の基質を切断するタンパク質分解酵素。キイロショウジョウバエゲノム上にはMmp1、Mmp2の2つが存在する。
- 注5)骨形成タンパク質(BMP: Bone Morphogenetic Protein)
- 骨の形成を誘導する生理活性物質で、多彩な生理機能を持つことが知られている。キイロショウジョウバエにおいても初期発生や幹細胞制御において重要な働きを持つ。
研究資金
本研究は、国立研究開発法人日本医療研究開発機構(AMED)革新的先端研究開発支援事業(AMED-CREST)「全ライフコースを対象とした個体の機能低下機構の解明」研究開発領域における研究開発課題「成長期の栄養履歴が後期ライフステージに与える機能低下のメカニズム」(研究期間:平成29年度~令和4年度)、日本学術振興会科学研究費助成事業 新学術領域研究「生殖幹細胞インテグリティ制御におけるホルモンと神経伝達物質の役割の解明」(平成31年度~令和2年度)、日本学術振興会科学研究費助成事業 基盤研究(A)(研究期間:平成26~28年度、平成29年度~令和元年度)、特別研究員奨励費(研究期間:平成27~29年度、平成30年度~令和2年度)、科学技術振興機構(JST)戦略的創造研究推進事業さきがけ「慢性炎症」における研究課題「内因性リガンドによる進化的に保存された自然免疫活性化機構の解明」(研究期間:平成24~27年度)、および公益財団法人武田科学振興財団・ライフサイエンス研究助成の支援により実施されました。
掲載論文
- 題名
- Neuronal octopamine signaling regulates mating-induced germline stem cell increase in female Drosophila melanogaster
(神経由来のオクトパミンシグナリングが雌ショウジョウバエにおいて交尾依存的な生殖幹細胞の増加を引き起こす) - 著者名
- Yuto Yoshinari(吉成 祐人・筑波大学大学院生命環境科学研究科・日本学術振興会特別研究員)、Tomotsune Ameku(天久 朝恒・筑波大学大学院生命環境科学研究科(当時)・日本学術振興会特別研究員)、Shu Kondo(近藤 周・国立遺伝学研究所・助教)、Hiromu Tanimoto(谷本 拓・東北大学大学院生命科学研究科・教授)、Takayuki Kuraishi(倉石 貴透・金沢大学医薬保健研究域薬学系・准教授)、Yuko Shimada-Niwa(島田 裕子・筑波大学生存ダイナミクス研究センター・助教)、Ryusuke Niwa(丹羽 隆介・筑波大学生存ダイナミクス研究センター・教授)
- 掲載誌
- eLife
- 掲載日
- 2020年10月20日
- DOI
- 10.7554 /eLife.57101
お問合わせ先
研究に関すること
丹羽 隆介(にわ りゅうすけ)
筑波大学 生存ダイナミクス研究センター 教授
取材・報道に関すること
筑波大学広報室
AMEDに関すること
日本医療研究開発機構(AMED)
シーズ開発・研究基盤事業部 革新的先端研究開発課