脳疾患の病因解明と新規細胞治療法に期待
2021-08-26 山梨大学,九州大学,日本医療研究開発機構
概要
山梨大学医学部薬理学、GLIAセンター 小泉修一教授及びパラジュリ ビージェイ特任助教らのグループは、ミクログリア[1]と呼ばれる脳細胞を完全非侵襲的に脳に移植して新しいミクログリアと入れ替える経鼻移植法[2]を開発しました。塩野義製薬株式会社、九州大学中島欽一教授らが協力しました。またヒトiPS細胞[3]から効率良くミクログリア(iPSMG)を作る方法を開発し、このiPSMGを用いた本技術を使ってマウス脳内に移植することで、ミクログリアがヒト細胞に置き替わったヒト化マウス[4]の作製に成功しました。
ミクログリアは疾患の超早期、また老化の初期段階で環境変化を感知・反応する脳細胞で、様々な疾患の発症や進行、さらにエイジングによる脳機能低下に大きく関係するとして非常に注目されています。しかしこれまでの多くの研究はマウス等げっ歯類ならびにそのミクログリアを用いた研究で、ヒトのミクログリアが実際の脳内でどのような働きをし、どのように疾患や老化を制御しているのかについては明らかになっていません。本研究により、ミクログリアが関係する種々の脳疾患、老化の仕組みがヒトミクログリアを使ったin vivo研究(生体と同様環境下での研究)によって明らかになること、さらにはミクログリア移植による新しい「細胞治療法[5]」が開発されることが期待されます。本研究成果は、医学雑誌GLIAに英文原著論文として、2021年7月27日にオンライン版に掲載されました。
論文情報
- 論文タイトル
- Transnasal transplantation of human induced pluripotent stem cell-derived microglia to the brain of immunocompetent mice.
- 著者
- Bijay Parajuli#, Hiroski Saito#, Youichi Shinozaki, Eiji Shigetomi, Hiroto Miwa, Sosuke Yoneda, Miki Tanimura, Shigeki Omachi, Toshiyuki Asaki, Koji Takahashi, Masahide Fujita, Kinichi Nakashima, Schuichi Koizumi*(#同一貢献度の第1著者,*責任著者)
- 掲載誌
- GLIA
- DOI
- 10.1002/glia.23985
背景
最近、グリア細胞と呼ばれる脳細胞が、脳の機能で重要な役割を果たしていることが明らかとなり、大変注目を集めています。特にミクログリアは、脳内外の環境変化に敏感で、種々の脳疾患及び老化の初期に変化を感知することで、疾患発症、進行、さらに老化による機能低下誘導等、変化のスイッチとして重要な役割を果たす細胞として大きな注目を集めています。しかしこれまでのほとんどのミクログリア研究は、マウス等げっ歯類を使ったもので、実際にヒトミクログリアが疾患や老化でどのような役割を果たしているのかは不明のままでした。またミクログリアは敏感な細胞なので、in vitro研究(試験管レベルの研究)で得られた成果は、実際の脳内での働きと大きく違っていることが指摘されていました。しかし、ヒトミクログリアの役割を、ヒト脳を使ったin vivo研究(実際の生体と同様環境下での研究)で行うことは出来ません。そこで本研究では、ヒトiPS細胞からミクログリアを作成し、これをマウス脳内に非侵襲的に移植する技術「経鼻移植法」を開発し、ヒトiPS由来ミクログリア(iPSMG)の働きをマウス脳内で解明することを計画しました。これにより、ヒトミクログリアの働き・役割を脳内で解析することが可能となり、真のミクログリア機能の役割が解明されることが期待出来ます。さらに本移植技術により、病態時の異常ミクログリアや加齢による老化ミクログリアを、正常ミクログリア、若齢ミクログリアに入れ替えることが可能となります。これにより、ミクログリア置換による新しい「細胞治療法」が開発されることが期待できます。
研究成果
今回研究チームは、先ずヒトiPS細胞から効率良く大量のミクログリア(iPSMG)を作る技術を開発しました(塩野義製薬 特許2018-537566)。次にiPSMGをマウス脳内に移植するために、(1)既存のマウスミクログリア除去、(2)従来の外科手術とは異なる完全非侵襲的移植、を組み合わせた移植技術を開発しました。(1)は、図1で示すようにCSF1R拮抗薬[6]を用いました。CSF1R拮抗薬を投与すると(ON)、マウス脳内ミクログリアはほぼ消失し、同薬剤を除去すると(OFF)、ミクログリアは自己再生により元に戻ります。(2)の完全非侵襲的移植には、図2に示すように経鼻移植法を開発しました。マウスの鼻腔にiPSMGを一定時間静置すると、ミクログリアは篩板を通過し、そこから各脳部位に移動、増殖そして定着します。これらを組み合わせ、CSF1R拮抗薬をONからOFFにするタイミングで、iPSMGを経鼻移植することで、元のマウス脳内に存在するミクログリアのほぼすべてをiPSMGと置換することが可能となりました(図3)。経鼻移植されたiPSMGは、極めて安定的な形状を示し移植60日後でもマウス脳内で生着していることがわかり、ミクログリアがヒト細胞に変化した、ヒト化マウスの開発に成功しました(図4)。
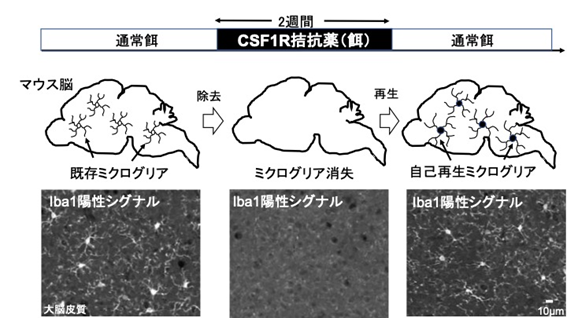
図1 CSF1R拮抗薬のON/OFFによるマウスミクログリアの除去/自己再生CSF1R拮抗薬を餌に混ぜて投与すると、2週間以内にほぼすべてのミクログリアはマウス脳内から消失する(Iba1陽性シグナル)。CSF1R拮抗薬を除去すると、ミクログリアは自己再生しCSF1R拮抗薬投与前とほぼ同数にまで戻る。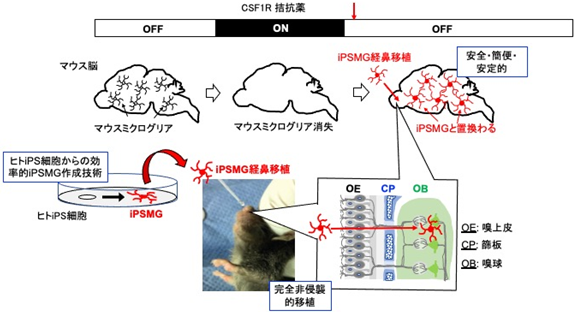
図2 経鼻移植法によるiPSMGの移植CSF1R拮抗薬のONによりマウスミクログリアを除去した後、ヒトiPS細胞から分化誘導したiPSMGを経鼻移植法を用いて完全非侵襲的にマウス脳内に移植する(赤矢印、CSF1RはOFF)。iPSMGを鼻腔内に静置すると、iPSMGは嗅上皮(OE)、篩板(しばん)(CP)を通過し、脳内の嗅球(OB)に到達する。ミクログリアは、ここから各脳部位へ移動し、増殖し、そこで定着する。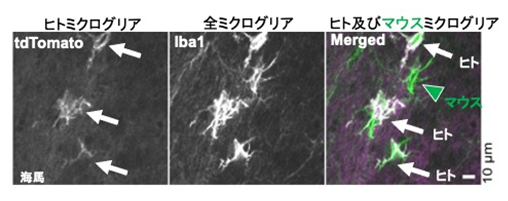
図3 iPSMGの経鼻移植後、ほとんどのミクログリアはiPSMGに置き換わるiPSMG経鼻移植3日後の海馬のミクログリア像。
左図矢印:移植したiPSMG(ヒトミクログリア)
中央図:全ミクログリア(Iba1陽性シグナル)。マウス及びヒトミクログリアが含まれる。
右図:矢印iPSMG(ヒトミクログリア)、緑矢頭(マウス由来ミクログリア)。
ほとんどのミクログリアがiPSMGに置き換わっている。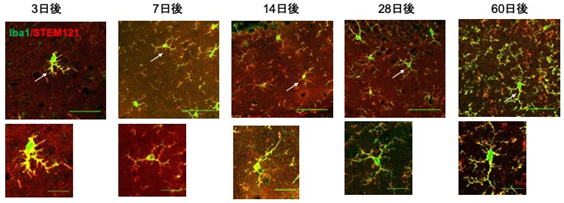
図4 経鼻移植後の海馬iPSMGの形態変化iPSMG(Iba1/STEM121陽性シグナル)の形態は、移植直後は活性化型(短い突起と大きな細胞体)を呈するが、徐々に静止型(長いく細かい突起)へと変化する。移植60日後でも、マウス脳内ミクログリアはほぼiPSMGに置き替わったままで正常に定着しており、ヒト化マウス(ミクログリアがヒト細胞に置き換わった)の状態が維持されていた。
今後の展開
本ヒト化マウスを用いて病態や老化研究を遂行することで、ヒトミクログリアが実際の脳内でどのように機能しているのか、また疾患や老化を如何に制御しているか等、重要な課題が明らかになることが期待できます。さらに今回開発した経鼻移植法は、簡便、安定的、そして外科手術を伴わないため非常に安全な移植法です。CSF1R拮抗薬ON/OFFと組み合わせることで、簡単にマウスのミクログリアをiPSMGに置換することができます。今回はiPSMGへと置換しましたが、任意のミクログリア、例えば若年期のミクログリア、特定の遺伝子を改変したり、薬剤処理を行ったミクログリアへの置換が可能となります。また安全な置換法ですので、ヒトへの応用も比較的早い時期に実現することが期待できます。すでにマウスを使った病態モデルでは、ミクログリアを制御することが疾患治療や、老化抑制に有効であると報告されています。今回の完全非侵襲的ミクログリア置換法は、新しい「細胞治療法」として脳疾患や老化による機能障害に対し、簡単、安全で、革新的な治療戦略となることがと考えられます。
本研究は、科研費 学術変革領域(A)「グリアデコード」(20H05902)(研究代表者:小泉修一)、新学術領域研究「MANネットワークの異常と脳情報動態学研究」(20H05060)(研究代表者:小泉修一)、基盤研究(A)「網膜グリア細胞による眼の生理機能・病態制御機構の解明」(21H04786)(小泉修一)、日本医療研究開発機構(AMED)の革新的先端研究開発支援事業「健康・医療の向上に向けた早期ライフステージにおける生命現象の解明」研究開発領域AMED-CREST(研究開発代表者:中島欽一、研究開発分担者:小泉修一)、三菱財団、武田科学財団及び山梨大学先端脳‐免疫研究助成(小泉修一)による支援を受けて行われました。
用語説明
- [1]ミクログリア
- グリア細胞の1種で脳内では唯一の免疫担当細胞です。脳内・脳外の環境変化に非常に敏感で、それらを感知すると即座に大きく変化して、病気の発症や進行を先導する役割を果たしています。自然免疫細胞として、炎症応答、不要細胞や断片の除去等に加えて、シナプス再編等による神経回路の再構築等でも重要な役割を果たしています。
- [2]経鼻移植法
- 経鼻移植法は、従来の外科手術による方法とは大きく異なり、鼻腔から細胞を脳に届ける最新で完全非侵襲的な細胞移植法です。鼻腔内に細胞を静置するだけで、細胞は篩板という構造を介して脳内に進入することが出来ます。安全、安定的、さらに簡便な移植方法ですが、移植効率が高くないので、大量の移植用細胞を準備する必要があります。
- [3]iPS細胞
- 山中伸弥教授が見いだした多能性幹細胞。皮膚等の体細胞に、特殊な少数の因子を導入し培養すると、それらの細胞は初期化し、様々な組織や臓器に分化する能力、無限に増殖する能力を獲得した多能性幹細胞に変化することが出来ます。これがiPS細胞です。再生治療や疾患解明の切り札になる細胞として期待されています。
- [4]ヒト化マウス
- マウスの遺伝子、細胞、組織の一部がヒトのそれらに置き換わったマウスのこと。今回の例では、マウスの脳内に、ヒトの細胞(ミクログリア;iPSMG)を定着させた細胞レベルでのヒト化マウス。
- [5]細胞治療法
- 自身(或いは他者)の細胞を体外で培養・増殖させ、再度体内に戻して疾患を治療する最新の治療法。細胞そのものを補充するために行う場合もありますが、培養時に鍛えられた細胞が、様々な分子を産生することで、身体の修復機能や自己治癒力を高めることで治療効果を発揮すると考えられています。免疫細胞や間葉系幹細胞を用いた治療法が既に行われています。
- [6]CSF1R拮抗薬
- コロニー刺激因子1受容体(CSF1R)はミクログリアの生存に必須です。このCSF1Rを阻害する薬剤がCSF1R拮抗薬でPLX5622などが知られています。CSF1R拮抗薬のON/OFFで、ミクログリアを可逆的に除去/自己再生させることが可能です(図1参照)。
お問い合わせ先
研究に関する問合せ
国立大学法人山梨大学 医学部
薬理学講座 教授 小泉 修一(コイズミ シュウイチ)
AMED事業に関する問合せ
国立研究開発法人日本医療研究開発機構(AMED)
シーズ開発・研究基盤事業部 革新的先端研究開発課