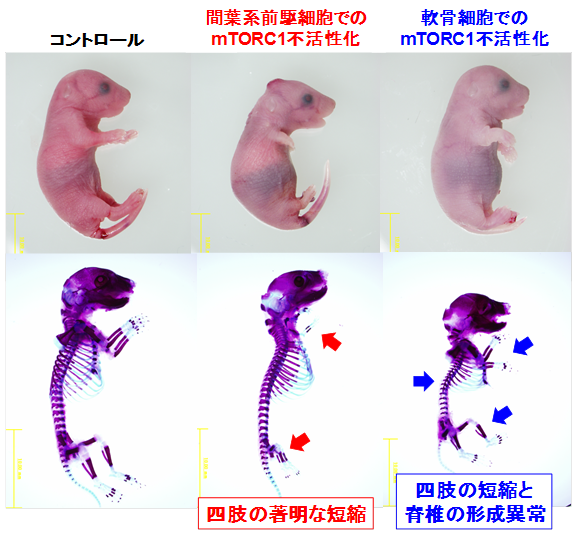
世界初の体外診断用医薬品の開発成功につながるチオプリン製剤の重篤な副作用を予測する日本人に最も適切な遺伝的マーカーを同定
2018-06-29 東北大学病院,株式会社医学生物学研究所,日本医療研究開発機構
発表のポイント
- 東北大学病院 消化器内科 角田洋一助教らの研究グループは、炎症性腸疾患注1、白血病注2、リウマチ性疾患、臓器移植後の治療におけるチオプリン製剤注3の重篤な副作用を予測する、日本人に最も適切な遺伝的マーカーを探索するため、全国32施設による多施設共同研究にて収集された2,630人の炎症性腸疾患の患者DNAを解析し、NUDT15(Nudix Hydrolase 15)遺伝子のコドン注4139が最も適切な遺伝的マーカーであることを示した(参考文献1)。
- 本成果は、科学雑誌『Journal of Gastroenterology』に掲載されるのに先立ち、オンライン版(6月19日)に公開された。
- NUDT15遺伝子のコドン139の遺伝子多型注5を検出するキット(製品名:MEBRIGHT NUDT15 キット)を株式会社医学生物学研究所と共同開発し、世界で初めて体外診断用医薬品として製造販売承認(平成30年4月6日)を取得した。本キットの発売は平成30年7月2日を予定(図1, 2)。
- 本研究は国立研究開発法人 日本医療研究開発機構(AMED)のゲノム創薬基盤推進研究事業「チオプリン不耐例を判別するNUDT15 R139C遺伝子多型検査キットの開発を軸とした炎症性腸疾患におけるゲノム実用化フレームワークの確立」(以下、本研究課題)において行われた。
研究の背景
チオプリン製剤は、炎症性腸疾患を始め、小児の急性リンパ性白血病注6を始めとする白血病、リウマチ性疾患、臓器移植後の治療に効能効果が認められる安価かつ有用な薬剤であり(参考文献2, 3, 4)、日本国内で広く使用されています(参考文献5, 6, 7)。国内における炎症性腸疾患の患者数は約29万人とされ、年々増加の一途を辿っており、その年間新規患者数は約1万5千人と推計されます。また、チオプリン製剤の使用頻度が高い小児急性リンパ性白血病の患者数は約2千人と推計され、年間新規患者数は約600人に上ります。
しかしながら、日本人を含む東アジア人では、チオプリン製剤を投与した一部の患者さんにおいて、早期に重度の白血球減少注7症や全脱毛注8といった重篤な副作用を生じることが知られています。重度の白血球減少症は、致死的な感染症を合併するリスクを増大させることから生命に重大な影響を及ぼし、発見や治療が遅れると患者さんが死亡するケースもあります。また、脱毛は一度発こるとチオプリン製剤の投与中止後も進行し、完全脱毛に至ると回復に数か月以上を要するため、日常生活に著しい影響を及ぼします。
これまではチオプリン製剤による重篤な副作用の事前予測方法がなかったため、慎重に投与するしかありませんでしたが、それにも関わらず一部の患者さんでは重篤な副作用が発症し、治療の中断や入院加療を余儀なくされてきました。また、このような重篤な副作用への懸念からチオプリン製剤による治療法の選択を避けることも少なくありませんでした。
近年、チオプリン製剤の投与による重篤な副作用には、NUDT15遺伝子多型が強く関連していることが発見されました(参考文献8)。NUDT15タンパク質はチオプリン製剤の薬効を示す活性型分子の代謝に関与する酵素であり、その遺伝子多型によって酵素活性が大きく変化します。特にNUDT15遺伝子のコドン139の塩基配列がアルギニンからシステインとなる遺伝子多型を持つ場合、その酵素活性が著しく低下します。複数の研究結果から、NUDT15遺伝子のコドン139の塩基配列がシステインとなる遺伝子多型のみを持つ患者さんは、チオプリン製剤の活性型分子の代謝が抑制され薬効が強く出てしまうため、チオプリン製剤の投与による重篤な副作用のリスクが高いことが報告されています(参考文献9, 10)。さらに、東北大学病院 消化器内科 角田 洋一助教らが中心となって行った本研究課題の分担研究の一つである臨床研究プロジェクト「NUDT15遺伝子多型検査の有用性に関する多施設共同研究」(以下、MENDEL Study)は、日本人の炎症性腸疾患患者さんにおいては、NUDT15遺伝子のコドン139がチオプリン製剤の投与による重篤な副作用を予測するための遺伝的マーカーとして最も有用であることを報告しました(図3)(参考文献1)。
そこで今回、研究グループは、適切な治療選択に結びつけることを目的に、チオプリン製剤の投与による重篤な副作用に関与するNUDT15遺伝子のコドン139の遺伝子多型の情報を正確かつ迅速に提供できる体外診断用医薬品キットの開発を、株式会社医学生物学研究所(研究開発分担者:阿部由紀子)らと共同で行いました。
研究の内容
開発したキット(製品名:MEBRIGHT NUDT15 キット、以下「本キット」)は、患者さんの血液から抽出されたゲノムDNAを検体に用いてNUDT15遺伝子多型を検出する試薬です(図4)。リアルタイムPCR法を原理としており、3種類のアレル(アルギニン、システインもしくはヒスチジンをコードする塩基配列)に対応する蛍光標識プローブの反応から、検体中のNUDT15遺伝子のコドン139の遺伝子多型を検出します(図5)。また、本キットの試薬調製から判定までに必要な時間はおよそ2時間程度であり、多数検体の同時測定も可能なことから、迅速性を特徴としています。
本キットの性能を評価するため、3施設(国立大学法人東北大学病院、医療法人社団 綾和会 浜松南病院、杏林大学医学部付属病院)から160症例の炎症性腸疾患の患者さんを登録し、臨床性能試験を実施しました。対照法としてダイレクトシークエンス法を用い、本キットとダイレクトシークエンス法の判定結果の一致率を解析したところ、160症例の全てで判定結果が一致しました。さらに、本キットの判定結果とチオプリン製剤による重篤な副作用との関連を解析したところ、重度の白血球減少症、全脱毛を発症した患者さんは全員、コドン139がシステインとなる遺伝子多型のみを持つと判定され、それ以外の組み合わせを持つと判定された患者さんでは重篤な副作用を発症していませんでした(図6)。したがって、本キットは迅速かつ正確にNUDT15遺伝子のコドン139の遺伝子多型を検出し、その判定結果と重篤な副作用の発症には非常に強い関連が確認されました。
なお、東北大学東北メディカル・メガバンク機構が構築した3,554人の日本人の全ゲノムリファレンスパネルでは、アルギニンがシステインに変化するアレルが10.5%、ヒスチジンに変化するアレルが0.7%の頻度で確認されています。また、東北大学東北メディカル・メガバンク機構は、バイオバンクとしての役割を担っており、MENDEL Studyで収集された約3千検体の全国の炎症性腸疾患患者さんのDNAの管理を行うことでプロジェクトに貢献しました。今回、本キットの臨床性能試験は、このバイオバンクで保管されているDNA検体を用いて行われました。
研究の意義・今後期待される展開
世界で初めて体外診断用医薬品として製造販売承認され、迅速かつ正確にNUDT15遺伝子のコドン139の遺伝子多型を検出できる性能を有する本キットの開発によって、チオプリン製剤の投与前に重篤な副作用を発症するリスクの高い患者さんを特定できるようになりました。日本人では、重篤な副作用を発症するリスクの高いNUDT15遺伝子のコドン139の塩基配列がシステインとなる遺伝子多型のみを持つ方の割合は、1%程度と報告されています(参考文献11)。チオプリン製剤による治療法を医師が安心して選択できるようになり、また重篤な副作用を恐れてより高額な別の治療法を選択していた患者さんがチオプリン製剤を使うようになることで医療費の適正化にも貢献するものと期待されます(図7, 8)。 またNUDT15遺伝子多型とチオプリン製剤の重篤な副作用は、日本だけでなく、中国、韓国など東アジアを中心に多数報告されているため、日本発の遺伝子検査薬として国際的に貢献することが期待されます。
参考図

図1. 本研究課題の分担研究プロジェクトの紹介

図2. キットの開発と体外診断用医薬品
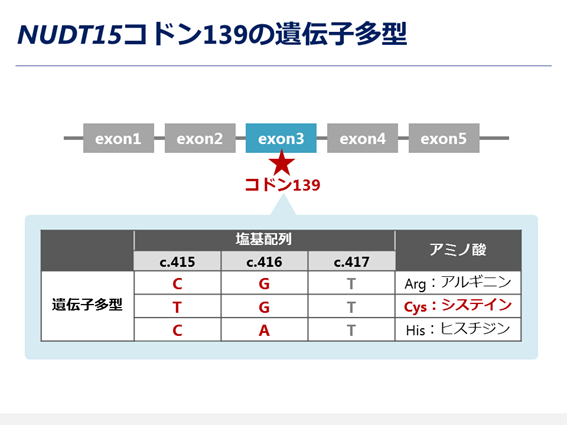
図3. NUDT15コドン139の遺伝子多型

図4. MEBRIGHT NUDT15 キットの概要
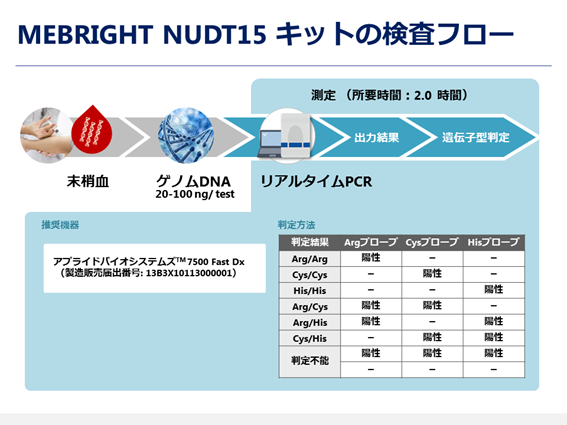
図5. MEBRIGHT NUDT15 キットの検査フロー
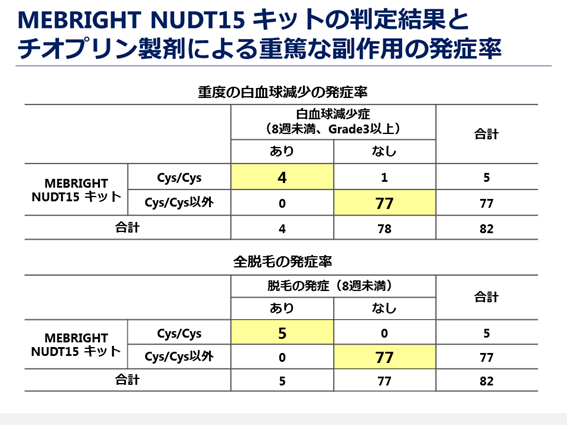
図6. MEBRIGHT NUDT15 キットの判定結果とチオプリン製剤による重篤な副作用の発症率
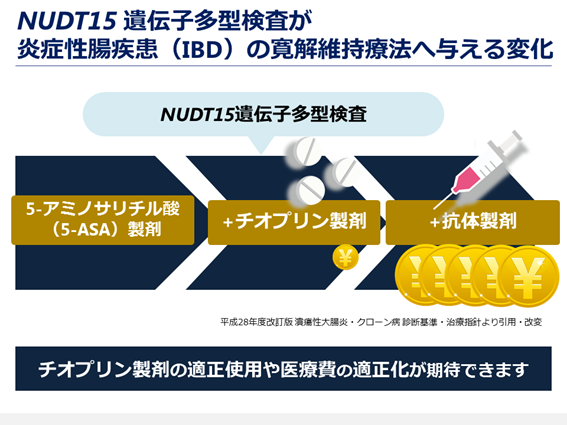
図7. NUDT15遺伝子多型検査が炎症性腸疾患(IBD)寛解維持療法へ与える変化

図8. NUDT15遺伝子多型検査によるメリット
用語説明
- 注1.炎症性腸疾患(Inflammatory Bowel Disease: IBD):
- 炎症性腸疾患は主に潰瘍性大腸炎とクローン病の二つの疾患からなる、大腸及び小腸の粘膜に慢性の炎症や潰瘍が生じる原因不明の難治性炎症性腸管障害です。慢性的あるいは寛解と再燃を繰り返す疾患であり、治療では速やかな寛解導入療法と寛解の維持療法が重要となります。
- 注2.白血病:
- 白血病は急性骨髄性白血病や急性リンパ性白血病に代表される血液のがんであり、血液細胞ががん化し骨髄内で増殖することで正常な血液細胞が減少し、免疫機能の低下、出血、貧血などの症状が現れる疾患です。
- 注3.チオプリン製剤:
- 日本国内で使用されているチオプリン製剤は、アザチオプリンとメルカプトプリン水和物散が存在します。チオプリン製剤は生体内で代謝され、活性型分子(TGTPおよびTdGTP)となって効能・効果を発揮します。NUDT15はチオプリン製剤の代謝関連酵素として、活性型分子の脱リン酸化に関与しています。
- 注4.コドン:
- タンパク質を構成している20種類のアミノ酸に対応する、3個1組の塩基配列のことを言います。1種類のアミノ酸を指定するコドンはアミノ酸の種類によって複数存在するものもあり、生体内での翻訳のステップでは1つのコドンから1つのアミノ酸が合成されます。
- 注5.遺伝子多型:
- 遺伝子を構成しているDNA配列でみられる個人差であり、一般的に人口の1%以上の頻度で存在するものと定義されます。遺伝子多型によって遺伝子の機能が変化する場合があり、病気との関係や薬の効果予測など、臨床に役立つ遺伝的マーカーへの利用が期待されています。
- 注6.急性リンパ性白血病:
- 急性リンパ性白血病はリンパ系幹細胞ががん化した白血病であり、小児の白血病/悪性リンパ腫の70%を占めます。化学療法により大部分の患者が寛解しますが、再発がみられるため、寛解導入療法の後も、2~3年間にわたって強化療法や維持療法が行われます。
- 注7.白血球減少:
- 血中の白血球数が一定基準未満に減少することを指します。白血球の減少に伴い、一般に免疫機能が大幅に低下します。副作用のグレードとして、下記分類があります。
Grade1 Grade2 Grade3 Graed4 範囲(/mm3) <LLN※~3,000 <3,000~2,000 <2,000~1,000 <1,000 ※LLN:(施設)基準値下限
(Common Terminology Criteria for Adverse Events (CTCAE) Version 4.0、有害事象共通用語規準 v4.0 日本語訳 JCOG版(略称:CTCAE v4.0 – JCOG))より引用・改変) - 注8.全脱毛:
- 毛髪、全身の体毛が失われてしまうことを指します。薬剤によって引き起こされる高度の脱毛は、一度発症すると服用を中止しても全脱毛に至る場合があり、回復に長い時間が必要です。そのため、かつらやヘアピースが必要になるなどQOLが大幅に低下します。
参考文献
- Kakuta Y, Kawai Y, Okamoto D, et al., NUDT15 codon 139 is the best pharmacogenetic marker for predicting thiopurine induced severe adverse events in Japanese patients with inflammatory bowel disease: A multicenter study. J Gastroenterol. 2018; (in press).
- アスペンジャパン株式会社. イムラン®錠50mg. 添付文書. 2017年2月改定(第16版)
- 田辺三菱製薬株式会社. アザニン®錠 50mg. 添付文書. 2016年1月改定(第15版)
- 大原薬品工業株式会社. ロイケリン®散10%. 添付文書. 2017年6月改定(第12版)
- 炎症性腸疾患(IBD)診療ガイドライン 2016. 編集 日本消化器病学会. 南江堂2016
- 平成28年度 改訂版 潰瘍性大腸炎・クローン病 診断基準・治療指針. 厚生労働科学研究費補助金 難治性疾患等政策研究事業 「難治性炎症性腸管障害に関する調査研究」(鈴木班) 平成28年度分担研究報告書 別冊
- 小児白血病診療ガイドライン. 日本癌治療学会 がん診療ガイドライン
- Yang SK, Hong M, Baek J, et al., A common missense variant in NUDT15 confers susceptibility to thiopurine-induced leukopenia. Nat Genet. 2014; 46(9):1017-20.
- Kakuta Y, Naito T, Onodera M, et al., NUDT15 R139C causes thiopurine-induced early severe hair loss and leukopenia in Japanese patients with IBD. Pharmacogenomics J. 2016; 16(3):280–5
- Tanaka Y, Kato M, Hasegawa D, et al., Susceptibility to 6-MP toxicity conferred by a NUDT15 variant in Japanese children with acute lymphoblastic leukaemia. Br J Haematol. 2015; 171(1): 109-15
- Kakuta Y, Kinouchi Y, Shimosegawa T., Pharmacogenomics of thiopurines for inflammatory bowel disease in East Asia: prospects for clinical application of NUDT15 genotyping. J Gastroenterol. 2018; 53(2):172-80
問い合わせ先
研究に関すること
東北大学病院 消化器内科
助教 角田 洋一(かくた よういち)
株式会社医学生物学研究所
研究開発本部 遺伝子試薬開発ユニット
ユニット長 阿部 由紀子(あべ ゆきこ)
報道に関すること
東北大学病院 広報室
株式会社医学生物学研究所
総務部 本社総務グループ
グループリーダー 東 成見(あずま まさちか)
AMED事業に関すること
日本医療研究開発機構
基盤研究事業部 バイオバンク課