2022-02-14 京都大学,日本医療研究開発機構
概要
京都大学大学院薬学研究科医薬創成情報科学専攻システムバイオロジー分野の土居雅夫教授と同大学院生の佐々木玲奈、濵田悠貴、鑓水大介らのチームは、京都府立医科大学、京都市立病院、東京医科歯科大学、千葉大学、昭和大学、慶應義塾大学、千寿製薬、理化学研究所との共同研究により、加齢によって生じるドライアイの原因疾患に対し、眼局所のホルモンを制御するイントラクライン機構の発見という独自の新所見に基づいた、新たな作用機序の治療アプローチを見出すことに成功しました。
ホルモンは内分泌腺で作られて標的臓器に届けられます。しかし、ステロイドホルモンについては、イントラクライン機構とよばれるホルモンが血流に放出されることなく、その場で効果を発揮する地産地消型の作用機序があり、1990年代から提唱され注目され続けてきましたが実際の役割が十分にわかっていませんでした。
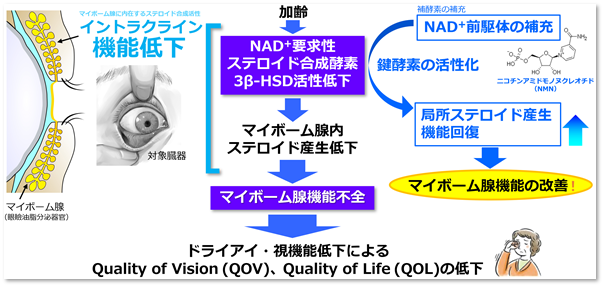
本研究は、このイントラクライン機構を眼のまぶたのマイボーム腺に見つけ、そのホルモン合成酵素の解明に基づいた補酵素点眼療法により、高齢者のドライアイの主原因となる同腺機能不全を改善できることを明らかにしました。マイボーム腺の機能には顕著な日周リズム(サーカディアンリズム)があり、酵素の活性ピーク時刻を狙った投薬が最も有効であることも明らかにしました。
老化メカニズムの解明とその制御は、超高齢化社会において喫緊の課題となっています。なかでも加齢にともなう血中の男性ホルモン/女性ホルモンの減少は、老化にみられる不可避な特徴です。今回の研究では、従来の血中を流れるホルモンではなく、組織局所のイントラクライン機構を操作するというこれまでにはない新しい発想に立った治療薬による加齢性疾患へのアプローチのあり方を初めて示すことができたといえます。
本成果は、2022年2月10日(現地時刻)に米国の国際学術誌「Nature Aging」にオンライン掲載されました。
背景
『イントラクライン』とは、英語で内分泌を表す『エンドクライン』という言葉に対比される言葉です。高校の教科書にも載っている「内分泌」の場合、ホルモンは内分泌腺で作られ 血流に乗って標的臓器へ届けられます。これに対し、イントラクラインは、作られたホルモンは血流に放出されることなく、合成されたその場で作用します。この地産地消に似たホルモンのメカニズムは、1990年代にイントラクラインという名で提唱された重要な概念ですが、実際の生体における役割や病気への関与がよくわかっていませんでした(図1)。
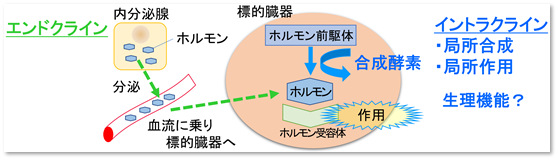
図1 ホルモンの内分泌(エンドクライン)による作用(左)とイントラクラインによる作用(右)の比較
一方、マイボーム腺機能不全(Meibomian Gland Dysfunction: MGD)は、ドライアイ発症の主な要因であり、シェーグレン症候群や抗緑内障点眼長期使用患者、重症オキュラーサーフェイス疾患にも高頻度に併発する病気です。MGDは典型的な加齢性疾患であり、高齢者に発症する割合が高いため、超高齢化社会に向け患者の増加が予測されています。
しかし、なぜ加齢にともなってMGDの発症率が高くなるのか、その根本的な原理を説明する分子機構が全くわかっていませんでした。そのため、現在のMGDの治療はいまだ満足度の低い対症療法にとどまっており、科学的有効性の実証された治療薬は世界的にみても開発が進んでいませんでした。
研究手法・成果
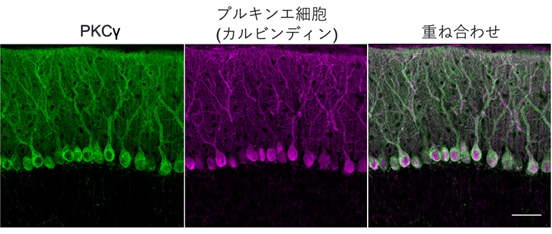
マイボーム腺は、眼のまぶた(瞼)にある生体最大の皮脂腺で、涙液の最表層を形成する脂質を産生する器官です(図2)。研究グループは、まず、ヒトおよびマウスにおいてマイボーム腺の組織形態が加齢により萎縮や脱落をすること(図2)、さらには、ステロイドホルモンを局所で産生するイントラクライン機構がマイボーム腺に存在することをマウスを用いた実験で明らかにし、その活性が加齢により弱まることを示しました(図3)。
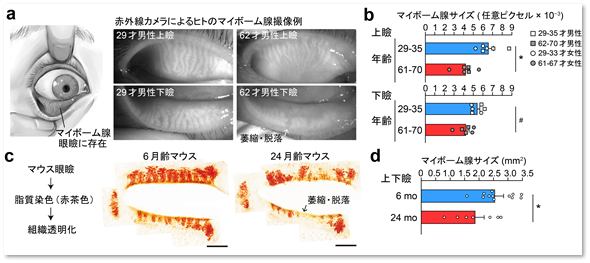
図2 加齢で萎縮するマイボーム腺の組織像とマイボーム腺サイズの統計データ(a、b)ヒト、(c、d) マウス
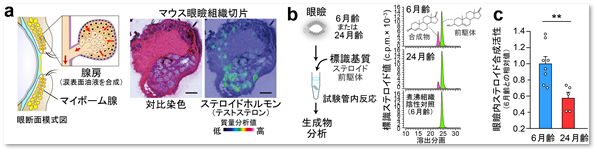
図3 マイボーム腺に検出されたステロイドホルモン(テストステロン)(a)と本組織自身にステロイドを合成する活性が存在することの証明(煮沸失活による活性消失)(b)、加齢によるステロイド合成活性の低下(c)
さらに、研究グループは、マイボーム腺のイントラクライン活性の要となる酵素として、ニコチンアミドアデニンジヌクレオチド(NAD+)*1要求性の3β-ヒドロキシステロイドデヒドロゲナーゼ(3β-HSD)*2を同定しました(図4a、b)。遺伝学的に眼局所の3β-HSDを欠損させると、組織局所のステロイド合成能がなくなり、組織増生に必要な遺伝子群の発現低下とともにマイボーム腺の萎縮とドライアイが発症しました(図4c-e)。つまり、この酵素の活性をうまく取り戻すことがMGDの治療につながるのではないかと考えられます。
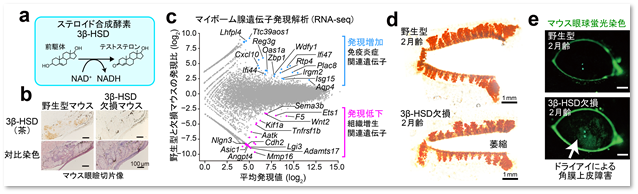
図4 3β-HSD(a)とその欠損(b)によるマイボーム腺の遺伝子発現変化(c)と組織萎縮(d)、ドライアイの発症(e)
研究グループは、さらに、マイボーム腺の3β-HSD活性には昼夜の顕著なリズムがあること(図5)、そして、そのリズムや加齢による活性低下の原因が、酵素自身の発現量の変化ではなく、酵素が触媒反応に用いるNAD+の細胞内濃度変化に依存することを突き止めました(図6)。
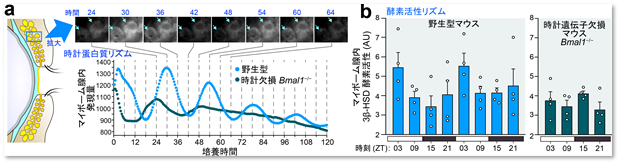
図5 マイボーム腺の腺房に内在する概日時計機能(a)と酵素活性リズム(b):時計遺伝子欠損により消失
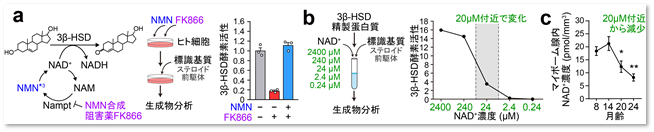
図6 ステロイド合成酵素である3β-HSDは、細胞内で使えるNAD+の量によって酵素活性が大きく変化
実際、ヒトのステロイド産生細胞において、細胞内のNAD+合成を阻害あるいは活性化すると酵素活性が変化すること(図6a)、さらには、試験管内での精製酵素タンパク質を用いた実験においても、生理的濃度のNAD+変化に応じて酵素活性が劇的に変化することを明らかにしました(図6b)。マウスの生体においても、酵素の発現量はあまり変わらないのに対し、マイボーム腺内のNAD+濃度は加齢により減少します(図6c)。
以上の知見をもとに、研究グループは、NAD+のマイボーム腺内濃度を効率よく上げる方法によって MGDの抑制が可能になることを初めて明らかにしました(図7)。
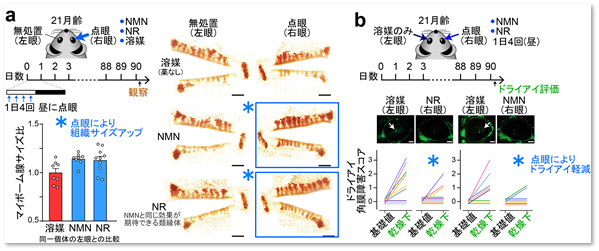
図7 NMN点眼によるマイボーム腺の組織萎縮の回復(a)とドライアイ症状の改善(b)
具体的には、NAD+の生体内前駆物質であるニコチンアミドモノヌクレオチド(NMN)*3を用いて、3β-HSDの酵素活性ピーク時刻をねらった点眼投与を行うことで、マイボーム腺のイントラクライン機構が効率よく再活性化され、それによって、腺細胞の増生とともにドライアイが緩和されることを明らかにしました。
波及効果、今後の予定
研究グループはヒトのマイボーム腺の細胞にもマウスと同一のNAD+要求性3β-HSDが強く発現することを既に見出していることから、今後、ヒトへの臨床応用が期待されます。
いまのところ、ステロイドを直接用いる方法は、副作用や用量用法の問題でまだ成功には至っていません。これに対し、今回のイントラクライン活性化法は、非ステロイドのNMNの投与によって、マイボーム腺の本来あるべき場所で生来のステロイドホルモンを活性化することができるため、副作用などの問題を回避できること、さらには、生体内物質であるNMNの眼局所への時間特異的な投与法であるため、様々な影響を他の臓器に与えてしまうリスクも低いのではないかと考えられます。
MGDのみならず加齢性疾患の解明と制御は、高齢化社会において喫緊の医療課題となっています。なかでも血中のステロイドホルモンの低下は加齢において不可避な特徴です。今回の研究では、従来の血中を流れるホルモンではなく、組織局所のイントラクライン機構を利用するという、これまでにはない発想に立った新しい治療概念による加齢性疾患へのアプローチ法を世界に先駆け示すことができたといえます。
研究プロジェクトについて
本研究は、日本医療研究開発機構(AMED)「老化メカニズムの解明・制御プロジェクト」(JP21gm5010002)、日本学術振興会科学研究費補助金基盤研究(A)(17H01524, 18H04015)、学術変革領域研究(B)(20B307)、小林財団研究助成、京都大学創立125周年記念ファンドくすのき・125の支援を受けて行われました。
用語解説
- *1 ニコチンアミドアデニンジヌクレオチド(NAD+)
- 3β-HSDの補酵素。この他、抗老化に働くSIRTなどのNAD+消費酵素の基質にもなることが知られている。
- *2 3β-ヒドロキシステロイドデヒドロゲナーゼ(3β-HSD)
- 3β-水酸化ステロイド脱水素酵素。テストステロンを含むすべてのステロイドホルモンの合成に必須の鍵酵素。
- *3 ニコチンアミドモノヌクレオチド(NMN)
- NAD+の前駆物質。細胞内でニコチンアミドモノヌクレオチドアデニル転移酵素によりNAD+に変換される。
論文タイトルと著者
- タイトル
- Intracrine activity involving NAD-dependent circadian steroidogenic activity governs age-associated meibomian gland dysfunction.(イントラクライン活性というNADに依存する概日性のステロイドホルモン合成活性が加齢性マイボーム腺機能障害を支配する)
- 著者
- L Sasaki, Y Hamada, D Yarimizu, T Suzuki, H Nakamura, A Shimada, KT Nguyen Pham, X Shao, K Yamamura, T Inatomi, H Morinaga, EK Nishimura, F Kudo, I Manabe, S Haraguchi, Y Sugiura, M Suematsu, S Kinoshita, M Machida, T Nakajima, H Kiyonari, H Okamura, Y Yamaguchi, T Miyake, and M Doi
- 掲載誌
- Nature Aging
- DOI
- 10.1038/s43587-021-00167-8
お問い合わせ先
土居 雅夫(どい まさお)
京都大学大学院薬学研究科・教授
報道・取材に関するお問い合わせ先
京都大学 総務部広報課国際広報室
AMED事業に関するお問い合わせ先
老化メカニズムの解明・制御プロジェクト
日本医療研究開発機構(AMED)
疾患基礎研究事業部 疾患基礎研究課