2023-06-27 農研機構,タカラバイオ株式会社
ポイント
農研機構とタカラバイオ株式会社は、リアルタイムPCR法1)でのウイルス遺伝子検出において、短時間の熱処理および遠心操作のみで血液中のウイルスから核酸を迅速に抽出するとともに、PCR反応を阻害する成分の影響を簡単に除去することができる、血液試料の簡易な前処理法を新たに開発しました。本手法は、都道府県の病性鑑定施設で利用されている「豚熱ウイルス・アフリカ豚熱ウイルス識別検査法2)」や野生イノシシを対象とした「豚熱ウイルス野外株・ワクチン株識別検査法3)」に適用でき、血液や組織乳剤など多様な検体を用いた豚熱・アフリカ豚熱の迅速な検出を可能にすることで、本病の早期摘発や緊急的な防疫措置の発動に貢献することが期待されます。本技術に適した前処理試薬は、令和5年6月28日にタカラバイオ株式会社から発売されます。
概要
豚熱(CSF)は2018年に国内の養豚場で26年ぶりに発生して以降、現在まで発生が続いており、また、野生イノシシでもCSFウイルス陽性の個体が継続して確認されています。一方、アフリカ豚熱(ASF)は国内での発生は認められていませんが、日本や台湾を除くアジア各国で猛威を振るっていることから、その侵入には厳重な警戒が必要です。CSFとASFは、別々のウイルスが原因の異なる病気でありながら、臨床症状が酷似するため、両疾病の鑑別にはそれぞれのウイルスの検出を目的にした遺伝子検査が必要です。
今回、農研機構動物衛生研究部門とタカラバイオ株式会社は共同で、これまでより簡易・迅速に血液等からリアルタイムPCR検査に適した核酸試料を調製する手法を新たに開発しました。我々は既にCSFとASFとを迅速、正確に識別して診断するための検査法(https://www.naro.go.jp/publicity_report/press/laboratory/niah/144474.html)や国内でのCSFの流行に伴い、豚や野生イノシシの免疫力を高めるために利用されるワクチンに含まれるウイルス株と野外で流行するウイルス株とを識別するための検査法(https://www.naro.go.jp/publicity_report/press/laboratory/niah/157752.html)を共同で開発しており、これらの検査法は都道府県が行うCSFおよびASFの病性鑑定に利用されています。しかし、これらの検査ではリアルタイムPCR法でのウイルス検出に適さない血液や保存状態の良くない試料を用いなければならないことも多く、検査に供することのできる試料を調製する前処理に時間を要していました。今回開発した手法を用いると、試料と試薬を混和した後に短時間の熱処理と低速での遠心分離操作をするだけで、試料を検査に適した状態にすることが可能になります。
この手法を、上述の「CSFウイルス・ASFウイルス識別検査法」や野生イノシシにおける「CSFウイルス野外株・ワクチン株識別検査法」に適用すれば、両疾病の迅速な摘発や早期の防疫措置の発動に貢献すると期待されます。なお、本技術に適した前処理試薬は令和5年6月28日にタカラバイオ株式会社から発売されます。
関連情報
予算 : 農林水産省委託研究「安全な農畜水産物安定供給のための包括的レギュラトリーサイエンス研究推進委託事業」(官民・国際連携によるASFワクチン開発の加速化)
問い合わせ先など
研究推進責任者 :
農研機構動物衛生研究部門 所長勝田 賢
研究担当者 :
同 越境性家畜感染症研究領域 研究領域長國保 健浩
同主任研究員西 達也
タカラバイオ株式会社中筋 愛、吉崎 美和、名倉 有一
広報担当者 :
農研機構動物衛生研究部門 研究推進部吉岡 都
タカラバイオ株式会社 広報・IR部
詳細情報
開発の社会的背景
2018年9月に国内の養豚場で26年ぶりとなる豚熱(CSF)が発生して以来、2023年3月7日までに18都県で86例の発生が報告され、また、34都府県で700頭を超える野生イノシシの継続的な感染が確認されています。一方、アフリカ豚熱(ASF)は、国内では未発生ながらも、現在世界的に流行が拡がり、特に東アジアや東南アジアなどの近隣地域では軒並み続発が見られていることから、国内への侵入に対する厳重な警戒が必要となっています。両疾病はともに豚のウイルス性伝染病であり、その強い伝播力と病原性により養豚業に壊滅的な被害を与えることから大変恐れられています。また両疾病とも感染の拡大には、豚だけではなく、野生動物、特にイノシシの関与が強く示唆されており、現在、豚・イノシシ双方を対象とした防疫対応が家畜衛生上の重要な課題になっています。CSFとASFは臨床症状が酷似するため、迅速で高精度な遺伝子検査法により、可能な限り早期に感染を見出し、防疫措置を実施する必要があります。そのため、現在、国や都道府県の病性鑑定施設において、主にリアルタイムPCR法を用いた疑い事例の検査や監視が行われています。
研究の経緯
CSFおよびASFの速やかな検知、摘発のため、現在、農研機構動物衛生研究部門とタカラバイオ株式会社が共同開発した「豚熱ウイルス・アフリカ豚熱ウイルス識別検査法」および「豚熱ウイルス野外株・ワクチン株識別検査法」の普及が進んでいます。両検査法には、豚およびイノシシから採取した血清や臓器乳剤が試料として用いられる一方、赤血球に含まれるヘモグロビン色素に富み、またRNA分解酵素等を多量に含むなどリアルタイムPCR法による遺伝子検出を妨害しがちな血液(全血)の検査には向いておらず検査にかけることができません。そのため血液を試料とする場合、検査前に煩雑で高価な試薬を必要とする核酸の精製工程4)により、被検試料となる核酸のみを回収しておく必要があります。特に、野外で発見あるいは捕獲された野生イノシシから採取した試料には溶血(赤血球の破壊)などによりしばしば色素成分が混入して正確な判定を困難にする場合が多いことから、検査のさらなる迅速化や省力化に向けて、血液から両ウイルスの遺伝子について直接検出を可能にする検査手法の開発が望まれています。
そこで農研機構動物衛生研究部門とタカラバイオ株式会社は、これらの課題を克服する検査手法の開発に共同で取り組みました。
研究の内容・意義
血液試料について、CSFおよびASF検査で用いられているマルチプレックスダイレクトリアルタイムPCR法5)を適用可能にする簡易・迅速な前処理法を開発しました。
被検血液と前処理用試薬を混合し、得られた混合物を98°Cで3分間加熱することでPCR反応を妨害する主要な阻害成分を分解、凝塊化します。これを低速で短時間遠心分離して固相側に分離することにより、液相側に赤血球を含まずヘモグロビン色素の大半が除去された試料が得られます(図1)。これを上記のマルチプレックスダイレクトリアルタイムPCR法に供することで、検出阻害の影響を大幅に低減しつつ、ウイルス遺伝子を高精度で検出できることがわかりました(図2)。
この前処理法では、通常の核酸の精製工程で要する特殊な機器や有機溶剤等の試薬は不要で、また長時間を要する抽出精製を省略することできるため、試料の交差汚染等による誤判定のリスクを減らしながら、核酸増幅に適した試料を調整できます。これを用いて検査を実施することにより、標的となる遺伝子を再現性良く検出することが可能です。またこの方法は、従来の血清や組織乳剤試料にも利用可能なことから、試料の種類によらずに一律に前処理を行うこともでき、多検体処理にも向いています。本手法の開発により、CSFおよびASF検査法の適用範囲が大幅に拡張されるとともに、簡便で効率的な検査が可能となります。
今後の予定・期待
今回開発した検査法は、国が定める特定家畜伝染病防疫指針の診断マニュアルに記載されているリアルタイムPCR法に適した試料の前処理法として活用できるだけでなく、豚やイノシシ以外の畜種についても、リアルタイムPCR法をはじめとする類似の検査において血液やヘモグロビン色素の混入した試料の前処理法としての利用が期待されます。
用語の解説
- 1)リアルタイムPCR法
- 増幅したい遺伝子(標的遺伝子)をはさむように一組の短いDNA鎖を設計し、これを起点にして耐熱性のDNA合成酵素を反復して作用させることにより標的遺伝子を合成、増幅する方法をPCR(polymerase chain reaction)法といいます。このうち、特に標的遺伝子の増幅過程を専用の検出機器でリアルタイムに検出、解析するPCR法をリアルタイムPCR法と呼びます。この方法では、標的遺伝子の増幅過程を連続して観察、記録することで反応開始前の試料に含まれていた標的遺伝子量を定量することが可能なため、定量的PCR(quantitative PCRまたはqPCR)法と呼ばれることがあります。通常のPCR法と違い、反応後に電気泳動を行って標的遺伝子の増幅の有無を確認する必要がないため、検査時間を大幅に短縮できます。
- 2)豚熱ウイルス・アフリカ豚熱ウイルス識別検査法
- 豚熱ウイルスはフラビウイルス科ペスチウイルス属に属し、またアフリカ豚熱ウイルスはアスファウイルス科アスフィウイルス属に属する互いに異なるウイルスです。しかし、両ウイルスは豚やイノシシに外見上極めて類似した症状を引き起こすため、これらをそれぞれ区別して診断する必要があります。農研機構とタカラバイオ株式会社は、これを迅速かつ同時に実施できる検査法を共同で開発し、「豚熱ウイルス・アフリカ豚熱ウイルス識別検査法」として2021年11月に上市しました(詳細は本文に記載のURLをご参照ください)。
- 3)豚熱ウイルス野外株・ワクチン株識別検査法
- 国内で流行する豚熱の防疫を目的として、2019年10月から豚および野生イノシシを対象に豚熱ワクチンが使用されています。そのため野外で検出されたCSFウイルス陽性例がワクチン株によるものか野外株によるものかを簡易、迅速に識別するリアルタイムPCR法の開発が求められたため、農研機構とタカラバイオ株式会社は、これを迅速かつ同時に実施できる検査法を共同で開発し、「豚熱ウイルス野外株・ワクチン株識別検査法」として2022年3月22日に上市しました(詳細は本文に記載のURLをご参照ください)。現在、本製品は「CSFウイルス陽性」と判定された野生イノシシの検査に利用されています。
- 4)核酸の精製工程
- 検査対象となる検体(ウイルスや細菌、細胞などを含む)から核酸(DNAまたはRNA)を抽出した後、核酸以外の不純物を取り除くための試料の前処理工程のひとつ。ウイルスの核酸はウイルス粒子を構成するタンパク質の殻や脂質から成る膜に覆われているため、ウイルス遺伝子の検出にあたってはこれらを取り除き、核酸を取り出す工程が必要です。
- 5)ダイレクトマルチプレックスリアルタイムPCR法
- リアルタイムPCR法のうち、一度の増幅反応で複数の標的遺伝子を同時に増幅・識別・検知できるPCR法をマルチプレックスリアルタイムPCR法と呼びます。この際、被検試料として未精製の試料(血液、血清、組織乳剤等)を直接反応液に添加して増幅を行う方式のPCRをダイレクトマルチプレックスリアルタイムPCR法と呼んでいます。
参考図

図1 血液試料の前処理手順
血液と前処理用試薬を混合した後、熱処理と遠心分離をすることによって、血球の不溶成分や色素成分が大幅に除去された試料が得られる。得られた上清は直接リアルタイムPCR反応に供することが可能。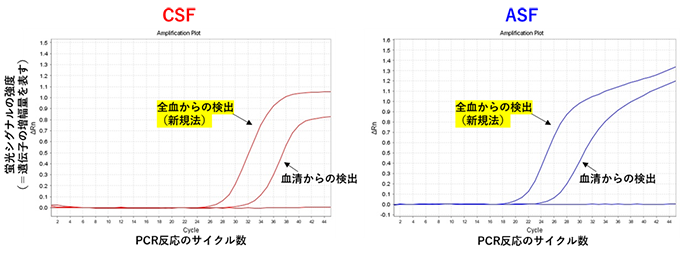
図2 新しい前処理方法を用いた全血試料からのウイルス遺伝子の検出
豚熱(CSF、左)およびアフリカ豚熱(ASF、右)に感染した豚から採取した血清と本前処理法で調整した血液を被検試料としてマルチプレックスダイレクトリアルタイムPCR法に供した。CSFおよびASFの原因ウイルスはともに血清よりも血球中に多く含まれることから、CSFおよびASFに感染したそれぞれ同一の個体から得た検体を検査に供する場合、従来の前処理法により血清を被検試料として検出する場合(従来法)よりも血球成分を含む血液(全血)を被検試料として検出する場合(新規法)の方が、検出効率が向上する(増幅曲線が左方へ移る)。


