2026-05-12 シンガポール国立大学(NUS)

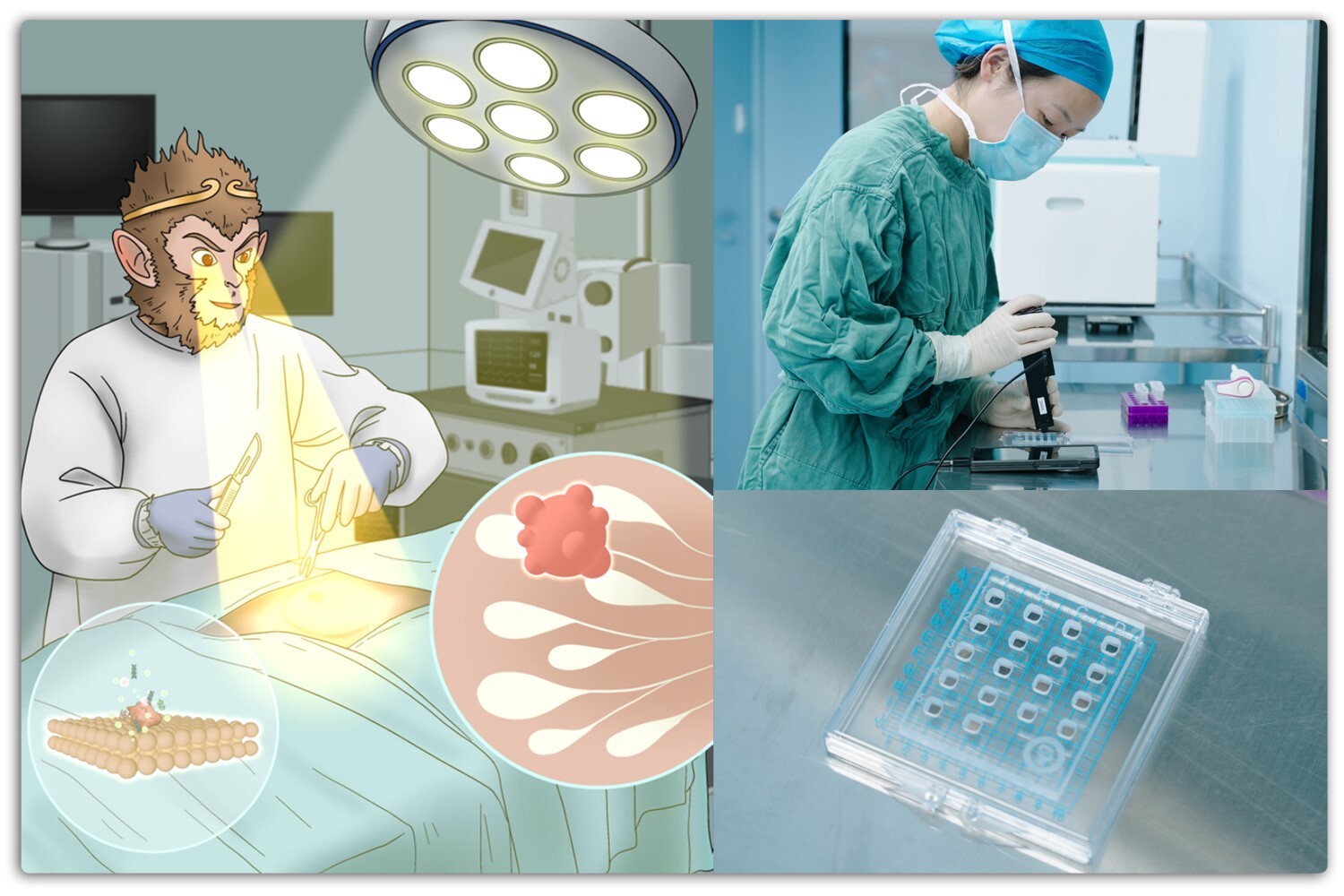
By tagging nanoparticles with unique DNA “barcodes”, the NUS research team was able to track and compare dozens of designs simultaneously in living tumour models, rapidly identifying those most effective at reaching mitochondria (energy centres inside cancer cells).
<関連情報>
- https://news.nus.edu.sg/dna-barcodes-help-nus-researchers-pinpoint-gold-nanoparticles/
- https://advanced.onlinelibrary.wiley.com/doi/10.1002/adma.202517706
腫瘍ミトコンドリア標的化のための金ナノ粒子のハイスループット生体内細胞内分析 High-Throughput In Vivo Subcellular Analysis of Gold Nanoparticles for Tumor Mitochondrial Targeting
Xingyue Huang, Xuehao Tian, Kuei Chen, Yang Wu, ChenCheng Xue, Yingjie Quek, Jessalyn Low, Arun Kumar, Andy Tay
Advanced Materials Published: 17 February 2026
DOI:https://doi.org/10.1002/adma.202517706
ABSTRACT
Mitochondrial targeting is a powerful strategy for cancer precision therapy. This study presents a subcellular DNA barcoding system for high-throughput in vivo screening of mitochondrial-targeting gold nanoparticles (NPs). After validating the robustness of the barcode system with six PEG/TPP‑modified NPs in vitro, the materials library expands to 30 NP species differing in shape, size, and ligand. Their biodistributions are systematically evaluated across subcutaneous, orthotopic, and contralateral tumor models at organ, cell-subtype, and mitochondrial levels. This multiplexed approach yields more than 1000 data points on in vivo nanoparticle uptake and targeting behaviors, while requiring 30-fold fewer mice than conventional approaches. The data reveal a strong correlation between tumor accumulation and mitochondrial delivery, indicating that effective tumor accumulation is a prerequisite for mitochondrial targeting. 80 nm cube (CL‑FA) and sphere (PL‑FA) nanoparticles tagged with folic acid (FA) emerge as top performers, with CL‑FA achieving 99% tumor regression when combined with mild photothermal therapy and mitochondria-targeted siRNA delivery. Underlying mechanisms are attributed to geometry-dependent protein corona formation patterns and cellular uptake via clathrin‑mediated endocytosis and specific curvature‑sensing protein interactions. Overall, this subcellular high-throughput barcoding platform offers a rational framework to select inorganic nanomaterials for precision subcellular drug delivery.