慢性閉塞性肺疾患:COPD(タバコ病)に、有害な鉄による脂質酸化依存的細胞死が深く関与する病態機序を解明
2019-07-18 東京慈恵会医科大学,北里大学,日本医療研究開発機構
研究成果のポイント
- COPD(慢性閉塞性肺疾患、通称“タバコ病”)は全世界で約2億人以上が罹患し、死亡原因第4位の病気です。
- COPD患者の肺の組織には鉄の過剰な蓄積があり、肺上皮細胞(注1)の鉄依存性の脂質酸化依存的細胞死(フェロトーシス)を引き起こすことで病態形成に関与することを証明しました。
- 過剰な鉄は、タバコの煙によって誘発される鉄特異的オートファジー(注2)であるフェリチノファジーによってさらに有害な遊離鉄(注3)に分解され、病態を悪化させる機序を解明しました。
- 根本的治療法のなかったCOPDに対する新たな予防法・治療薬の開発につながる研究成果です。
概要
東京慈恵会医科大学呼吸器内科 桑野和善教授、皆川俊介講師、吉田昌弘大学院生及び北里大学薬学部 今井浩孝教授らの研究グループは、喫煙によって有害な遊離鉄の産生が亢進し、肺上皮細胞の脂質酸化依存的な細胞死(フェロトーシス)につながることがCOPD病態形成に深く関与することを明らかにしました。本研究は文部科学省科学研究費補助金、新学術領域「ダイイングコード」「リポクオリティ」及び国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業(AMED-CREST)の支援で行われ、研究成果は英科学誌「Nature communications」オンライン版に2019年7月17日午前10時(ロンドン時間)に発表されます。
研究の背景
COPDは主に喫煙が原因の、慢性進行性の気管支閉塞と肺気腫を呈する難治性の病気です。2015年のWHOの調査では全死因の第4位ですが今後第3位になると予測されており、医療経済的にも重要な疾患です。タバコなどの煙を長期間吸い込むことで、咳、痰、呼吸困難を引き起こし、禁煙後も老化とともに進行します。現時点において気管支を拡張させて症状を和らげる薬はありますが、COPDの病態解明は十分になされておらず、予後を著明に改善させる有効な薬物療法の開発は遅れていました。
COPDに罹患した患者の肺(以下、COPD肺)では、喫煙により肺の上皮細胞が傷害され、細胞死が起こっていることは報告されていましたが、その機序は十分には解明されていませんでした。
研究の経緯
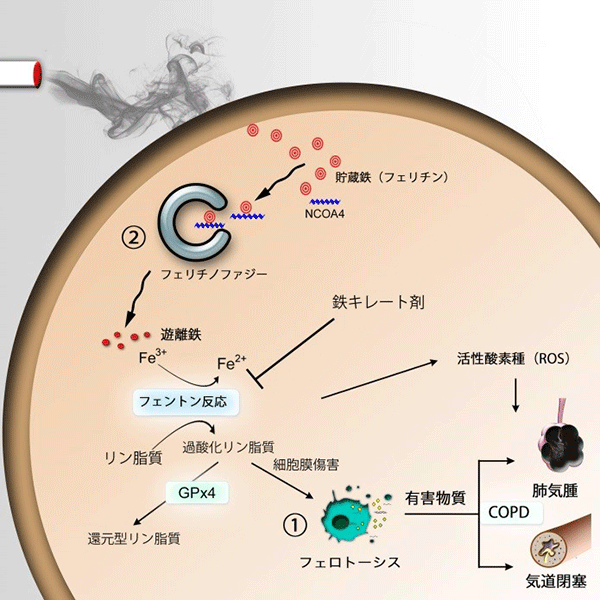
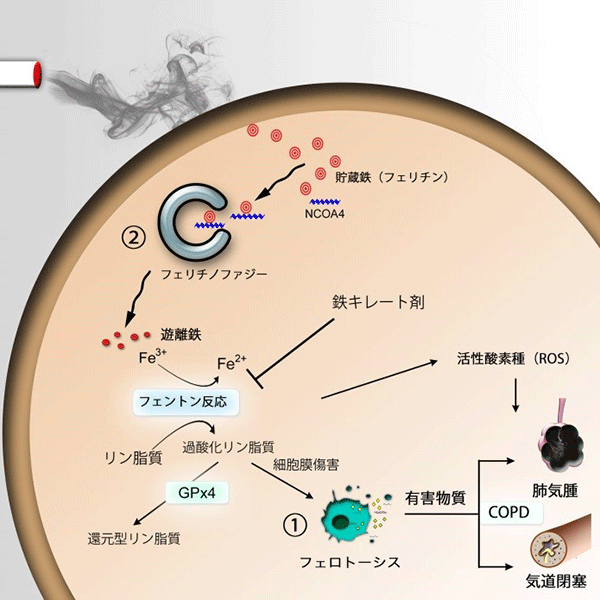
これまで細胞死は、偶発的なものと考えられていましたが、高度にプログラムされた計画的な細胞死が存在することが明らかとなってきました。その代表的な細胞死がアポトーシスという細胞死で、これまでCOPDとの関連も報告されていました。近年新たな細胞死の形態として、鉄依存性の細胞死であるフェロトーシスが報告されました。フェロトーシスは、細胞内の有害な遊離鉄によって細胞膜を構成する脂質が酸化反応を起こし、細胞死を引き起こすというものです。我々は、COPD肺に鉄の過剰な蓄積が起こっていることに着目し、フェロトーシスが喫煙によって誘導されることを証明しました(図中①)。また細胞内の鉄は、フェリチンという安定、無害な状態で通常貯蔵されていますが、オートファジー機構(細胞内タンパクの分解機構)によって有害な遊離鉄へと分解されることを明らかにしました(図中②)。このフェリチンを特異的に分解するオートファジーはフェリチノファジーと呼ばれており、NCOA4という積み荷タンパクにフェリチンを乗せてオートファジー機構へ運搬することが知られています。今回肺上皮細胞においてNCOA4を不活性化すると細胞死が減少し、COPD形成を抑制する結果が示されました。さらにフェロトーシス経路の核となる脂質の酸化反応を抑制するGPx4というタンパクに着目し、このGPx4発現低下(不活性化)マウスおよび高発現マウスを用いて、タバコ喫煙暴露の実験を行いました。GPx4高発現マウスでは、通常のマウスに比べてCOPDの病態形成が軽減され、GPx4発現低下マウスではCOPD病態が悪化しました。
研究結果の意義
本研究によって、COPD病態形成における、これまで報告されていた機序とは全く異なる新しいプロセスが、細胞レベルならびに分子レベルで明らかになりました。この結果を踏まえて、これまで根本的治療法のなかったCOPDに対する新たな予防法・治療薬の開発が進むものと期待されます。
用語解説
- (注1)肺上皮細胞;
- 気管支や肺胞の最上層を構成する細胞。タバコの煙や外気に直接暴露される細胞であり、様々な刺激からの防御、他の細胞への情報伝達などにも重要な細胞。
- (注2)オートファジー;
- 2016年大隅 良典教授がノーベル医学生理学賞を受賞したことでも知られる、細胞内のタンパク分解機構。不要な細胞の中にある小器官やタンパク質を分解して再利用するシステムと考えられているが、環境によっては有害となる報告もある。
- (注3)
- 鉄は細胞内で貯蔵用タンパク質であるフェリチンに結合した状態で保存されているが、これが様々な機序で分解されると有害な遊離鉄(鉄イオン; Fe2+)を産生する。細胞内では通常このフェリチンと遊離鉄のバランスが保たれている。
研究支援
※本成果は、以下の研究課題によって得られました。
国立研究開発法人日本医療研究開発機構(AMED)の革新的先端研究開発支援事業ユニットタイプ(AMED-CREST)
「画期的医薬品等の創出をめざす脂質の生理活性と機能の解明」研究開発領域(研究開発総括:横山信治)
研究開発課題名:酸化脂質をターゲットとした疾患メカニズム解明および創薬基盤研究
研究開発代表者:山田健一
研究開発期間:2017年度~2022年度
お問い合わせ先
内容に関するお問い合わせ先
東京慈恵会医科大学
内科学講座呼吸器内科講師 皆川 俊介(ミナガワ シュンスケ)
北里大学
薬学部衛生化学教授 今井 浩孝(イマイ ヒロタカ)
報道に関するお問い合わせ先
学校法人慈恵大学経営企画部広報課
学校法人北里研究所総務部広報課
AMED事業に関するお問い合わせ先
国立研究開発法人日本医療研究開発機構(AMED)
基盤研究事業部 研究企画課