難病治療薬の開発に向けた一歩
2020-12-08 東京医科歯科大学,日本医療研究開発機構
研究成果のポイント
- 研究グループがこれまでに独自に開発した次世代核酸医薬である「DNA/RNAヘテロ2本鎖核酸(HDO)※1」を発展させ、革新的な次世代核酸医薬である「DNA/DNA 2本鎖核酸」を開発しました。
- DNA/DNA 2本鎖核酸は、1本鎖DNAであるアンチセンス核酸※2に相補的なDNA鎖を結合した2本鎖構造で、マウスの肝臓においてアンチセンス核酸の標的遺伝子抑制効果を飛躍的に向上させることに成功し、また近年核酸医薬で課題となっている副作用を回避する方法の一つとなります。
- DNA/DNA 2本鎖核酸は基盤技術であり、RNA(mRNA、pre-mRNA、マイクロRNAなど)を標的とする様々な疾患への治療薬としての応用が可能です。将来的にB型肝炎、非アルコール性脂肪肝炎(NASH)、アルツハイマー病などのこれまで治療法のなかった難治疾患への応用が期待されます。
概要
東京医科歯科大学大学院医歯学総合研究科脳神経病態学分野(脳神経内科)の横田隆徳教授、永田哲也プロジェクト准教授、吉岡耕太郎特任助教、浅見裕太郎大学院生らの研究グループは、アイオニス・ファーマシューティカルズ社(IONIS Pharmaceuticals)との共同研究で、RNAを標的とした従来のアンチセンス核酸医薬の効果を飛躍的に向上する新技術の開発に成功しました。この研究は日本医療研究開発機構(AMED)の先端的バイオ創薬等基盤技術開発事業における研究課題「次世代血液脳関門通過性ヘテロ核酸の開発による脳神経細胞種特異的分子標的治療とブレインイメージング」(研究代表者:横田隆徳)などの支援のもとでおこなわれたもので、その研究成果は、国際科学誌Molecular Therapyに、2020年12月7日午前11時(米国東部時間)にオンライン版で発表されます。
研究の背景
アンチセンス核酸は細胞内のRNAを治療標的とし、従来の低分子量化合物や抗体等の医薬品では制御が難しい細胞内の遺伝子を標的にして治療するための有望な技術です。近年複数のアンチセンス核酸が臨床応用されており、臨床試験も数多く行われています。
研究グループは、従来のRNAを標的とした1本鎖アンチセンス核酸の効果を大幅に向上できるDNA/RNAヘテロ2本鎖核酸(2015年8月11日東京医科歯科大学プレスリリース)を開発しました。さらにこの技術を実用化に向けて開発するため、東京医科歯科大学発のバイオベンチャーとして「レナセラピューティクス株式会社(レナ社)」が設立されました。その後、レナ社から日米の大手製薬企業に次々とヘテロ2本鎖核酸技術(2018年12月26日東京医科歯科大学プレスリリース)がライセンスアウトされています。
一方で、DNA/RNAヘテロ2本鎖核酸が効果を発揮するには、標的細胞内でDNA/RNAの2本鎖を切断する酵素であるRNaseH※3によりRNA相補鎖が切断されることが必要となります。このため、これまでは2本鎖核酸のデザインが限られていました。そこで、これを改善してより臨床応用に近づけるためにDNA/DNA 2本鎖核酸を新規に考案しました。DNA分解酵素の細胞内外における発現の違いからDNA相補鎖を用いたDNA/DNA 2本鎖核酸が細胞内でのみ治療効果を発揮するとの仮説を立て、検証を行いました。
研究成果の概要
アンチセンス核酸にDNAを基本構造とする相補鎖を結合したDNA/DNA 2本鎖核酸を合成し、相補鎖にビタミンE誘導体を結合してマウスの静脈内に投与すると、1本鎖アンチセンス核酸に比べて肝臓の標的RNAを顕著に抑制し(図右)、血中のLDLコレステロールも有意に低下させることがわかりました。遺伝子抑制効果の向上は、複数の標的RNAに対して証明され、元となるアンチセンス核酸の長さや化学修飾を変えても保たれたことから、様々な標的遺伝子に対して応用が可能であると考えられました。また、DNA相補鎖はRNA相補鎖に比べて肝臓内でより速く分解されており、DNA/DNA 2本鎖核酸は細胞内でDNA/RNAヘテロ2本鎖核酸とは異なるタンパク質に認識されたり代謝を受けたりしていると考えられ、生物学的にも異なった意義を持っていることが示唆されました。また、近年核酸医薬で臓器障害やサイトカイン上昇などの副作用が問題となっていますが、DNA/DNA 2本鎖核酸はマウス投与後の肝臓や腎臓への障害はなく、サイトカイン上昇も認められませんでした。
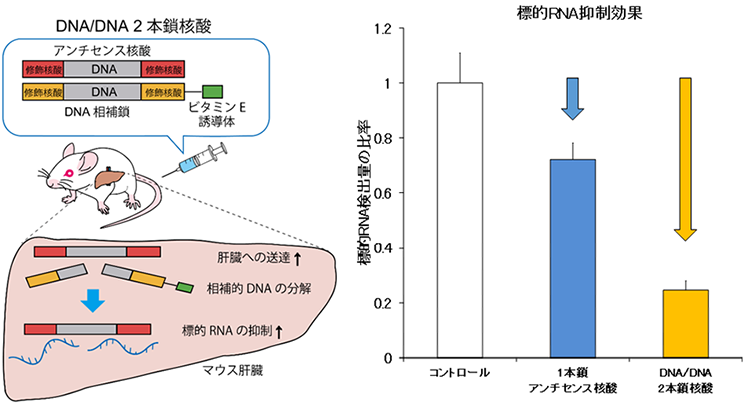
図:(左)DNA/DNA 2本鎖核酸をマウスに静脈投与した際の肝臓の標的遺伝子(RNA)抑制の概念図。(右)DNA/DNA 2本鎖核酸は従来の1本鎖アンチセンス核酸の標的RNA抑制効果を飛躍的に向上させた(図は代表例)
研究成果の意義
核酸医薬は近年副作用が問題になっており、DNA/DNA 2本鎖核酸はその副作用を回避できる方法の一つとして期待されています。また、DNA/DNA 2本鎖核酸がアンチセンス核酸の効果を飛躍的に高めることから、従来の核酸医薬の構造の概念が拡張され、これは今後の治療薬としての臨床応用に向けて重要な知見となります。さらに、DNAはRNAよりも化学的に安定で扱いやすく製造コストが安いため、2本鎖核酸の製剤化にあたって優位性があると考えられます。DNA/DNA 2本鎖核酸はあらゆるアンチセンス核酸医薬に応用が可能な基盤技術であるため、将来的にB型肝炎、NASH、アルツハイマー病などの今まで治療が困難であった疾患への臨床応用が見込まれます。
用語解説
- ※1 DNA/RNAヘテロ2本鎖核酸(HDO)
- 核酸医薬としての活性を有するDNA核酸分子(DNA鎖)に対して相補的なRNA鎖を結合させたDNA/RNAヘテロ2本鎖構造を有する、新規構造の核酸医薬技術。研究グループが独自に開発し、一般的に核酸医薬の主流であるsiRNA(small interfering RNA)、アンチセンス核酸に続く、第3の核酸医薬技術として注目されている。
- ※2 アンチセンス核酸
- 細胞内に存在するRNA(mRNA、pre-RNA、miRNAなど)を標的とする核酸医薬で、DNA鎖を基本構造とし様々な化学修飾が施されている。既存の低分子医薬や抗体医薬では標的にできない細胞内のRNAを標的にして、その標的RNAから翻訳される疾患に係わるタンパク質量を一過性に低下させ機能を抑制することができることから、これまで治療法のなかった疾患の治療薬として注目されている。主な承認薬として脊髄性筋萎縮症に対するヌシネルセンや家族性ポリアミロイドニューロパチーに対するイノテルセン(米国、欧州)などがあり、現在も複数の臨床治験が進行中である。
- ※3 RNaseH
- 主に細胞の核内に存在し、DNA/RNA 2本鎖構造を認識してそのRNA鎖のみを切断する酵素。
論文情報
- 掲載誌
- Molecular Therapy
- 論文タイトル
- Efficient Gene Suppression by DNA/DNA Double-Stranded Oligonucleotide In Vivo
研究者プロフィール
横田隆徳(ヨコタタカノリ) Takanori Yokota
東京医科歯科大学 大学院医歯学総合研究科
脳神経病態学分野 教授
永田哲也(ナガタテツヤ) Tetsuya Nagata
東京医科歯科大学 大学院医歯学総合研究科
脳神経病態学分野 プロジェクト准教授
吉岡耕太郎(ヨシオカコウタロウ) Kotaro Yoshioka
東京医科歯科大学 大学院医歯学総合研究科
脳神経病態学分野 特任助教
浅見裕太郎(アサミユウタロウ) Yutaro Asami
東京医科歯科大学 大学院医歯学総合研究科
脳神経病態学分野 大学院生
研究領域:神経内科学、核酸医薬
お問い合わせ先
研究に関すること
東京医科歯科大学大学院 医歯学総合研究科
脳神経病態学分野 横田隆徳(ヨコタタカノリ)
報道に関すること
東京医科歯科大学 総務部総務秘書課広報係
AMED事業に関すること
国立研究開発法人日本医療研究開発機構(AMED)
創薬事業部 医薬品研究開発課 先端的バイオ創薬等基盤技術開発事業担当