2021-08-11 理化学研究所
理化学研究所(理研)環境資源科学研究センター統合メタボロミクス研究グループの中林亮研究員(研究当時、現客員研究員)、斉藤和季グループディレクターらの共同研究グループは、新しく開発したメタボロミクス[1]の解析法を用いて、アスパラガスの代謝物アスパラプチンAの生合成経路、中間体および類縁体を明らかにし、またアスパラプチンAに血圧降下作用があることを示しました。
本研究成果は、アスパラプチンAが健康維持や医療現場で活用されること、高機能アスパラガスの品種改良などに貢献するものと期待できます。
今回、共同研究グループは、13C[2]標識および非標識のメタボローム[1]データのMS/MSスペクトル[3]の類似性を一斉に解析する手法を新たに開発しました。13Cで標識したバリンを用いて培養したアスパラガスのカルス[4]と通常条件で培養したカルスのメタボロームを、液体クロマトグラフィー-タンデム質量分析(LC-MS/MS)[5]装置で測定しました。得られたMS/MSスペクトルの類似性のネットワーク解析を実施し、13C標識および非標識の代謝物由来のイオンの網羅的なペアリングを行いました。その結果、①アスパラプチンAの生合成の出発物質がバリンであること、②生合成中間体がS-(2-carboxy-n-propyl)-cysteineであること、③2種類の類縁体アスパラプチンBおよびCの存在が明らかになりました。さらに、④アスパラプチンAが高血圧モデルマウスに対して血圧降下作用があることが分かりました。
本研究は、科学雑誌『Journal of Agricultural and Food Chemistry』(8月4日号、オンライン版7月16日付)に掲載され、本誌のSupplementary Coverに選出されました。

アスパラガスのカルス(左)とアスパラプチンAの構造式(右)
背景
世界中で生産されている主要な野菜の一つであるアスパラガスには、血圧の上昇を抑制する作用があることが分かっており、その成分の一つとしてニコチアナミン[6]が知られています。
中林亮研究員らは、これまでに含硫黄代謝物を標的としたメタボローム解析注1)により、アスパラガスからアスパラプチンという代謝物を発見し、この成分が血圧の調節因子の一つであるアンジオテンシン転換酵素(ACE)[7]の阻害活性を示すことを明らかにしました注2-3)。今回、共同研究グループは、質量分析、安定同位体標識、MS/MSスペクトルの類似性解析を組み合わせたメタボローム解析において、アスパラプチンの生合成経路、中間体および類縁体の一斉解析を試みるとともに,アスパラプチンの血圧降下作用を調べました。
注1)2013年1月17日レスリリース「硫黄を含んだ代謝物を網羅的に解析する「S-オミクス」を確立」
注2)2015年5月26日プレスリリース「血圧上昇に関与する酵素を阻害する新規含硫黄代謝物を発見」
注3)特許6735518号「新規アンジオテンシン転換酵素阻害剤」
研究手法と成果
共同研究グループはまず、アスパラプチンの構成因子の一つと考えられる含有硫黄カルボン酸のアスパラガス酸がアミノ酸のバリンから生合成される可能性を考慮し、13Cで標識したバリンで培養したアスパラガスのカルスと、非標識(12C)のバリン(通常条件)で培養したアスパラガスのカルスのメタボロームデータを、液体クロマトグラフィー-タンデム質量分析(LC-MS/MS)を用いて網羅的に取得しました。これらのデータを多変量解析手法[8]の一つであるS-プロット[8]で解析したところ、それぞれのサンプルの代謝物由来のイオンはきれいに分離しました(図1)。これは、アスパラガスカルス中のバリン由来の代謝物に13C標識バリンの13Cが取り込まれたことを示しています(図1)
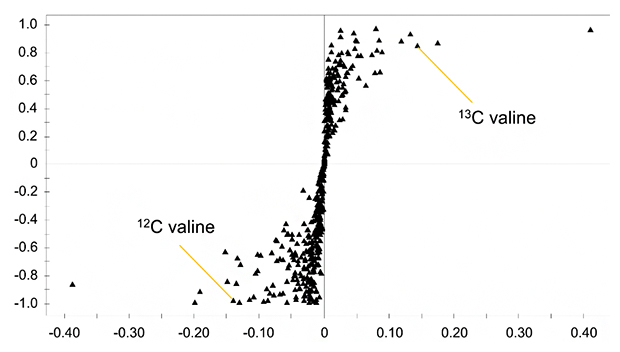
図1 13C標識および非標識メタボロームデータを用いたS-プロット
各▲は代謝物由来のイオンを表す。左右の位置の違いは、バリン由来の代謝物が存在することを示す。(Reprinted with permission from Nakabayashi et al., J. Agric. Food Chem., 10.1021/acs.jafc.1c01183. Copyright (2021) American Chemical Society.)
次に、これらのデータを用いてMS/MSスペクトルの類似度によるペアリングを行いました。13C標識の代謝物と非標識の代謝物は、質量電荷比(m/z)の値以外はほぼ類似した開裂パターンを示します。この点に着目し、得られたイオンを類似性でペアリングし、類似性によるネットワークを構築しました(図2)。このペアリングを用いることで、バリン由来の代謝物のイオンの存在を自動的に判断することができます。構築したネットワークに、アスパラプチン、中間体および類縁体に関係するイオンのペアがあることが分かりました。
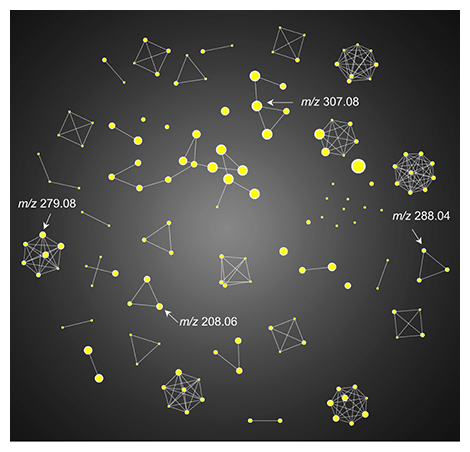
図2 13C標識および非標識メタボロームデータのMS/MSスペクトルの類似性解析
黄色の〇は、13C標識および非標識代謝物由来のイオンのペアを表す。〇をつなぐ線は類似性を表す。(Reprinted with permission from Nakabayashi et al., J. Agric. Food Chem., 10.1021/acs.jafc.1c01183. Copyright (2021) American Chemical Society.)
これらのMS/MSスペクトルのペアを用いて構造解析した結果、アスパラプチンのasparagusyl基がバリン由来であること、また、生合成中間体として考えられていたS-(2-carboxy-n-propyl)-cysteineの2-carboxy-n-propyl基もバリン由来であることが分かりました。
さらに、残りの代謝物に関するイオンのペアについても解析しました。MS/MSスペクトルから、これらの代謝物はアミノ酸のリジンあるいはヒスチジンとアスパラガス酸との結合体であることが考えられました。そこで、13Cリジンあるいは13Cヒスチジンと13Cバリンで培養したアスパラガスカルスのメタボロームデータを取得し、そのMS/MSスペクトルを構造解析に加えました。解析の結果、これらの代謝物は新規であり、アスパラプチンの類縁体であることが明らかとなりました。そこで、元のアスパラプチンをアスパラプチンAと改名し、リジン型をアスパラプチンB、ヒスチジン型をアスパラプチンCと命名しました。
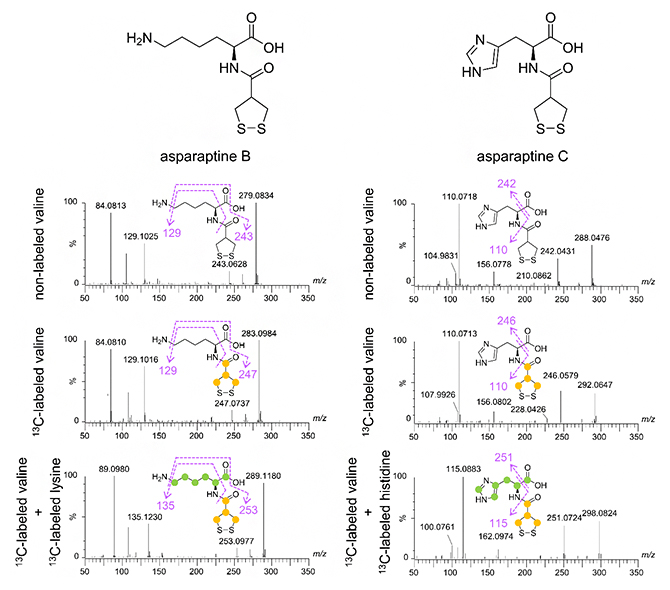
図3 アスパラプチンBおよびCの構造解析
黄色の〇は、13C標識バリン由来、緑の〇はリジンあるいはヒスチジン由来であることを示す。(Reprinted with permission from Nakabayashi et al., J. Agric. Food Chem., 10.1021/acs.jafc.1c01183. Copyright (2021) American Chemical Society.)
最後に、アスパラプチンAは試験管内においてACEに対する阻害活性を示すことから、高血圧モデルマウスを用いて生体内の血圧降下作用を調べました。アスパラプチンAを経口投与したマウスでは、投与1時間後には迅速に血圧低下が見られ、投与2時間後で最大の血圧低下作用が確認されました。さらに、投与3時間後には血圧低下作用は軽減し、投与2日後には元の血圧に戻ることが分かりました。これらの結果は、アスパラプチンAが短時間作用型のACE阻害剤としての効果を持つことを示しています。
強い降圧効果を持つ短時間作用型のACE阻害剤は、急速な降圧が必要となる患者に対して、救急・集中治療領域などで実用化が期待されます。現在、医療現場で使用されているACE阻害剤は、内服で長時間作用型の降圧剤となるため、大動脈解離や大動脈瘤破裂などで緊急に外科手術を必要とする患者には、使用しにくい現状があります。アスパラプチン Aは、ヒトにおいて降圧効果と分解作用を併せ持つ可能性があることから、将来的に医療現場で使用可能な降圧剤の重要な候補となる可能性があります。
今後の期待
代謝物の解析を効率化するコンピュータを用いた解析には、標準化された手法が求められます。本手法により、安定同位体標識の代謝物と非標識の代謝物を同時に解析して、構造推定や生合成経路を解析することが可能となりました。
本手法を、既存の類似性解析に組み込むことで、未知代謝物の構造解析の精度が大きく高まることが期待できます。類似性を用いたネットワーク解析に、既知の代謝物、その代謝物が示す生物活性、代謝物の起源などの情報を組み込み、可視化することで、類縁体や活性物質の探索、何も情報がない未知代謝物の発見を簡便化できるものと期待できます。
また、本手法を用いたアスパラプチンBおよびCの発見により、アルギニン以外のアミノ酸とアスパラガス酸が結合したアスパラプチン類の存在が示されました。未発見のアスパラプチン類の中には、より強いACE阻害活性を示すものがあるかもしれません。今後、より高感度の最先端質量分析装置と本研究で開発した解析手法により、その一部または全てが発見される可能性があります。
本研究は、国際連合が2016年に発効した17項目の「持続可能な開発目標(SDGs)[9]」のうち、「3. すべての人に健康と福祉を」に貢献するものと考えます。
補足説明
1.メタボロミクス、メタボローム
メタボローム解析ともいう。メタボロームは細胞内で合成された低分子代謝産物の総体を指す。メタボローム解析とは、このメタボロームを網羅的に測定・解析すること。
2.13C
安定同位体の一種。原子番号(陽子数)が同じで、質量数(陽子と中性子の数の和)が異なる原子を互いに同位体という。そのうち、安定に存在するものを安定同位体といい、放射線と呼ばれる粒子やエネルギーを放出して他の原子に変わる同位体を放射性同位体という。安定同位体の13C、15N、18O、34Sといった原子核は、天然存在比が低いものの安全な同位体核であるため、これらを含んだ化合物を生物に取り込ませることができる。
3.MS/MSスペクトル
質量分析装置内でイオンを壊し(フラグメント化)、その生成イオン群(プロダクトイオン)を測定することをMS/MS分析といい、得られるスペクトルをMS/MSスペクトルという。MS/MSスペクトルの情報から、化合物構造の同定・推定が可能である。
4.カルス
培地上などで培養されている分化していない状態の植物細胞の塊のこと。
5.液体クロマトグラフィー-タンデム質量分析(LC-MS/MS)
液体クロマトグラフィーにより分離された化合物を質量分析装置でイオン化し、定性および定量を行う分析手法のこと。
6.ニコチアナミン
天然の植物の代謝物の一つ。
7.アンジオテンシン転換酵素(ACE)
血圧や細胞外容量の調節に関わるホルモン系であるレニンーアンジオテンシン系におけるアンジオテンシンⅠからアンジオテンシンⅡへの反応を触媒する酵素。
8.多変量解析手法、S-プロット
メタボローム解析で用いられる判別分析の一つ。二つのサンプルグループを最大限分離する判別モデルを作成する解析法。
9.持続可能な開発目標(SDGs)
2015年9月の国連サミットで採択された「持続可能な開発のための2030アジェンダ」にて記載された2016年から2030年までの国際目標。持続可能な世界を実現するための17のゴール、169のターゲットから構成され、発展途上国のみならず、先進国自身が取り組むユニバーサル(普遍的)なものであり、日本としても積極的に取り組んでいる(外務省ホームページから一部改変して転載)。
共同研究グループ
理化学研究所環境資源科学研究センター
統合メタボロミクス研究グループ
研究員(研究当時) 中林 亮(なかばやし りょう)
(現 客員研究員)
テクニカルスタッフⅠ 西澤 具子(にしざわ ともこ)
グループディレクター 斉藤 和季(さいとう かずき)
メタボローム情報研究チーム
テクニカルスタッフⅠ 山田 豊(やまだ ゆたか)
質量分析・顕微鏡解析ユニット
専門技術員 森 哲哉(もり てつや)
岩手医科大学 薬学部
助教 浅野 孝(あさの たかし)
虎の門病院 集中治療科・循環器センター内科
医師 桑原 政成(くわばら まさなり)
原論文情報
Ryo Nakabayashi*, Yutaka Yamada, Tomoko Nishizawa, Tetsuya Mori, Takashi Asano, Masanari Kuwabara, and Kazuki Saito, “Tandem Mass Spectrum Similarity-Based Network Analysis Using 13C-Labeled and Non-labeled Metabolome Data to Identify the Biosynthetic Pathway of the Blood Pressure-Lowering Asparagus Metabolite Asparaptine A”, Journal of Agricultural and Food Chemistry, 10.1021/acs.jafc.1c01183*, 責任著者
発表者
理化学研究所
環境資源科学研究センター 統合メタボロミクス研究グループ
研究員(研究当時) 中林 亮(なかばやし りょう)
(現 客員研究員)
グループディレクター 斉藤 和季(さいとう かずき)
報道担当
理化学研究所 広報室 報道担当