2021-10-01 京都大学 iPS細胞研究所
ポイント
- 近接する細胞同士が、それぞれの分化段階や細胞形質を同調させている現象(細胞形質同調)を新たに発見し、それが細胞外小胞1)によって担われていることを解明しました。
- 細胞形質同調にはmiR-132というマイクロRNA2)が関わっていることを見出し、miR-132を含んだ人工のナノ粒子を作製してマウスの胚に添加したところ、心筋細胞への分化が促進されることを確認しました。
- 本研究の成果は再生医療に向けた基礎研究に新たな知見をもたらします。
1. 要旨
からだを形作る細胞は、胚の発生過程で細胞の運命付けに従ってさまざまな細胞へと分化することにより生み出されます。このとき、細胞は周囲の細胞たちと同調しながら目的の細胞へと分化し、正常な組織や臓器を形成していくと考えられますが、この同調のしくみは解明されていませんでした。
皆川朋皓特定研究員(CiRA増殖分化機構研究部門)と山下潤教授(CiRA同部門)らの研究グループは、マウスのES細胞3)を用いた研究により、細胞外小胞を介した細胞間コミュニケーションによって、近接する細胞同士が、それぞれの分化段階や形質を同期・同調させていることを初めて突き止め、この現象を「細胞形質同調(Phenotypic Synchrony of Cells: PSyC)」と名付けました。
さらに、細胞形質同調には細胞外小胞内に含まれるmiR-132というマイクロRNAが関わっていることを見出し、miR-132を含んだ人工のナノ粒子を作製してマウスの胚に添加したところ、心筋細胞への分化が促進されることを確認しました。細胞形質同調は発生や生体恒常性に広く関わっていると考えられるため、今回の知見は今後の再生医療に向けた基礎研究に影響を与えることが期待できます。
この研究成果は2021年 9月 17日に米国科学誌「Journal of Extracellular Vesicles」でオンライン公開されました。
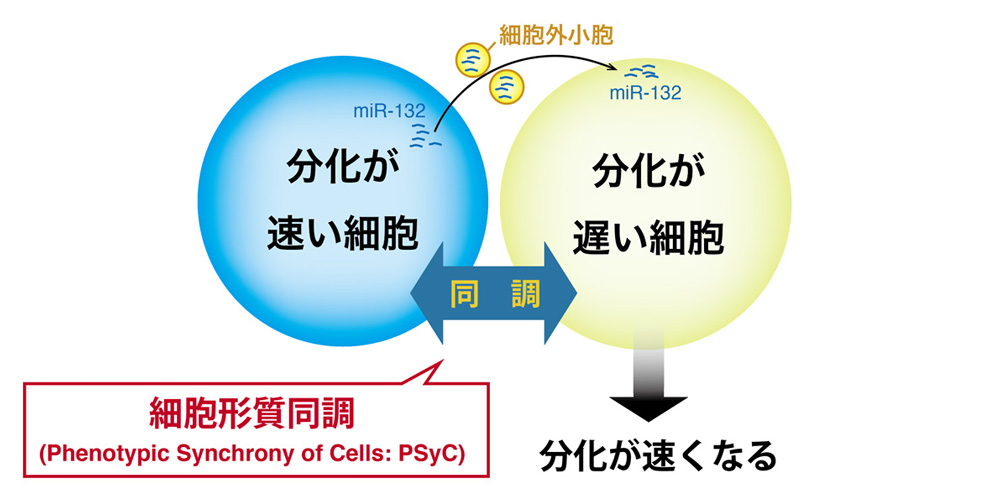
論文概要図
2. 研究の背景
胚の発生は細胞同士の分化が極めて高度に調整されて起こる現象です。各々の細胞の分化がどのように調整されているか突き止めるため、これまで多くの研究が行われてきました。それら研究の多くは細胞のシグナル伝達経路や遺伝子発現などを調べるものでしたが、細胞同士が協調しながら分化していく現象のしくみは解明されていませんでした。
研究グループはこれまで、分化の速度が異なったマウスES細胞の作製技術を開発しており、分化の遅いES細胞と速いES細胞を同時に共培養させることができます。本研究では、分化の速度が異なるES細胞を共培養し、細胞同士の分化の同調とそのしくみを調べました。
3. 研究結果
1) 近接するES細胞同士の分化の同調を確認
これまでのマウスのES細胞を使った研究の中で、ドキシサイクリン4)を操作することにより恒常的に活性化されるプロテインキナーゼA(PKA) 5)を発現するマウスES細胞(PKA-ESC)を作製し、細胞内のPKAの活性化を薬剤により制御可能なES細胞分化システムを開発してきました。PKA-ESCは、ドキシサイクリンをなくすと、活性型PKAを発現し中胚葉6)への分化が速くなります。逆に、PKA-ESCにドキシサイクリンを働かせると、活性型PKAの発現は起こらず、通常の速度で分化が起こります。
本研究では、ドキシサイクリンをなくすとPKAの活性化により分化が速くなるES細胞(PKA-ESC)と、活性型PKAを有しておらずドキシサイクリンの有無によって分化速度が変わらない細胞(対照:分化の遅いES細胞)を共培養し、同時に中胚葉へと分化誘導させました。
ドキシサイクリンをなくし、PKA-ESCの分化を速くしたところ、ドキシサイクリンの影響を受けない分化が遅いES細胞の分化も速まり、分化が速いES細胞と同程度まで分化が進む現象が観察できました(図1)。このことは、分化の速度が違うES細胞の間で分化の同調現象が起こっていることを意味します。この現象を「細胞形質同調(Phenotypic Synchrony of Cells: PSyC)」と名付けました。
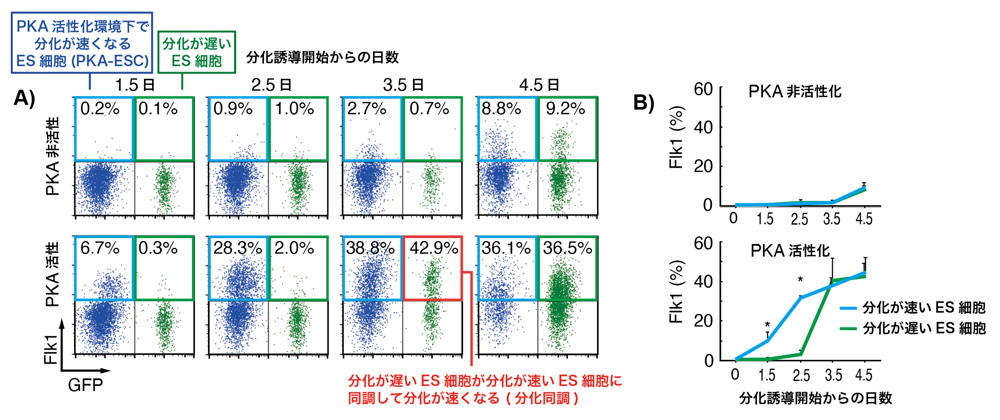
図1:共培養した分化速度の違うマウスのES細胞による細胞形質同調の確認
(A)フローサイトメトリー解析7) による分化速度の違うES細胞の中胚葉マーカー遺伝子Flk1と緑蛍光タンパク質GFPの発現分布図。Flk1は中胚葉に分化した細胞の数を反映し、GFPは対照(分化の遅い細胞;緑)でのみ発現する。PKA-ESC(青)はGFPを発現しない。
(B)(A)におけるFlk1の割合を示したグラフ。PKA活性化環境下において、分化誘導開始から2.5〜3.5日の間に分化が遅いES細胞のFlk1の割合が急上昇する。
2) 細胞形質同調のしくみの解明
次に、この細胞形質同調のしくみを解明するため、どのように細胞間でコミュニケーションが行われているかを調べました。細胞間コミュニケーションの重要な媒介の一つとして細胞外小胞が考えられますが、細胞外小胞を放出するには、nSMase2という酵素が関わっていることが分かっています。
そこで、nSMase2阻害剤を共培養分化誘導時に添加すると、分化の遅いES細胞の分化促進現象が阻害され、細胞形質同調が行われていないことが分かりました。さらに、PKA-ESCから分泌された細胞外小胞を単離し、分化の遅いES細胞に添加すると、分化の遅いES細胞の中胚葉への分化が速まっていることが確認できました(図2)。以上の結果から、細胞外小胞が細胞形質同調に関わっていると結論付けられます。
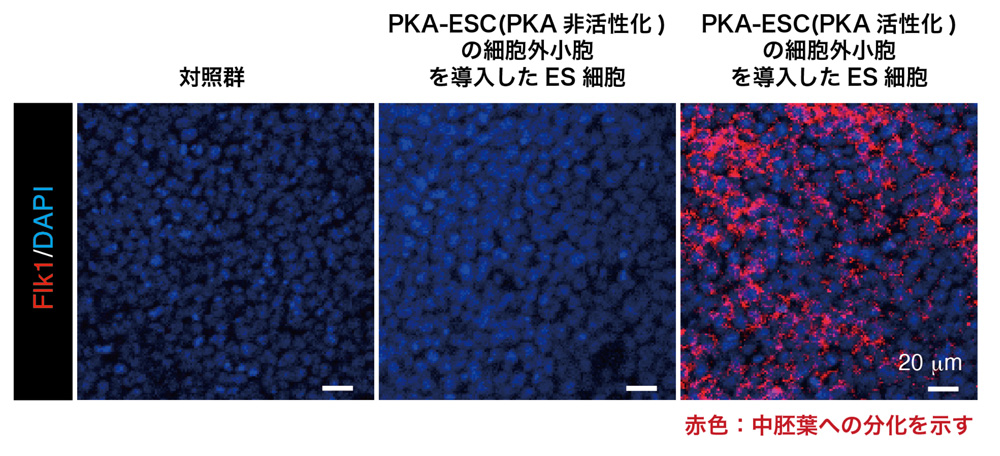
図2:中胚葉のマーカー(Flk1)に免疫染色したES細胞の画像
PKA活性化環境下におけるPKA-ESCの細胞外小胞を添加したES細胞のみ、中胚葉への分化を示す赤色が示された。
さらに、細胞外小胞の中のどのような物質が細胞形質同調に寄与したか同定するため、PKA-ESCから分泌された細胞外小胞をmiRNA-seq解析8)したところ、miR-132というマイクロRNAが候補の一つとなりました。そこで、ゲノム編集技術9)によってmiR-132を取り除いたPKA-ESCを作製し、その細胞から分泌される細胞外小胞を分化の遅いES細胞に添加しましたが、分化が速まる現象は起きませんでした。以上より、細胞外小胞の中のmiR-132が細胞形質同調に寄与する主な物質だと考えられます。
また、miR-132を受け取った細胞の中でどのような反応が起こっているかを調べると、miR-132による複数の遺伝子の制御を介して、結局は分化の速度に関わるPKA活性につながっていることが分かりました。これらをまとめると、細胞形質同調のメカニズムは図3のように説明できます。
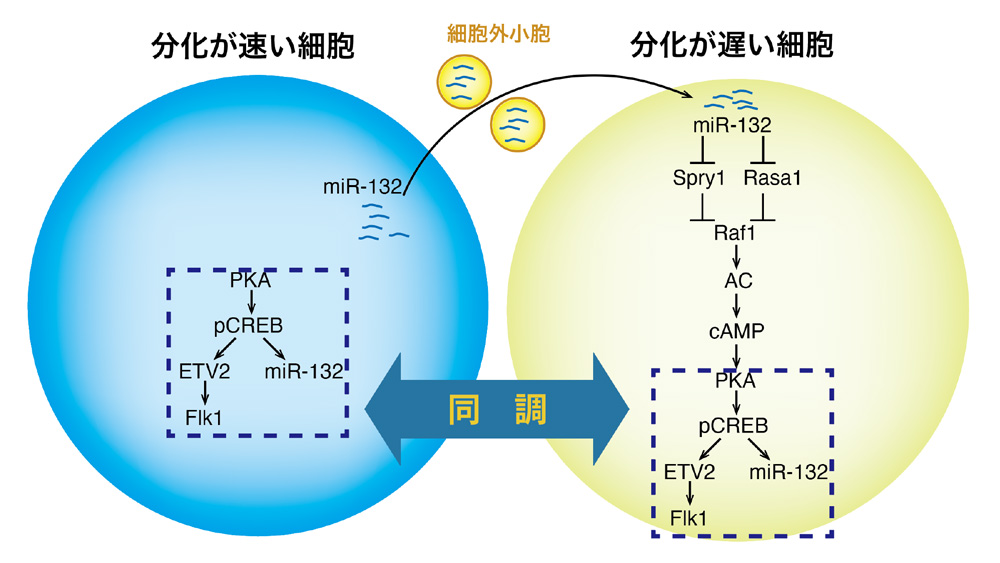
図3:細胞形質同調のメカニズム
3) マウス胚(生体外)による実験
最後に、PKA-ESCから分泌された細胞外小胞およびmiR-132が胚発生にどのような影響を及ぼすかを調べるため、マウス胚を使った実験を行いました。
まず、PKA-ESCから分泌された細胞外小胞を生体外に取り出したマウス胚に添加する実験を行いました。受精後3.5日のマウス胚を取り出し、PKA-ESC(PKA活性化)から分泌された細胞外小胞と培養すると、通常の培養ではほとんど認められない心筋細胞への分化が促進され、培養後8日〜10日において拍動を開始していることが確認できました (図4)。
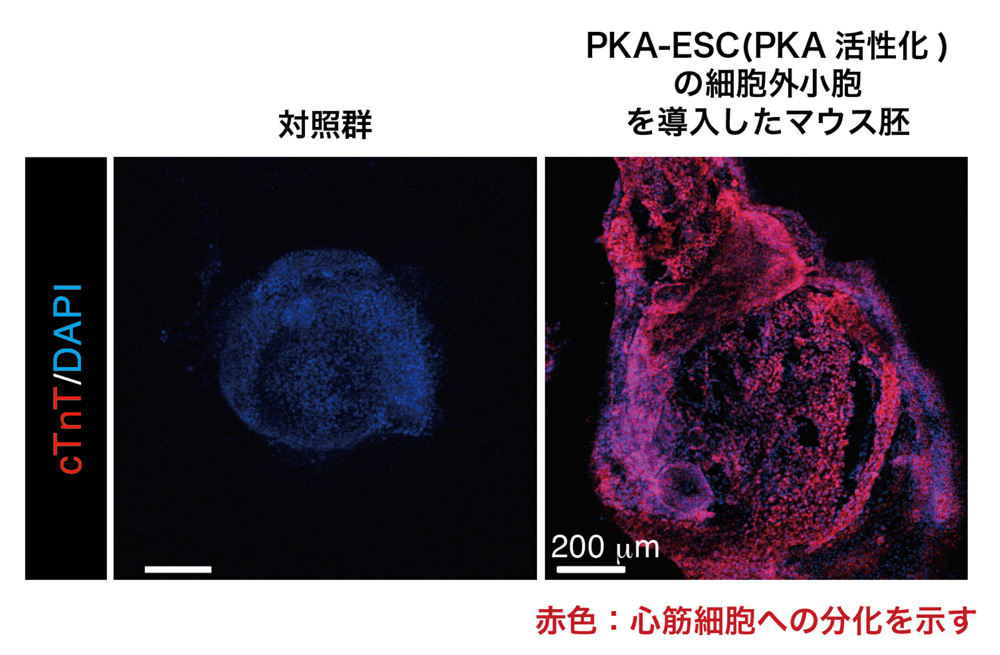
図4:心筋細胞のマーカー(cTnT)に免疫染色したマウス胚の画像(細胞外小胞による実験)
PKA活性環境下におけるPKA-ESCの細胞外小胞を導入したマウス胚では、心筋細胞への分化を示す赤色が示された。PKA-ESCの細胞外小胞はESCに対しては中胚葉への分化誘導したが、マウス胚に対しては中胚葉からさらに分化が進んだ心筋細胞を誘導した。
上記の実験で細胞外小胞が細胞の運命決定に関わっていることが分かりましたが、(2)で同定したmiR-132単体でも同様の結果が得られるか確かめるため、生体で分解する高分子を用いて、miR-132を含んだ人工のナノ粒子を作製し、受精後3.5日のマウス胚に添加しました。すると、PKA-ESC(PKA活性)から分泌された細胞外小胞を添加した場合と同様に、培養後8日〜10日において拍動する心筋細胞が確認できました(図5)。以上より、PKA-ESCから分泌された細胞外小胞およびmiR-132は、中胚葉への分化からさらに心筋細胞への分化にまで影響を及ぼすことが分かり、細胞の運命決定に大きく関わっていると言えます。
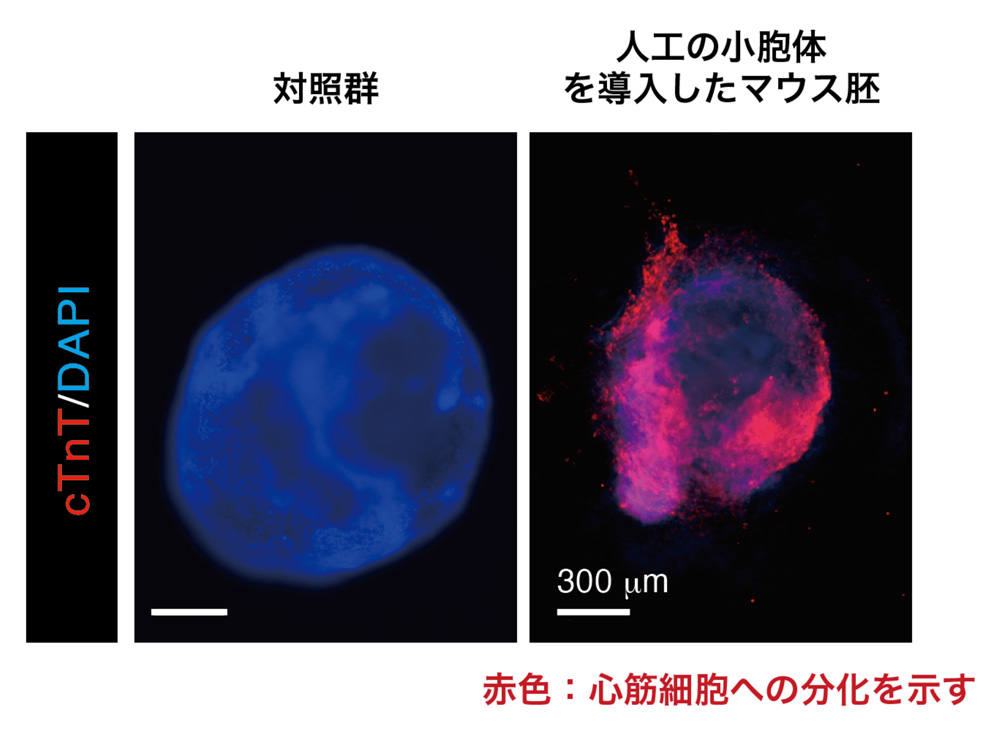
図5:心筋細胞のマーカー(cTnT)に免疫染色したマウス胚の画像(人工の小胞による実験)
miR-132を含んだ人工のナノ粒子を添加したマウス胚において心筋細胞への分化を示す赤色が示された。
4. 本研究の意義と今後の展望
本研究では、これまで謎に包まれていた細胞同士が同調して分化していく現象について、そのしくみを解明し、細胞外小胞を介した細胞コミュニケーション「細胞形質同調(Phenotypic Synchrony of Cells: PSyC)」と名付けました。さらに、今回、細胞形質同調にmiR-132が関わっていることを見出しましたが、細胞外小胞はマイクロRNAやタンパク質を含めた数万以上となる生体物質から成り立っており、miR-132は細胞形質同調に関わる物質の一つに過ぎない可能性があります。また、本研究は中胚葉系列への分化に関する細胞形質同調のみを調べており、細胞の種類や環境の違いによっては細胞形質同調のメカニズムが異なると考えられるため、今後別条件においても調べる必要があります。
細胞形質同調は分化の同調のみならず、発生や組織の恒常性に広く関わっていると考えられます。今回得られた知見は、将来、発生異常やがんなどの疾患の解明や人工的なナノ粒子を用いた再生医療の実現へ貢献されることが期待できます。
5. 論文名と著者
- 論文名
Extracellular vesicles synchronize cellular phenotypes of differentiating cells - ジャーナル名
Journal of Extracellular Vesicles - 著者
Tomohiro Minakawa1,*, Tetsuya Matoba2, Fumiyoshi Ishidate3, Takahiro K. Fujiwara3, Sho Takehana4, Yasuhiko Tabata4, and Jun K. Yamashita1,**
*:筆頭著者 **:責任著者 - 著者の所属機関
- 京都大学 iPS細胞研究所(CiRA)
- 九州大学大学院医学研究院
- 京都大学 アイセムス 物質-細胞統合システム拠点(WPI-iCeMS)
- 京都大学 ウイルス・再生医科学研究所
6. 本研究への支援
本研究は、下記機関より支援を受けて実施されました。
- 国立研究開発法人科学技術振興機構(JST)科研費 CREST
7. 用語説明
注1)細胞外小胞(EV)
細胞が外に放出する小胞の総称。小胞のサイズや形成過程のちがいによって、エクソソーム(Exosome)やマイクロベシクル(microvesicle)と呼ばれる。細胞間のコミュニケーションを媒介する物質と考えられている。
注2)マイクロRNA(miRNA)
20〜30塩基程度の長さの短いノンコーディング(タンパク質をコードしていない)RNA。相補的な配列を持つmRNA(メッセンジャーRNA)と結合して翻訳を抑制したり、mRNAを分解したりすることで、そのmRNAからのタンパク質の合成を抑制する働きをもつと考えられている。
注3)ES細胞
胚性幹細胞(ES細胞:embryonic stem cell)のこと。ES細胞はマウスの場合受精後3、4日目の胚盤胞から細胞を取り出し、それを培養することによって作製される多能性幹細胞の一つで、あらゆる組織の細胞に分化することができる。
注4)ドキシサイクリン(Doxycycline)
抗生物質の一種。遺伝子工学ではこの物質に反応して遺伝子のオンオフを制御する仕組みがよく用いられている。
注5)プロテインキナーゼA(PKA)
タンパク質分子をリン酸化する酵素の一種。この酵素の働きによりリン酸化(リン酸基H2PO4-を付加させる化学反応)されたタンパク質は構造が変わり、活性化したり、情報を伝達することができる。
注6)中胚葉
受精後の胚からできる3つの細胞の塊(内胚葉、中胚葉、外胚葉)の一つ。中胚葉へ分化した細胞はさらに、側板中胚葉、中間中胚葉、沿軸中胚葉などに分かれる。側板中胚葉は、血管、血球、心筋などへ、中間中胚葉は腎臓、生殖腺などを含む泌尿生殖系の器官へ、沿軸中胚葉は椎骨や肋骨、骨格筋、軟骨などの細胞へと分化する。
注7)フローサイトメトリー解析
流動細胞計測法。レーザー光を用いて光散乱や蛍光測定を行うことにより、水流の中を通過する単一細胞の大きさ、DNA量など、細胞の生物学的特徴を解析することができる。
注8)miRNA-seq解析
次世代シーケンサーを用いてRNA のシーケンシング(配列情報の決定)を行い、細胞内、あるいは細胞外小胞中に存在する全miRNAの定量を行う解析。
注9)ゲノム編集技術
人工DNA切断酵素によってゲノムDNAにDNA二本鎖切断を誘導し、その修復過程において、標的遺伝子への欠失や挿入変異を導入(遺伝子ノックアウト)したり、ドナーベクターのゲノム DNA への組み込みを促進することで遺伝子を挿入(遺伝子ノックイン)したりする最先端の遺伝子改変技術。