2021-11-01 東京医科歯科大学,東京大学医科学研究所,日本医療研究開発機構
ポイント
- ヒト表皮幹細胞の運動能力が、幹細胞の自己複製や表皮再生に必須であることを明らかにしました。
- 加齢によって、皮膚再生時の表皮増殖因子(EGF)受容体シグナル活性の低下が起こることを見出しました。
- EGF受容体シグナルは、表皮幹細胞の機能に必須であるXVII型コラーゲン(COL17A1)の安定化に寄与していることを明らかにしました。
- COL17A1は細胞骨格を介してヒト表皮幹細胞の運動性を制御していることを見出しました。
- 糖尿病性潰瘍や褥瘡(床ずれ)などの難治性皮膚潰瘍の病態解明と新規治療法開発への応用が期待できます。
概要
東京医科歯科大学・難治疾患研究所・幹細胞医学分野の難波大輔准教授と西村栄美教授(東京大学医科学研究所・老化再生生物学分野教授兼任)の研究グループは、大阪大学の土岐博特任教授、国際医療福祉大学の松崎恭一主任教授、愛媛大学の佐山浩二教授および白石研講師との共同研究で、加齢による皮膚再生能力低下の原因が、XVII型コラーゲンの分解による表皮幹細胞の運動能低下であることをつきとめました。この研究は文部科学省科学研究費補助金、新学術領域研究「数理解析に基づく生体シグナル伝達システムの統合的理解」、武田科学振興財団、ならびに日本医療研究開発機構(AMED)『老化メカニズムの解明・制御プロジェクト』の支援のもとでおこなわれたもので、その研究成果は、米国科学誌Journal of Cell Biologyに、2021年9月22日午前10時(米国東部時間)にオンライン版で発表されました。
研究の背景
高齢者に多い皮膚潰瘍や床ずれは、生活の質(QOL)ならびに寿命に大きく関わることから、超高齢化社会においてその対策が喫緊の課題となっています。加齢そのものによる皮膚の再生能力の低下に加え、糖尿病など加齢に関連する基礎疾患が、糖尿病性足潰瘍や静脈性下肢潰瘍、褥瘡(床ずれ)に大きく関与しています。これらの難治性皮膚潰瘍※1では、老化や基礎疾患による創傷治癒の遅延に細菌感染を伴うことが多く、細菌叢バイオフィルムが形成されてさらに難治性となり、重症例では下肢切断が必要となります。したがって、難治性皮膚潰瘍の重症化を防ぐため、早期段階からの治療が必要ですが、効果的な治療法は未だに開発されていません。皮膚の再生では、周囲の表皮が欠損部分に移動し、その部分を覆う上皮化というプロセスが必須となります。常に細胞が入れ替わる組織である表皮の恒常性は表皮幹細胞※2が担っており、皮膚再生時の上皮化にも、この表皮幹細胞が関与していることが知られています。老化や基礎疾患などによって難治性皮膚潰瘍が誘発される環境では、この表皮幹細胞の機能が障害されている可能性が示唆されていましたが、その仕組みについては解明されていませんでした。
研究成果の概要
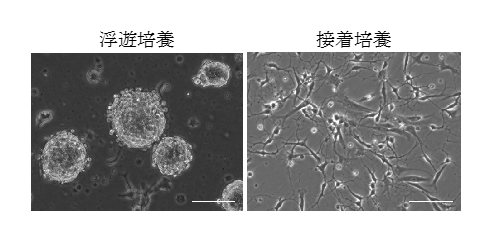
本グループは、まず採取されたヒト皮膚から表皮細胞が集団で移動する様子を、培養系で観察することに成功しました。この表皮細胞の集団移動は、皮膚の傷が治る際の上皮化と同じ細胞の運動形態であり(図1A上段)、同様の表皮細胞の集団運動は、ヒト表皮幹細胞が培養系でコロニーとして成長する際にも観察されました(図1A下段)。このことは、ヒト表皮幹細胞のコロニー形成が、上皮化研究の優れたモデルであり、培養系でのヒト表皮幹細胞の運動様式の解明が上皮化の仕組みの解明につながることを示しています。そこで、ヒト表皮幹細胞コロニーと幹細胞ではない表皮細胞が作るコロニー内での細胞の速度を調べたところ、幹細胞コロニー内の細胞の方が、素早く移動していることがわかりました(図1B)。さらに本グループは、ヒト表皮幹細胞の増殖や運動パターンを解析し、それらをモデル化することで、コンピューター内で表皮幹細胞の増殖を再現することに成功しました。そのシミュレーションから、表皮幹細胞が自己複製し、コロニーが成長するには、表皮幹細胞の運動能力が必須であることが分りました(図1C)。
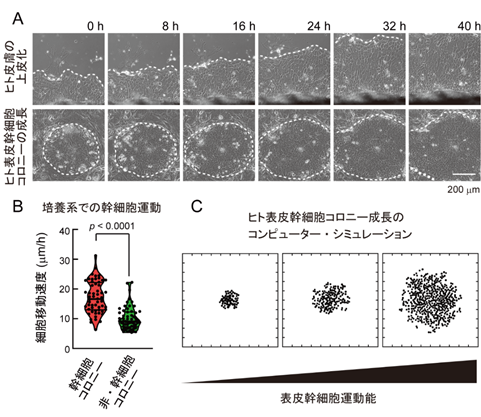
(図1)ヒト表皮幹細胞の運動能と自己複製能の相関
加齢による皮膚再生能力の低下には、上皮化の速度低下が関与していることが報告されています。そこで、本グループは、若齢マウスと老齢マウスに傷を作製し、傷が治る過程での様々な因子の活性状態を調べたところ、表皮増殖因子(Epidermal Growth Factor:EGF)受容体※3の活性化が、加齢に伴って減少することを発見しました(図2A)。そこで、培養系にEGFを添加し、ヒト表皮幹細胞のEGF受容体を活性化したところ、実際に表皮幹細胞の運動能力(図2B)だけでなく、増殖能力(図2C)も増加することを確認しました。この結果は、コンピューターシミュレーションで示されたヒト表皮幹細胞の運動能と自己複製能の相関を、培養系で実証するものです。続いて、EGF受容体の活性化が、表皮幹細胞の維持に必須であるXVII型コラーゲン(COL17A1)※4の量を増加させることを見出しました(図2D)。詳細な生化学的な解析から、ヒト表皮幹細胞では、EGF受容体が活性化すると、TIMP1※5と呼ばれるタンパク質分解酵素の活性を阻害するタンパク質の発現が誘導され(図2E)、このTIMP1によって、細胞膜にあるCOL17A1が分解されずに安定化することが明らかとなりました(図2F)。以上の結果は、これまで知られていなかったEGF受容体シグナルによるCOL17A1の安定化という、全く新しいCOL17A1の制御機構の存在を示しています。
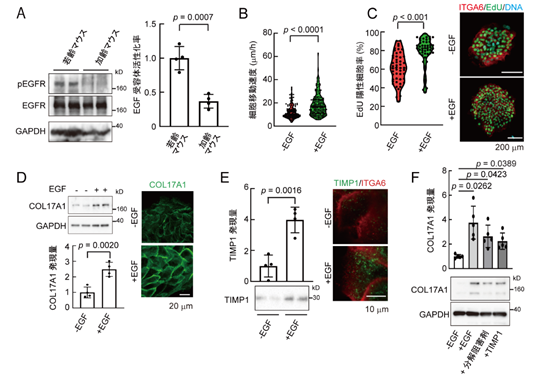
(図2)加齢によるEGF受容体シグナルの低下及びEGF受容体シグナルによるCOL17A1の安定化
本グループのこれまでの研究から、COL17A1は表皮幹細胞の機能維持に必須であることは知られていましたが(劉ら、Nature 2019)、細胞レベルでの詳細な仕組みはまだ明らかになっていません。そこで、表皮幹細胞でのCOL17A1の発現量を抑制する実験を行ったところ、表皮幹細胞の運動性が低下し、表皮細胞集団が移動する速度が大きく低下することを見出しました(図3A)。続いて、詳細な観察を行った結果、表皮幹細胞が移動する場合、その先端部分で細胞の運動性に関与する細胞骨格であるアクチン線維とケラチン線維の排他的な分布パターンが観察されますが、COL17A1の発現量を抑制すると、このパターンが変化し、アクチン線維の領域が大きく減少しました(図3B)。
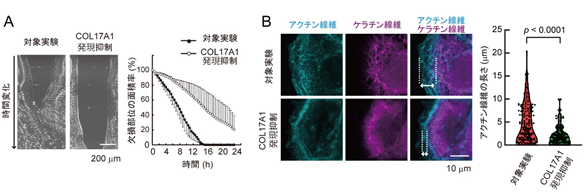
(図3)COL17A1発現抑制による運動能の低下と細胞骨格の変化
以上の結果をまとめますと、通常の表皮幹細胞では、EGF受容体にEGFなどが結合することで、EGF受容体シグナルが活性化し、タンパク質分解を阻害するTIMP1が細胞外に分泌されています。このTIMP1が、COL17A1の分解を防ぎ、COL17A1が細胞膜上で安定に存在することで、アクチン線維とケラチン線維のネットワーク形成により、表皮幹細胞の高い運動能力が維持されます。しかしながら、加齢によってEGFなどが減少し、EGF受容体が不活性化状態になると、TIMP1が継続的に供給されずに細胞膜上のCOL17A1が分解され、最終的に細胞骨格のネットワーク形成の破綻により、表皮幹細胞の運動能力が大きく低下します。このEGF受容体-TIMP1-COL17A1経路の不活性化が、加齢に伴う皮膚再生能力の低下に大きく関与していると考えられます(図4)。
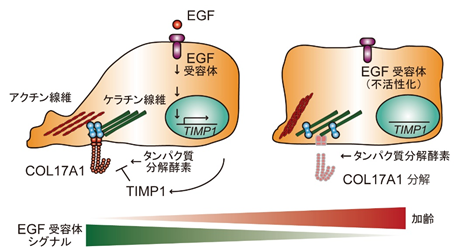
(図4)EGF受容体ーTIMP1ーCOL17A1経路によるヒト表皮幹細胞運動能の制御
研究成果の意義
ヒトにおいては、加齢に伴って皮膚でのCOL17A1の量が減少することが報告されていますが、同様にEGF受容体を活性化するEGFの量も、血液中などで減少することが報告されています。本グループが見出したEGF受容体-TIMP1-COL17A1経路の不活性化が、皮膚再生能力の低下の引き金になると考えられることから、糖尿病性潰瘍や床ずれなどの難治性皮膚潰瘍の発症とも、大きく関連している可能性があり、本研究成果は、これらの病態の発症機構の解明を大きく前進させます。また、この経路を活性化することで、加齢によって低下した皮膚再生能力の改善や、難治性皮膚潰瘍に対する新しい治療法の開発が期待されます。
用語解説
- ※1難治性皮膚潰瘍
- 通常ならば治るはずの皮膚にできた傷が、何らかの阻害要因によって、通常の治療では治らない傷(皮膚潰瘍)になったもの。
- ※2表皮幹細胞
- 表皮に存在する組織特異的幹細胞。培養系においても表皮組織を形成する能力を保持しており、培養表皮シートとして重度熱傷などの治療に用いられている。
- ※3表皮増殖因子受容体(EGF受容体)
- 細胞増殖因子の一つである表皮増殖因子(EGF)の受容体。EGFが結合することで活性化され、細胞内へ増殖シグナルなどを伝える。EGFだけでなく、TGFαやHB-EGFなど他のEGFファミリー分子もEGF受容体に結合し活性化する。
- ※4XVII型コラーゲン(COL17A1)
- 細胞と細胞外基質である基底膜をつなぐヘミデスモソームを構成する分子の一つ。細胞膜に存在し、細胞外領域はタンパク質分解酵素によって切断を受けることが知られている。
- ※5TIMP1(Tissue inhibitor of metalloproteinase 1)
- タンパク質分解酵素の一種であるメタロプロテアーゼの活性を阻害するタンパク質。細胞外に放出され、多くの種類のメタロプロテアーゼの活性を組織中にて阻害する。
論文情報
- 掲載誌
- Journal of Cell Biology
- 論文タイトル
- EGFR-mediated epidermal stem cell motility drives skin regeneration through COL17A1 proteolysis
- DOI
- 10.1083/jcb.202012073
研究者プロフィール
難波大輔(ナンバ ダイスケ)Daisuke Nanba
東京医科歯科大学 難治疾患研究所 幹細胞医学分野 准教授
研究領域
幹細胞生物学、皮膚科学など
西村栄美(ニシムラ エミ)Emi K. Nishimura
東京医科歯科大学 難治疾患研究所 幹細胞医学分野 教授
東京大学医科学研究所 老化再生生物学分野 教授
研究領域
幹細胞生物学、老化・再生生物学、皮膚科学、実験病理学など
お問い合わせ先
研究に関すること
国立大学法人東京医科歯科大学 難治疾患研究所
幹細胞医学分野 難波大輔(ナンバ ダイスケ)
報道に関すること
国立大学法人東京医科歯科大学 総務部総務秘書課広報係
国立大学法人東京大学医科学研究所 国際学術連携室(広報)
AMED事業に関するお問い合わせ
国立研究開発法人日本医療研究開発機構(AMED)
疾患基礎研究事業部 疾患基礎研究課
老化メカニズムの解明・制御プロジェクト