2026-05-01 京都大学 iPS細胞研究所
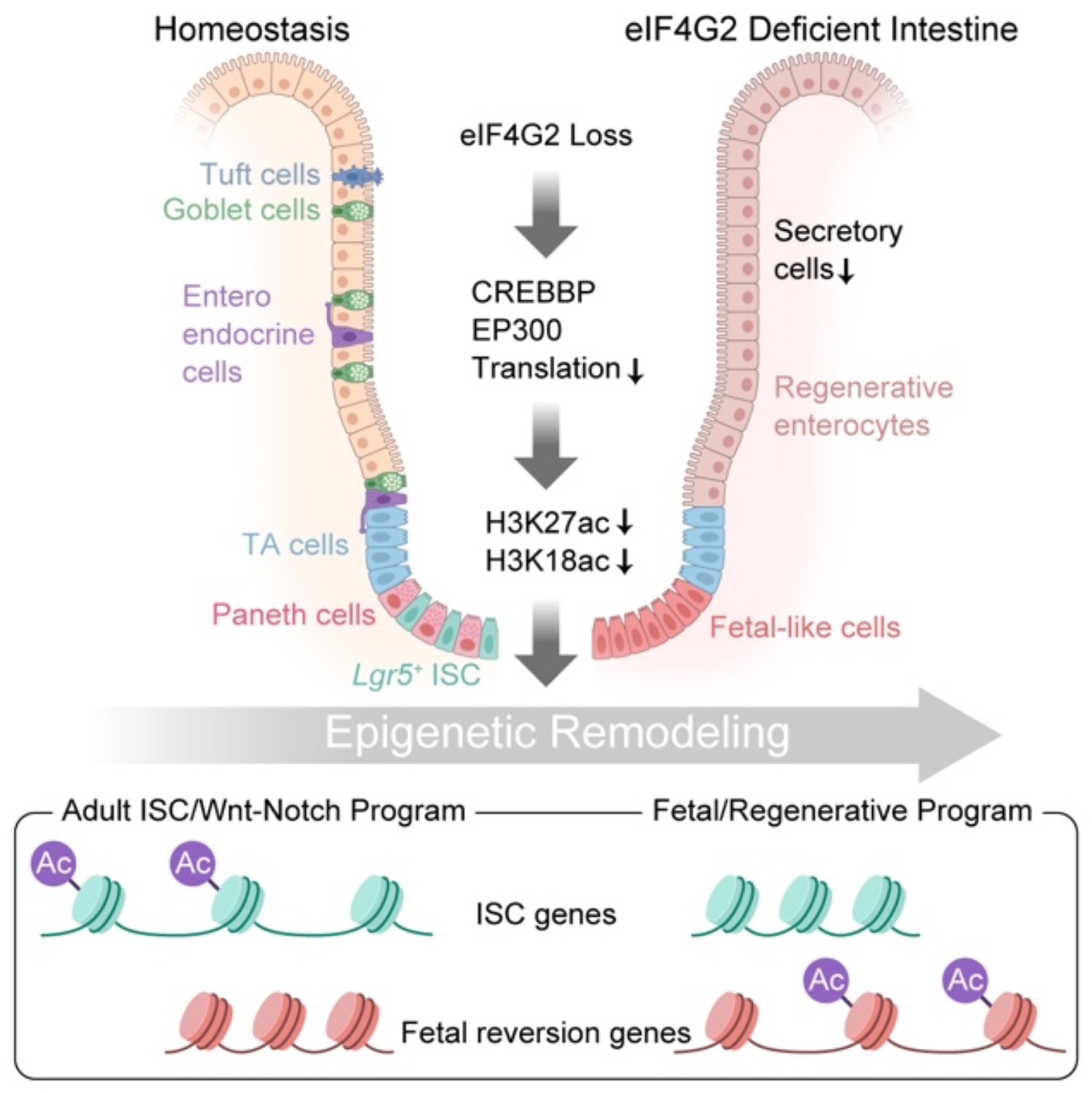
図1. 本研究の概要
<関連情報>
- https://www.cira.kyoto-u.ac.jp/j/pressrelease/news/260501-100000.html
- https://www.cell.com/cell-stem-cell/fulltext/S1934-5909(26)00146-3
eIF4G2を介したクロマチン調節因子の選択的翻訳は、成体腸幹細胞の同一性と分化を保護する eIF4G2-mediated selective translation of chromatin regulators safeguards adult intestinal stem cell identity and differentiation
Haruko Kunitomi ∙ Aye Myat Khaine ∙ Radia Jamee ∙ … ∙ Yuichi Shichino ∙ Shintaro Iwasaki ∙ Shinya Yamanaka
Cell Stem Cell Published:April 30, 2026
DOI:https://doi.org/10.1016/j.stem.2026.04.006
Highlights
- eIF4G2 stabilizes adult intestinal epithelial identity
- Eif4g2 loss triggers durable fetal-like and YAP-associated reprogramming
- Ribosome profiling links eIF4G2 to selective translation of chromatin regulators
- Translational buffering helps preserve adult enhancer and lineage programs
Summary
eIF4G2 (DAP5/NAT1) is a non-canonical translation initiation factor, but its role in homeostasis is unclear. Using inducible Eif4g2 knockout mice and intestinal organoids, we show that eIF4G2 loss collapses Lgr5+ intestinal stem cell (ISC) and secretory maturation programs while preserving villus architecture. Transcriptomic and single-nucleus multiome analyses reveal a durable fetal-like/regenerative state with YAP-TEAD activation and regenerative absorptive cells. Ribosome profiling identifies selective translation-efficiency loss among chromatin regulators, especially the KAT3 coactivators CREBBP and EP300, resulting in reduced KAT3 abundance and global histone acetylation; chemical KAT3 inhibition phenocopies this state. CUT&Tag and assay for transposase-accessible chromatin sequencing (ATAC-seq) demonstrate that reduced eIF4G2-KAT3 output drives locus-selective enhancer remodeling, with loss of adult ISC/Wnt-Notch elements and activation of TEAD-enriched fetal loci, without inflammatory or integrated stress response programs driving the transition. Fetal intestinal spheroids remain viable despite similar biochemical defects, highlighting a stage-specific requirement for translational buffering in maintaining adult identity.