神経筋接合部を標的とした病態解明と治療法開発に期待
2020-02-19 愛知医科大学,慶應義塾大学,名古屋大学,日本医療研究開発機構
愛知医科大学医学部内科学講座(神経内科)の岡田洋平准教授、小野寺一成研究員(名古屋大学大学院医学系研究科神経内科学客員研究者)らの研究グループは、慶應義塾大学医学部、名古屋大学大学院医学系研究科、新潟大学大学院医歯学総合研究科、東京医科歯科大学及び東京大学との共同研究により、難治性神経変性疾患である球脊髄性筋萎縮症(SBMA)※1の患者さんからiPS細胞を作成し、運動神経へと分化誘導させることでSBMAの新たな疾患モデルを作成しました。また、網羅的トランスクリプトーム解析※2を行い、SBMAの神経変性にシナプス※3の病態が深く関与することを見出しました。本研究により、病態のより深い理解、シナプスを標的とした今後の治療開発につながることが期待されます。本研究成果は、2020年2月19日に英国科学誌 『Molecular Brain』でオンライン公開されました。
本研究成果のポイント
- SBMAの患者さんから疾患特異的iPS細胞を樹立し、運動神経へ分化誘導させた後、フローサイトメトリー※4で運動神経を純化しました。
- 網羅的トランスクリプトーム解析を行ったところ、SBMA運動神経は、シナプス、神経伝達物質、エキソサイトーシス※5、エピジェネティクス※6関連の遺伝子群の発現上昇を示しました。
- 特にシナプス形成に重要なRSPO2、WNTリガンドの発現上昇を示しました。
- これらの結果から、SBMAの病態解明や新しい治療開発につながることが期待されます。
研究の背景
球脊髄性筋萎縮症(Spinal bulbar muscular atrophy:SBMA)は、成人で発症し、緩やかな進行を示す運動神経変性疾患で、根治療法がないとされる難病です。アンドロゲン受容体(AR)遺伝子のCAG反復配列の伸長(変異AR)※7が原因で発症することが明らかにされており、これまでのモデルマウスや細胞モデルを用いた研究により、ARのリガンドであるテストステロンに依存して変異ARが凝集体を形成し、運動神経を変性させることが示されてきました。しかし、モデルマウスと実際の患者さんの病態には相違があり、根本的な病態メカニズムは未だ解明されていません。正確な病態の解析・治療法の開発のためには、より正確にSBMA患者さんの病態を反映する疾患モデルが必要とされてきました。
通常、ヒト由来の運動神経を採取することは困難とされています。そこで、本研究グループでは、SBMA患者さんからiPS細胞を樹立し、運動神経へと分化誘導することでSBMAの新たな疾患モデルを作成するとともに、患者さん由来の運動神経を用いて病態解析を行いました。
研究内容
本研究グループは、まずSBMAの患者さんの皮膚線維芽細胞からiPS細胞を作成しました。原因となるARのCAG反復配列数はiPS細胞の樹立(リプログラミング)の過程で変化がありませんでした。次いで、iPS細胞を運動神経へ分化誘導し、4週間の成熟培養を行いました。解析する運動神経の純度を上げるために、運動神経を蛍光タンパクにより特異的に標識し(HB9e438::Venus)、フローサイトメトリーにより分取したところ、高純度の運動神経を得ることに成功しました。このように濃縮された運動神経では、iPS細胞株間の誘導効率の不均一さが改善していました。また、分取した運動神経からRNAを抽出して、RNAシークエンス解析※8を行い、健常者と比較してSBMAで変化している遺伝子群を探索しました(図1)。
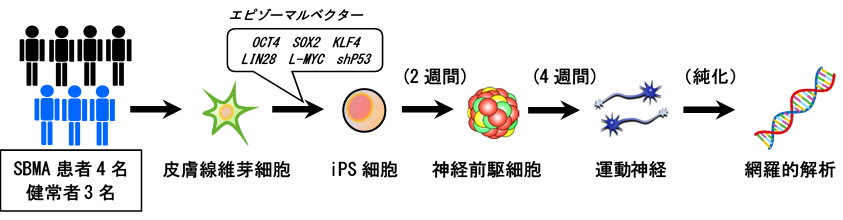 図1:iPS細胞を利用したSBMAの病態解析
図1:iPS細胞を利用したSBMAの病態解析
遺伝子オントロジー解析、パスウェイ解析※9では、SBMAの運動神経でシナプス、神経伝達物質、エキソサイトーシス、エピジェネティクス関連カテゴリーの遺伝子群が高発現していました。また、小胞体※10カテゴリーの遺伝子群の発現低下を認めました(図2)。
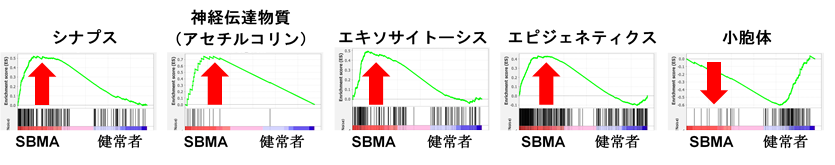 図2:SBMAで変化している遺伝子カテゴリー(エンリッチメント解析※11)
図2:SBMAで変化している遺伝子カテゴリー(エンリッチメント解析※11)
特にシナプス関連遺伝子群の中には、神経筋接合部(Neuromuscular junction:NMJ)※12の形成に必要不可欠なアセチルコリン受容体のクラスタリングを促すRSPO2遺伝子やWNTリガンド遺伝子の発現上昇(図3)、またNMJの形成を抑制的に制御するWNT3A遺伝子の発現上昇がみられ、NMJ形成異常の原因となっている可能性が示唆されました。
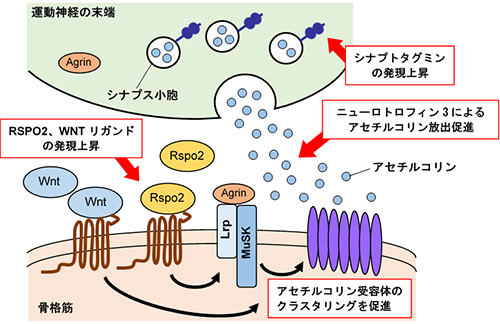
図3:神経筋接合部の形成に関わる遺伝子発現の変化
今後の展開
今回の研究成果から、SBMAの運動神経変性にシナプスの病態が深く関わることが明らかになりました。モデルマウスではNMJの変性が示されていますが、今回初めてSBMA患者iPS細胞由来運動神経におけるシナプス関連遺伝子の発現異常が示されました。こういった遺伝子の変動がSBMAの病態を理解する手がかりとなり、NMJを標的とした病気の進行を抑制する治療開発が期待されます。
用語説明
- ※1 球脊髄性筋萎縮症(Spinal bulbar muscular atrophy:SBMA):
- 成人男性に発症し、嚥下障害や四肢の筋力低下・筋萎縮が緩徐に進行する遺伝性神経変性疾患。
- ※2 トランスクリプトーム解析:
- 細胞のすべての転写産物(mRNA)を用いた遺伝子発現変動解析。
- ※3 シナプス:
- 神経細胞と神経細胞の間で神経情報を伝達する接触構造。
- ※4 フローサイトメトリー:
- レーザー光を用いて個々の細胞を光学的に分析する手法。標識した細胞のみを分取することができる。
- ※5 エキソサイトーシス:
- 分泌小胞の内容物(神経伝達物質など)を細胞外に開口放出する現象。
- ※6 エピジェネティクス:
- ヒストンのアセチル化/メチル化やDNAのメチル化等の状態により、DNAの配列変化によらない遺伝子発現を制御・伝達するシステム。
- ※7 変異アンドロゲン受容体(AR):
- AR遺伝子には、グルタミンをコードする3塩基(CAG)の反復配列が含まれている。健常者では、この反復配列は36回以下とされているが、SBMA患者さんでは38回から62回へと伸長しており、この変異ARが原因で発症するといわれている。
- ※8 RNAシークエンス:
- 次世代シークエンサーを用いたトランスクリプトーム解析で、低発現・高発現のmRNAの定量だけでなく、新規転写産物やスプライシングバリアントの解析も可能である。
- ※9 遺伝子オントロジー、パスウェイ解析:
- 発現変動のある遺伝子群を、生物学的概念で分類したカテゴリー(オントロジー)や、遺伝子間の相互作用や機能的なシグナル経路(パスウェイ)を用いて意義付けする解析。
- ※10 小胞体:
- 細胞内にある器官で、たんぱく質の合成・折りたたみや糖鎖付加などのプロセシングを行う。
- ※11 エンリッチメント解析:
- 2群間(今回はSBMAと健常者間)で、各カテゴリーに関連付けられた遺伝子の発現の差異の偏りをみる解析方法。
- ※12 神経筋接合部(Neuromuscular junction:NMJ):
- 運動神経終末と骨格筋間のシナプス。神経終末からシナプス間隙にアセチルコリン(神経伝達物質の1つ)が放出され、骨格筋のアセチルコリン受容体に結合して神経信号が伝達される。
研究成果の公表
本研究成果は、令和2年2月19日(日本時間の午前10時),Molecular Brain誌オンライン版として掲載されます。
- 論文タイトル:
- Unveiling synapse pathology in spinal bulbar muscular atrophy by genome-wide transcriptome analysis of purified motor neurons derived from disease specific iPSCs
(疾患特異的iPS 細胞から誘導した純化した運動神経におけるゲノムワイドなトランスクリプトーム解析による球脊髄性筋萎縮症のシナプス病態の解明) - 著者:
- 小野寺一成1,2、下門大祐1,3、石原康晴3、矢野真人4、宮冬樹5,6,7、坂野晴彦2、葛巻直子3,8、伊藤卓治1、岡田梨奈1、Bruno de Araujo Herculano1、大山学9、吉田真理10、角田達彦5,6,7、勝野雅央2、道勇学1、祖父江元11、岡野栄之3、岡田洋平1
- 1愛知医科大学医学部内科学講座(神経内科)
2名古屋大学大学院医学系研究科神経内科
3慶應義塾大学医学部生理学教室
4新潟大学大学院医歯学総合研究科神経生物・解剖学分野
5東京医科歯科大学難治疾患研究所医科学数理分野
6東京大学大学院理学系研究科生物科学専攻医科学数理研究室
7理化学研究所生命医科学研究センター医科学数理研究チーム
8星薬科大学薬理学研究室
9慶應義塾大学医学部皮膚科学教室
10愛知医科大学加齢医科学研究所
11名古屋大学大学院医学系研究科神経変性・認知症制御研究部門 - DOI:
- 10.1186/s13041-020-0561-1
本研究は、厚生労働科学研究委託費、日本医療研究開発機構(難治性疾患実用化研究事業、再生医療実現拠点ネットワークプログラム、疾患特異的iPS 細胞の利活用促進・難病研究加速プログラムを含む)(15ek0109025h0002、16bm0609003h0005、16ek0109025h0003、17ek0109243h0001、18ek0109243h0002、19ek0109243h0003、19dm0107105、19bm0804003h0003)、日本学術振興会・文部科学省科学研究費助成事業(15H01568、17H05707、17K19465、19H03576)、慶應義塾基軸プロジェクト研究推進プログラム、SBMAの会の支援を受けて行われました。
お問い合わせ先
研究内容に関して
愛知医科大学医学部 内科学講座(神経内科)
准教授 岡田 洋平
報道に関して
愛知医科大学 庶務課
AMED事業に関して
日本医療研究開発機構 戦略推進部 難病研究課
日本医療研究開発機構 戦略推進部 再生医療研究課