2022-04-07 自治医科大学医学部,日本医療研究開発機構
抗がん剤の開発にはさまざまな手法がありますが、正常細胞を傷害せずに、がん細胞の増殖を選択的に抑制する抗がん剤の開発は、極めて挑戦的な課題とされてきました。自治医科大学永井良三学長と仲矢丈雄准教授(病理学講座人体病理学部門)らの研究チームは、東京大学、理化学研究所、Prism Biolab社等との共同研究により、大腸癌に関わる転写因子KLF5を標的とする低分子化合物を新しい手法で開発し、KLF5の抑制作用だけでなく、一定程度の腫瘍選択的な増殖抑制効果を確認しました。
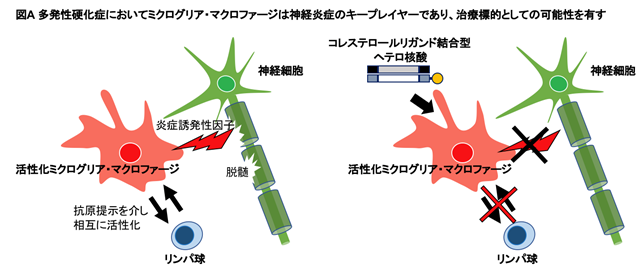
転写因子KLF5は腸上皮幹細胞からの腫瘍形成に必須の因子で、大腸癌の発症に深い関係があります。このことから、KLF5は大腸癌治療における有望な標的分子と考えられてきました。しかしKLF5は3次元の立体構造を解明できない天然変性蛋白であり、立体構造に基づく分子標的薬の創薬は不可能とされていました。
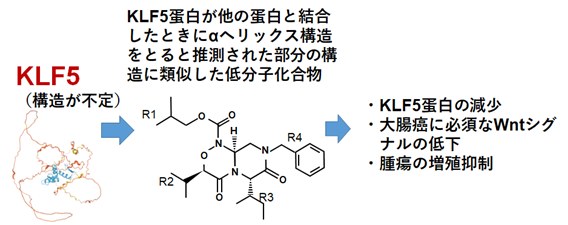
今回の研究では、KLF5が他の蛋白と相互作用した時に、KLF5蛋白のなかでαヘリックス構造をとる領域を数学的に推測し、その部分の構造を模倣した低分子化合物を合成しました。この化合物はKLF5蛋白と他の蛋白との相互作用を抑制する可能性があると考えられます。
興味深いことに、開発化合物は正常細胞に対する傷害は軽く、癌細胞をより選択的に抑制しました。また、KLF5蛋白だけでなく、大腸癌細胞の増殖に重要なWntシグナルも抑制しました。さらに、皮下に癌細胞を移植したマウスに本化合物を投与したところ、明らかな副作用を認めることなく、腫瘍の増生を抑制しました。
がんを起こす原因因子は、KLF5のような構造の決まらない蛋白であることが多く、これらの蛋白に対する分子標的薬の開発は進んでおりません。今回の化合物はそのまま臨床的に使用できるわけではなく、詳細な作用機序も十分に解明されていませんが、アミノ酸配列に基づいて構造の定まらない標的蛋白の重要な領域を推測し、その部分を模倣する低分子化合物を開発するという方法は、がんの新しい分子創薬として期待されます。 本研究成果は、2022年3月28日付で、米国化学会の科学誌ACS Medicinal Chemistry Letters に掲載されました。
論文情報
- 論文名
- Development of Low-Molecular-Weight Compounds Targeting the Cancer-Associated KLF5 Transcription Factor
- 著者
- Takeo Nakaya, Kenichi Aizawa, Yuki Taguchi, Kentaro Tsuji, Sachi Sekine, Kazuhiro Murakami, Masaji Kasai, Hirofumi Nakano, Yasumitsu Kondoh, Shingo Dan, Atsushi Yoshimori, Hiroyuki Kouji, Dai Takehara, Toru Suzuki, Hiroyuki Osada, Masayuki Murata, Akira Tanaka, and Ryozo Nagai*
- 掲載誌
- ACS Medicinal Chemistry Letters (2022)
- URL
- https://doi.org/10.1021/acsmedchemlett.1c00721
研究支援
本研究は、日本医療研究開発機構(AMED)次世代がん医療創生研究事業(P-CREATE)の支援を受けて実施されました。
お問い合わせ先
本件に関するお問い合わせ先
自治医科大学
学長 永井 良三(ながい りょうぞう)
AMED事業に関するお問い合わせ先
日本医療研究開発機構 (AMED)
創薬事業部 医薬品研究開発課
次世代がん医療創生研究事業 (P-CREATE)