2026-04-09 京都府立医科大学
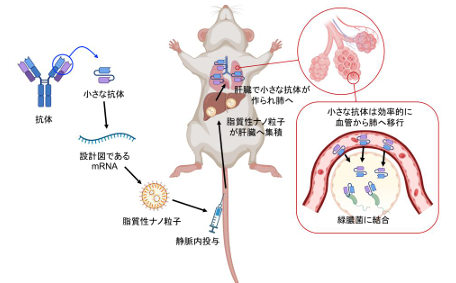
図1 本研究の概要
<関連情報>
- https://www.kpu-m.ac.jp/doc/news/2026/20260409press.html
- https://www.kpu-m.ac.jp/doc/news/2026/files/41498.pdf
- https://www.nature.com/articles/s41467-026-71040-8
Fc領域を持たない単鎖抗体を発現するmRNAを用いた、多剤耐性緑膿菌による気道感染の治療 Fc-free single-chain antibody mRNA therapy for airway infection of multidrug-resistant Pseudomonas aeruginosa
Mao Kinoshita,Ken Kawaguchi,Yuki Mochida,Nguyen B. T. Le,Atsushi Kainuma,Naoko Takeda-Miyata,Motohiro Kojima,Teiji Sawa & Satoshi Uchida
Nature Communications Published:09 April 2026
DOI:https://doi.org/10.1038/s41467-026-71040-8
Abstract
With the growing threat of antimicrobial resistance (AMR), alternatives to conventional antibiotics are urgently needed. Here, we show that mRNA-based therapeutics encoding single-chain variable fragment (scFv) antibodies—small, targeted antibody derivatives—provide robust protection against Pseudomonas aeruginosa, a major multidrug-resistant pathogen. We target the bacterial type III secretion system (T3SS), a needle-like apparatus used by the pathogen to inject toxins into host cells. When delivered intravenously via lipid nanoparticles, the scFv-encoding mRNA prompts sustained protein production, overcoming the typically short half-life of small antibody fragments. This treatment mitigates lung inflammation, reduces bacterial load, and improves survival in clinically relevant models, including immunocompromised mice infected with multidrug-resistant, exoU-positive (highly cytotoxic) clinical isolates. We find that Fc-free scFv antibodies, consisting only of the antigen-binding domain, migrate more efficiently from the bloodstream to the lung epithelium—the primary site of infection—than their larger counterpart conjugated to an Fc domain. This enhanced tissue penetration results in superior therapeutic outcomes. Overall, mRNA-encoded, Fc-free antibody fragments represent a promising and versatile platform for combating life-threatening bacterial infections without relying on traditional antibiotics.