2021-10-12 北海道大学,国立感染症研究所,日本医療研究開発機構
ポイント
- 変異株やその他のコロナウイルスを中和し、優れた治療効果を示すヒト抗体を作製。
- コロナウイルスの保存部位を認識し、抗体の定常領域と協調的に活性を強めるユニークな抗体と判明。
- 新型コロナウイルス変異株やSARS関連コロナウイルスの治療薬として開発が進むことが期待。
概要
国立感染症研究所治療薬・ワクチン開発研究センターの高橋宜聖センター長、小野寺大志主任研究官、安達悠主任研究官、森山彩野主任研究官らと、北海道大学大学院薬学研究院の前仲勝実教授、喜多俊介特任助教らの研究グループは、新型コロナウイルス(SARS-CoV-2)変異株やSARSコロナウイルスなどのコロナウイルスに広く有効な新しいヒト抗体を単離し、構造決定及び病理評価を行うことに成功し、その高い中和活性と交差反応性のメカニズムを解明しました。
今回研究グループは、鳥取大学及びTrans Chromosomics社で開発した完全型ヒト抗体を作るマウス(TC-mAbTMマウス)から、SARS-CoV-2に対して強い抗ウイルス活性(中和活性)を有し、変異株やその他のコロナウイルスも中和できる抗体NT-193を単離しました。このNT-193抗体は、定常領域がIgG3タイプであることにより中和活性を増強するユニークな抗体であるとわかりました。さらに、IgG3タイプのNT-193抗体は他のSARS関連コロナウイルスに対しても強い中和活性を示したことから、広くSARS関連ウイルスに対して有効な抗体であると示唆されました。変異株(アルファ株やガンマ株)に対しても高い中和活性を示しました。
NT-193抗体はスパイクタンパク質の受容体結合部位(RBD)と高い結合活性を示すことから、NT-193とRBDとの複合体の立体構造をX線結晶構造解析により決定することができました。その結果、受容体ACE2結合領域とコロナウイルスの保存性の高い領域の両方のほぼ全てを認識する抗体であることを特定し、それぞれの領域が中和活性とコロナウイルス交差反応性に寄与することが明らかになりました。さらに、ハムスターを用いた感染実験からこれまでに臨床応用されている抗体医薬品と比較して、遜色のない優れた予防・治療効果を示すことがわかりました。
NT-193抗体は、新型コロナウイルス変異株に対する治療薬に加え、SARSコロナウイルスを含むSARS関連コロナウイルスに対する治療薬として開発が進むことが期待できます。
なお、本研究成果は、2021年8月24日(火)公開のImmunity誌に掲載されました。
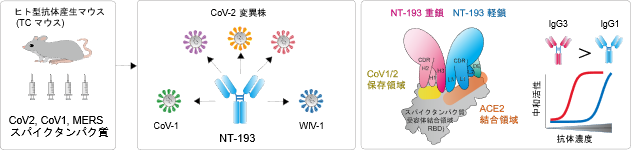
概要図.新型コロナ変異株やSARSに有効な新規抗体の作出とその特徴
背景
SARS-CoV-2ウイルスを中和するヒトモノクローナル抗体は、抗体カクテル療法等の治療薬にも利用されています。これまで出現したSARS-CoV-2ウイルス変異株の中には、中和抗体から逃避する能力を獲得したものも含まれ、変異株に活性を消失しない「交差中和抗体」を特定し、その中和メカニズムを科学的に理解することが新たな治療薬やワクチン開発に求められています。
研究手法
研究グループは、新型コロナウイルス(SARS-CoV-2)に対する新しいヒト抗体を単離するため、完全型ヒト抗体を作るマウス(TC-mAbTMマウス)を用いました。得られた交差中和抗体候補を抗ウイルス活性の強弱を基準に選別しました。最も有望な交差中和抗体候補について、スパイクタンパク質の受容体結合部位との複合体について立体構造を決定しました。最後に、交差中和抗体候補を感染動物実験により、その薬効を評価しました。
研究成果
本研究グループは、TC-mAbTMマウスから、変異株や他のコロナウイルスに結合するヒトモノクローナル抗体(NT-193)を単離しました。
NT-193は、抗体カクテル療法に使用されている抗体と比べた場合、従来株を同程度の高い活性で中和しました(図1左)。加えて、定常領域の種類(IgGサブクラス)を変えると、SARS-CoVウイルス等の他のコロナウイルスへの交差中和効果を高めることがわかりました(図1右)。
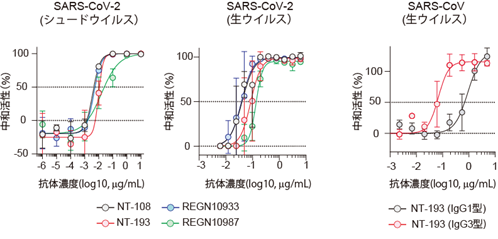
図1.SARS-CoV-2シュードウイルスへの中和活性(左)。SARS-CoV-2ウイルスへの中和活性(中)。SARS-CoVウイルスへの中和活性(右)。REGN10933及びREGN10987は抗体カクテル療法に使用されている抗体。
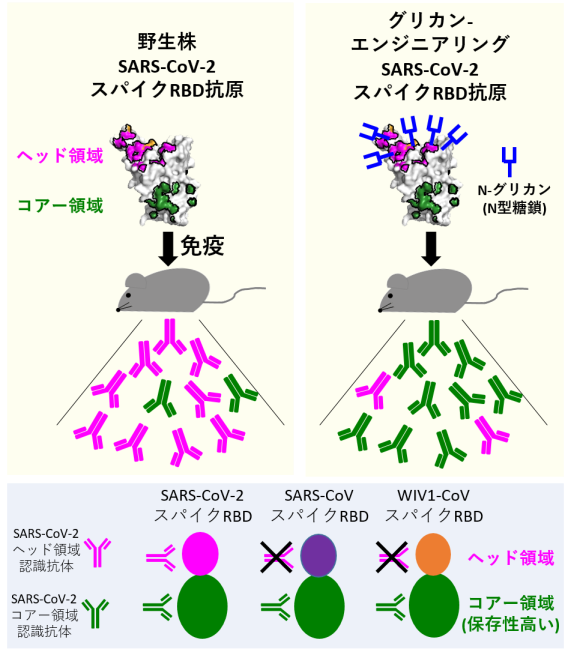
NT-193が標的としているスパイクタンパク質の受容体結合領域(Receptor Binding Domain; RBD)に結合する様子をX線結晶構造解析(分解能2.8Å)で明らかにしました(図2左)。すると、ヒト受容体であるACE2と同じようなアングルでRBDに結合するユニークな抗体であることがわかりました。加えて、抗体タンパク質を構成する重鎖と軽鎖が、それぞれSARS-CoV-2とSARS-CoVウイルスで保存性の高い領域と、ACE2結領域をそれぞれ認識することで、幅広い交差性と高い中和活性を両立していることが判明しました(図2右模式図)。
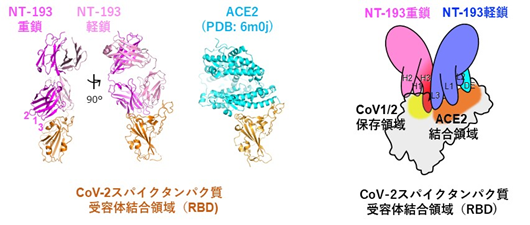
図2.NT-193とRBDの結合の様子NT-193-RBD複合体とACE2-RBD複合体の比較(左)。NT-193によるRBD認識の模式図(右)。
また、NT-193はアルファ変異株やガンマ変異株に対する中和活性を維持しており(図3)、新型コロナウイルスを感染させたハムスターに治療効果を有することが確認されています(図4)。
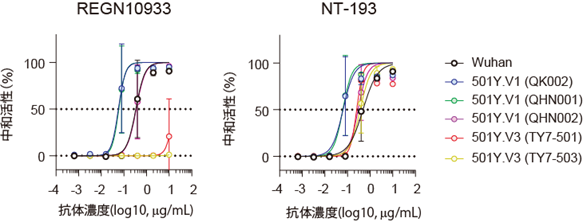
図3.コントロール抗体(左)とNT-193の変異株への中和活性Wuhan(従来株)に加え、501Y.V1(アルファ株)2株と501Y.V3(ガンマ株)3株に対する中和活性を比較検討した。
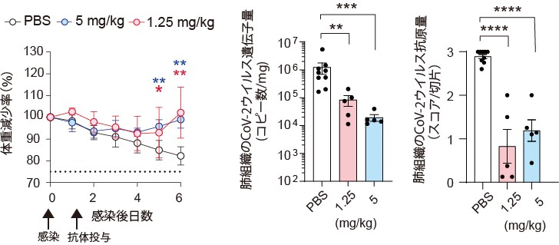
図4.SARS-CoV-2(従来株)を感染させたハムスターに治療効果ウイルス感染後1日後に記載量のNT-193抗体を投与し、体重減少を毎日観察するとともに(左)、6日後でのウイルス量を測定した(右)。
今後への期待
NT-193抗体は、新型コロナウイルス変異株に対する治療薬に加え、広くSARS関連コロナウイルスに対する治療薬として開発が進むことが期待できます。
研究支援
本研究は、国立研究開発法人日本医療研究開発機構(AMED)新興・再興感染症に対する革新的医薬品等開発推進研究事業(JP20fk0108298)、創薬等ライフサイエンス研究支援基盤事業(JP20am0101093)、特別経費(バイオサーフィス創薬国際連携研究教育拠点の構築(2018~2025年度))等の一環として行われました。
特記事項
本研究は、京都大学ウイルス・再生医科学研究所の橋口隆生教授ら、北海道大学人獣共通感染症国際共同研究所の澤洋文教授、佐藤彰彦客員教授ら、国立感染症研究所の鈴木忠樹部長、黒田誠センター長、福士秀悦室長ら、大阪大学の松浦善治教授、黒崎知博教授ら、Trans Chromosomics社の押村光雄代表取締役ら、鳥取大学の香月康宏准教授らとの共同研究として行われました。
論文情報
- 論文名
- A SARS-CoV-2 Antibody Broadly Neutralizes SARS-related Coronaviruses and Variants by Coordinated Recognition of a Virus Vulnerable Site(新型コロナウイルス抗体はSARS関連ウイルスと変異株の弱点部位を認識することで幅広く中和することが可能である)
- 著者名
- 小野寺大志1、喜多俊介2、安達 悠1、森山彩野1、佐藤彰彦3,4、野村尚生2、榊原修平5、井上 毅5、田所高志2、安楽佑樹2、湯本航平2、田 聡2、福原秀雄2,6、佐々木道仁4、大場靖子4、志和 希1、岩田奈織子1、永田典代1、鈴木干城7、佐々木慈英7、関塚剛史1、登内奎介1、孫 琳1、福士秀悦1、里深博幸8、香月康宏8、押村光雄9、黒崎知博5、黒田 誠1、松浦善治10、鈴木忠樹1、澤 洋文4,11、橋口隆生7、前仲勝実2,6、高橋宜聖1(1国立感染症研究所、2北海道大学大学院薬学研究院、3塩野義製薬株式会社、4北海道大学人獣共通感染症国際共同研究所、5大阪大学免疫学フロンティア研究センター、6北海道大学バイオサーフィス創薬グローバルステーション、7京都大学ウイルス・再生医科学研究所、8鳥取大学医学部生命科学科/染色体工学研究センター、9株式会社Trans Chromosomics、10大阪大学微生物病研究所、11北海道大学One Health Research Center)
- 雑誌名
- Immunity(一般科学誌)
- DOI
- 10.1016/j.immuni.2021.08.025
- 公表日
- 2021年8月24日(火)(オンライン公開)
お問い合わせ先
研究に関すること
北海道大学大学院薬学研究院
教授 前仲勝実(まえなかかつみ)
国立感染症研究所 治療薬・ワクチン開発研究センター
高橋宜聖(たかはしよしまさ)
北海道大学総務企画部広報課
国立感染研究所 総務部調整課
AMED事業に関すること
日本医療研究開発機構(AMED)
創薬事業部 創薬企画・評価課
新興・再興感染症に対する革新的医薬品等開発推進研究事業
創薬事業部 医薬品研究開発課
創薬等ライフサイエンス研究支援基盤事業(BINDS)