慢性期脊髄損傷治療へ応用目的での特許出願
2022-04-05 慶應義塾大学医学部,日本医療研究開発機構
慶應義塾大学医学部生理学教室の加瀬義高助教、佐藤月花(大学院医学研究科博士課程学生)、岡野雄士(医学部学生)、岡野栄之教授らの研究グループは、ヒトiPS細胞(注1)から作製した神経細胞(ニューロン)において神経突起(注2)伸長を促進する新しいシグナル経路(注3)を解明しました。また、抗生物質を産生する細菌であるストレプトマイセス属(注4)が産生する化合物RK-682が今回発見したシグナル経路を促進し、ヒトのニューロンの神経突起を伸ばすことを発見しました。
神経突起の伸長メカニズムの研究は、これまでヒト以外のニューロン(マウス、ラット、ゼブラフィッシュなど)で行われてきましたが、本研究は、今後の慢性期脊髄損傷の再生治療への応用を見据えて、ヒトiPS細胞から作製したヒトのニューロンに着目して行いました。ヒトiPS細胞由来神経幹細胞/前駆細胞(注5)を移植しての脊髄損傷再生医療では、それら移植された細胞がニューロンへ分化した後に、宿主のニューロンへ神経突起をいかに伸ばせるのかが再生の重要なポイントとなります。
研究の結果、GADD45G/p38 MAPK/CDC25Bというシグナル経路が、神経突起の骨組みとなる微小管(注6)の重合を促進する酵素であるCRMP2(注7)に作用して神経突起を伸ばすことがわかりました。このGADD45G(注8)という遺伝子は、ヒトの大脳の進化に重要な役割を果たしていることは知られていましたが、ヒトのニューロンにおける機能はわかっておらず、今回初めてニューロンにおける役割が解明されました。また、RK-682はこのシグナル経路のp38 MAPK/CDC25Bを活性化することで神経突起を伸ばすことがわかりました。
さらに、本グループは、これまでにヒトiPS細胞由来神経幹細胞/前駆細胞をγ-セクレターゼ阻害剤(注9)であるDAPTで処理した後に脊髄損傷部位に移植することにより、慢性期脊髄損傷が治療可能であることをマウスレベルで明らかにしてきました(注10)が、γ-セクレターゼ阻害剤の中でもCompound 34がDAPTの10分の1の量で同等の効果を発揮することを発見しました。
本研究成果は、2022年4月4日(米国東部標準時)に国際学術雑誌『iScience(Cell Press)』に掲載されました。また、これら発見を慢性期脊髄損傷に対するヒトiPS細胞由来神経幹細胞/前駆細胞の移植治療に応用できる形での特許出願も行いました。今回の研究成果はヒトの大脳の進化に重要なGADD45Gのニューロンでの役割を初めて解明したという生物学的意義と、慢性期脊髄損傷治療への応用という、基礎研究での成果を実際の臨床につなぐ、トランスレーショナルリサーチとしての意義の両面を有するものです。
研究の背景と概要
慶應義塾大学医学部生理学教室と整形外科学教室では、亜急性期脊髄損傷に対するヒトiPS細胞由来神経前駆細胞を用いた再生医療(試験 ID:UMIN000035074再生医療等提供計画、計画番号:jRCTa031190228)の臨床研究を開始しています。しかし、脊髄損傷患者の大部分は慢性期にあり、かつ、慢性期脊髄損傷は亜急性期の治療より難しいことから、慢性期脊髄損傷の治療技術の開発が求められています。
本研究グループは、これまでにγ-セクレターゼ阻害剤のDAPTをヒトiPS細胞由来神経幹細胞/前駆細胞に添加することで、移植後に分化したニューロンの神経突起が伸長し慢性期脊髄損傷モデルマウスを治療することに成功してきました。しかし、ヒトの神経突起伸長がどのようなメカニズムで生じているのか、どのようにすれば伸長を促進できるか、わかっていない部分がありました。
本研究では、γ-セクレターゼ阻害剤で前処理したヒトiPS細胞由来神経幹細胞/前駆細胞の集合体であるニューロスフェア(注11)一つひとつを、RNA-seq(注12)で解析して全転写産物を調べ、キーとなっている遺伝子を探すための網羅的解析を行いました。するとGADD45Gという遺伝子の発現が際立って高くなっていることが明らかになりました。さらに関連タンパク質の発現や、リン酸化の状態を調べていくと、このGADD45Gがp38のリン酸化を惹起し、さらにリン酸化p38がCDC25Bのリン酸化を惹起していることが明らかになりました。最終的には、CRMP2の514番目のトレオニン(threonine)の脱リン酸化を促進することで神経突起の骨組みである微小管の重合を促し、神経突起伸長を促進していることがわかりました(図1)。
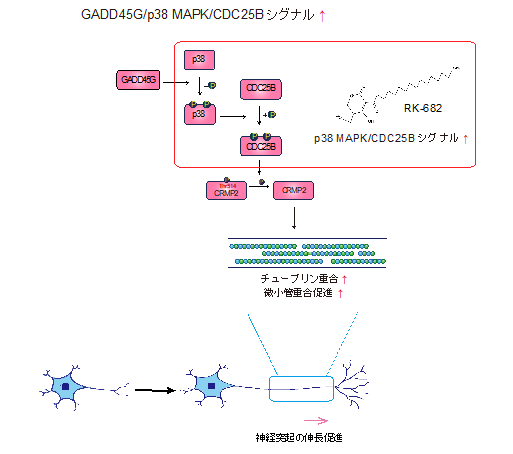
図1 GADD45G/p38 MAPK/CDC25Bシグナルのニューロンにおける役割神経幹細胞/前駆細胞から分化したニューロンはGADD45Gの発現が上昇し、p38のリン酸化を引き起こし、さらにCDC25Bのリン酸化を引き起こすことで最終的に神経突起の骨組みである微小管を重合する酵素であるCRMP2の514番目のトレオニン(threonine)のリン酸化を外すことで微小管の重合が促進されて神経突起が伸びる。RK-682は赤で囲んだ中のシグナルを促進して神経突起を伸ばす。
また、細菌の一種であるストレプトマイセス属が産生する化合物RK-682は、この新たに発見されたメカニズムの中のp38のリン酸化を維持することで、p38 MAPK/CDC25Bのシグナル経路を増強し、神経突起を伸長することがわかりました。さらに本研究グループでは、これまでγ-セクレターゼ阻害剤にはDAPTを使用してきましたが、Compound 34というγ-セクレターゼ阻害剤がDAPTの10分の1の量で同等の効果を発揮することを発見しました。
これら研究成果を、Cell Pressの『iScience』に発表するとともに、慢性期脊髄損傷治療に応用する目的で、「神経突起伸長促進用キット及びその使用」(出願番号:特願2021-089367)として特許出願を行いました。
さらに、興味深いことに、このシグナル経路の最初の起点であるGADD45Gは、遺伝子の発現を促進する遺伝配列上のエンハンサー(注13)がヒト特異的に欠失しているhCONDEL(注14)という遺伝子群のひとつです。マウスやチンパンジーではGADD45Gのエンハンサーは欠失しておらず、神経幹細胞/前駆細胞の増殖がヒトよりも劣っているため大脳が小さいと考えられています。しかしながら、幹細胞の状態から分化したニューロンのレベルではどのような機能を発揮しているのか全くわかっておらず、今回の神経突起伸長に関わっているという発見は、ニューロンでのGADD45Gの役割を解明した初めての報告となります。ヒトES細胞(注15)から作製したニューロンにおいても、ニューロンの成熟度が上がる過程でGADD45Gの発現が上昇してくることから、ヒトにおいては、幹細胞の状態から終末分化細胞であるニューロンになった後の精細なこの遺伝子の発現上昇が、ニューロンが機能を発揮するために必要な要素であることがわかりました。
研究の成果と意義・今後の展開
今回の研究では、ヒト以外の動物種ではなく、ヒトのニューロンでの神経突起伸長メカニズムを解明し、そのメカニズムに立脚した神経突起伸長化合物RK-682と強力なγ-セクレターゼ阻害剤作用を有するCompound 34を同定したものです。未だ課題の残る慢性期脊髄損傷治療のブレイクスルーとなる可能性がある成果です。
さらに、GADD45Gは、ヒトの大脳がなぜ他の動物種と異なり、大きく進化できたのかを説明できる遺伝子として注目されており、その遺伝子のニューロンにおける役割を初めて発見できた本研究結果は進化生物学的にも意義のある成果といえます。
まずは慢性期脊髄損傷治療への応用を見据えていますが、今回発見したシグナル経路の強度が老化とともに減少してしまうのかどうか、もしそうならばこのシグナル経路を増強すれば若返りにつながるのか、また他の神経軸索が変性してしまう神経変性疾患でも共通のメカニズムがあるのかどうかなど、現在検証を開始しています。
特記事項
本研究は、日本医療研究開発機構(AMED)・再生医療実現拠点ネットワークプログラム疾患・組織別実用化研究拠点(拠点A)「iPS細胞由来神経前駆細胞を用いた脊髄損傷・脳梗塞の再生医療」、JSPS科研費(JP 19K18438)、日本損害保険協会交通事故医療特定研究助成、武田科学振興財団の支援によって行われました。
論文・特許
論文
- 英文タイトル
- The GADD45G/p38 MAPK/CDC25B Signaling Pathway Enhances Neurite Outgrowth by Promoting Microtubule Polymerization
- タイトル和訳
- GADD45G/p38 MAPK/CDC25Bシグナル経路は微小管の重合を促進して神経突起を伸長する
- 著者名
- 加瀬義高、佐藤月花、岡野雄士、岡野栄之
- 掲載誌
- iScience(Cell Press)
- DOI
- 10.1016/j.isci.2022.104089
特許
- 発明の名称
- 神経突起伸長促進用キット及びその使用
- 発明者
- 加瀬義高、岡野栄之
- 特許出願人
- 学校法人慶應義塾
- 出願番号
- 特願2021-089367
用語解説
- (注1)iPS細胞
- 山中因子であるOct3/4, Sox2, Klf4などの転写因子を導入することにより、多分化能を人工的に持たせた細胞。
- (注2)神経突起
- ニューロンにおいて核を含む細胞体から伸ばす長細い突起のこと。この神経突起が伸び、他のニューロンと接続して信号のやりとりをすることができる。
- (注3)シグナル経路
- ひとつの刺激から次々と刺激や信号が伝達する仕組み、経路のこと。今回の研究ではGADD45G→p38のリン酸化→CDC25Bのリン酸化→CRMP2の脱リン酸化、とシグナルが伝わる。
- (注4)ストレプトマイセス属
- グラム陽性菌の一属で、ここに属する放線菌などからストレプトマイシン(抗結核薬)などの抗菌薬が誕生している。
- (注5)神経幹細胞/前駆細胞
- 未分化な状態を保ったまま増殖することができる自己複製能と、中枢神経系を構成するニューロン、アストロサイト、オリゴデンドロサイトの3系統の細胞へと分化することができる組織幹細胞。
- (注6)微小管
- 細胞の骨組みである細胞骨格のひとつ。
- (注7)CRMP2(Collapsin Response Mediator Protein 2)
- トレオニンの514番目が脱リン酸化されると微小管の重合を促進するタンパク質。その他の部位がリン酸化や脱リン酸化されると別の作用を生じる。
- (注8)GADD45G
- この遺伝子はヒトでだけ、その発現を上昇させるエンハンサーという遺伝子上の配列が失われている。マウスやチンパンジーなどではGADD45Gの発現が神経幹細胞/前駆細胞で高いため、神経幹細胞/前駆細胞の増殖能が低く抑えられているが、ヒトの神経幹細胞ではGADD45Gの発現が低くなるため、神経幹細胞/前駆細胞増殖が盛んになり大脳が大きく進化できたと考えられている。ただし、神経幹細胞/前駆細胞から分化したニューロンではGADD45Gが神経突起の伸長に重要であることが本研究で明らかになった。ヒトのES細胞から分化させたニューロンにおいても、その成熟に伴いGADD45Gの発現量が増加しており、神経幹細胞/前駆細胞と異なりニューロンではその機能を果たすためには、精細なGADD45G発現上昇が重要であることがわかってきた。
- (注9)γ-セクレターゼ阻害剤
- 神経系においては神経幹細胞からニューロンへの分化を促進する。脊髄損傷治療に用いる神経幹細胞/前駆細胞に添加している薬剤。
- (注10)
- 「脊髄損傷治療用ニューロスフェア誘導剤及びその使用」(出願番号:2019-215161、公開番号:2021-084882、発明者:加瀬義高、 大久保寿樹、 中村雅也、 岡野栄之)として特許出願と論文発表(doi:10.1016/j.stemcr.2018.10.022, 著者:大久保寿樹、加瀬義高、岡野栄之ら)もしている。
- (注11)ニューロスフェア
- 神経幹細胞/前駆細胞の集合体。今回の解析では100 μm直径のものを用いた。
- (注12)RNA-seq
- 細胞などの遺伝子発現量を転写レベルで網羅的に解析する手法。
- (注13)エンハンサー
- 当該遺伝子の発現を促進させる作用を有する遺伝子上の配列。
- (注14)hCONDEL
- ヒト特異的に遺伝上の配列が欠失している領域を指す。GADD45G以外にはアンドロゲン(男性ホルモン)受容体のエンハンサーもヒト特異的に欠失しているため、ヒトとマウスでは男性ホルモンの利き方が異なっていると考えられている。
- (注15)ES細胞
- 受精卵の内部細胞塊という箇所から作製される万能性の細胞のこと。
お問い合わせ先
本発表資料のお問い合わせ先
慶應義塾大学医学部 生理学教室
教授 岡野 栄之(おかの ひでゆき)
本リリースの配信元
慶應義塾大学信濃町キャンパス総務課:山崎・飯塚・奈良
AMED事業に関するお問い合わせ先
日本医療研究開発機構
再生・細胞医療・遺伝子治療事業部 再生医療研究開発課