ゲノム多様化領域に起因した生命現象の解明へ
2019-04-22 国立遺伝学研究所
Platanus-allee is a de novo haplotype assembler enabling a comprehensive access to divergent heterozygous regions
Rei Kajitani, Dai Yoshimura, Miki Okuno, Yohei Minakuchi, Hiroshi Kagoshima, Asao Fujiyama, Kaoru Kubokawa, Yuji Kohara, Atsushi Toyoda & Takehiko Itoh
Nature Communications 10, Article number: 1702 (2019) DOI:10.1038/s41467-019-09575-2
東京工業大学、国立遺伝学研究所、東京大学の共同研究グループは、真核生物のゲノム配列決定において、両親由来の配列を区別し、高精度にそれぞれを決定する、新しい情報解析手法の開発に成功しました。
ヒトなど真核生物のゲノム情報は、両親から受け継いだ情報を持ち合わせていますが、今までは両親由来ゲノムの差異を無視して配列決定を行うことが一般的でした。しかしながら、この差異の大きな領域は、種々の昆虫の表現型(紋様)との関連や、ヒトでの免疫型の決定、さらには疾患との関連も報告されるようになっています。そのため、簡便に両親由来の配列を区別して解析できる手法が求められていたのです。
研究チームが開発した「Platanus-allee(プラタナス アリー)」と呼ばれる新しいプログラムは、特殊な装置や前処理を必要とせず、現在の主流になっている次世代シークエンサーの大規模な断片配列データのみから、両親由来の配列を高精度に再構築できる画期的なものです。
本成果は、2019年4月12日付けの「Nature Communications」に掲載されました。
研究支援
本研究は、文部科学省科研費「新学術領域研究『学術研究支援基盤形成』」先進ゲノム解析研究推進プラットフォーム(16H06279)および、16H04719, 15H0597などの支援を受けて行われました。
国立遺伝学研究所の貢献
比較ゲノム解析研究室および先端ゲノミクス推進センターは、両親由来の配列を区別して高精度にゲノム配列を再構築できる新たな手法の開発にあたり、さまざまな生物種から高分子かつ高品質なゲノムDNAを調製するとともに、現在主流となっている次世代型シーケンサを用いて、開発・評価用にショートリードやロングリードの配列決定を実施しました。
- Platanus-allee:http://platanus.bio.titech.ac.jp/platanus2
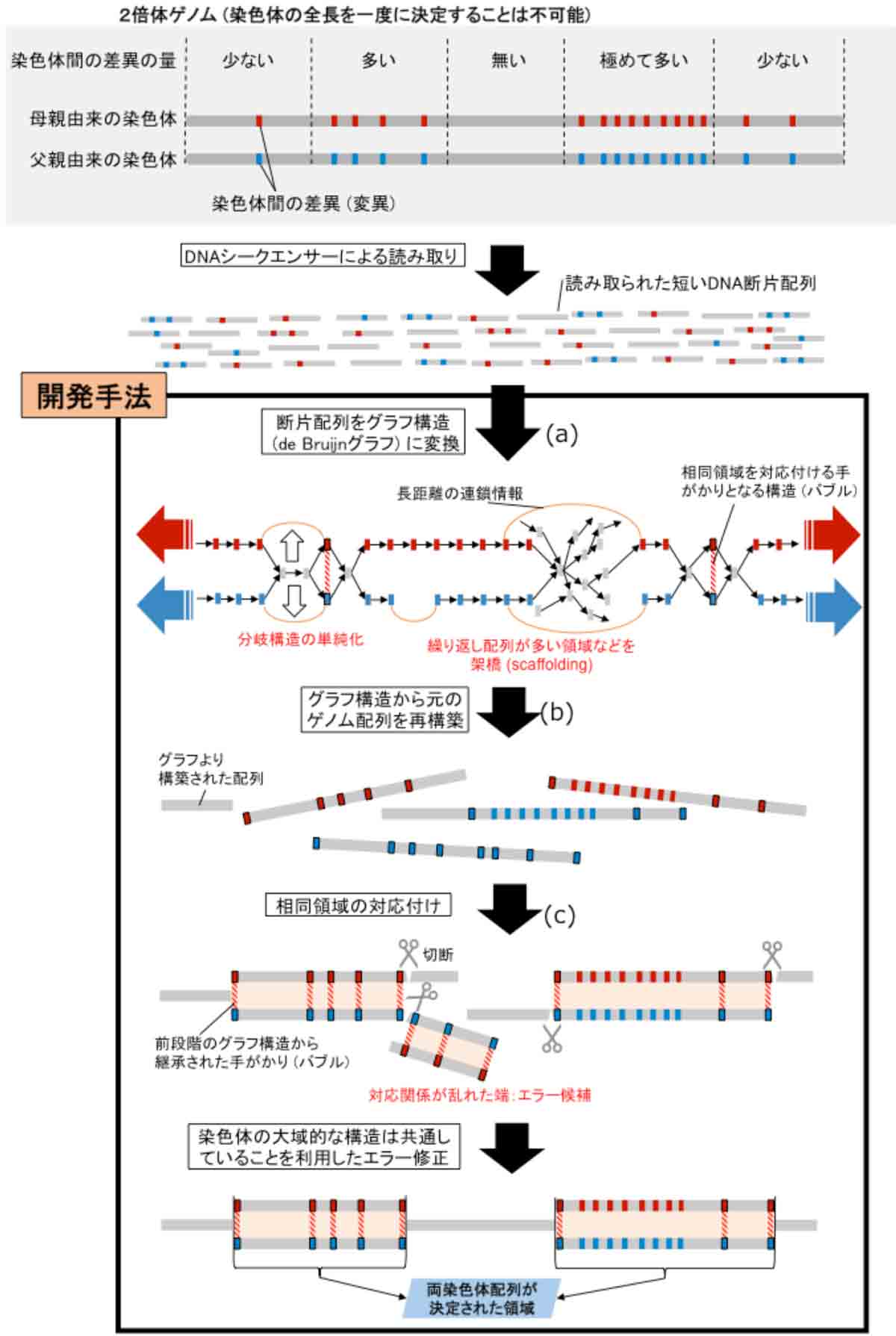
図:新たな情報解析プログラム「Platanus-allee」のアルゴリズムの模式図
プレスリリース資料
東京工業大学
情報・システム研究機構 国立遺伝学研究所
両親由来のゲノム配列を個別に決定する新手法
-ゲノム多様化領域に起因した生命現象の解明へ-
【要点】
○ 両親由来のゲノム配列を高精度にかつ個別に決定する情報解析手法
○ 哺乳類、無脊椎動物、植物などを対象にしたテストで性能を確認
○ 従来は解析が困難だった両親間のゲノムが多様化した領域を解析
【概要】
東京工業大学 生命理工学院 生命理工学系の梶谷嶺助教、吉村大大学院生(博士 後期課程 3 年・研究当時)、奥野未来研究員、伊藤武彦教授らの研究チームは、国 立遺伝学研究所の豊田敦特任教授、小原雄治特任教授、東京大学の窪川かおる特任 教授らと共同で、真核生物のゲノム配列決定において、両親由来の配列を区別し、 高精度にそれぞれを決定する、新しい情報解析手法の開発に成功した。
ヒトなど真核生物のゲノム情報は、両親から受け継いだ情報を持ち合わせている が、今までは両親由来ゲノムの差異を無視して配列決定を行うことが一般的だっ た。しかしながら、この差異の大きな領域は、種々の昆虫の表現型(紋様)との関 連や、ヒトでの免疫型の決定、さらには疾患との関連も報告されるようになってい る。そのため、簡便に両親由来の配列を区別して解析できる手法が求められていた。
研究チームが開発した「Platanus-allee(プラタナス アリー)」と呼ばれる新し いプログラムは、特殊な装置や前処理を必要とせず、現在の主流になっている次世 代シークエンサー(注1)の大規模な断片配列データのみから、両親由来の配列を 高精度に再構築できる画期的なものだ。
本成果は、2019 年 4 月 12 日付けの「Nature Communications」に掲載された。
●背景
2001 年にヒトの全ゲノム配列が決定されてから、わずか 20 年足らずの間に、 次世代シークエンサーの登場と解読システムの性能向上により、ゲノム配列を決 定するコストは数万分の1になり、読み取り時間も劇的に短くなっている。
ヒトに代表される一般的な高等動植物のゲノムは、母親と父親の両親から受け 継いだ両方の情報を持ち合わせている。しかしながら現状では、この差異を無視 して、両親由来のゲノム情報全体をモザイク状につなぎ合わせることで、ゲノム 配列を解読する手法が一般的に用いられている。
近年、両親由来のゲノム配列(相同染色体)間で差異が大きい領域が存在し、 これが様々な表現型(例えば、昆虫の体の紋様や性決定、ヒトの免疫型決定や疾 患など)とリンクしている事例が報告されている。そのため、両親由来のゲノム 配列を“分けて”解析することの重要性が認識されるようになってきたが、その 実現は技術・コストの面から多くの問題が存在していた。
●研究の内容
本研究で開発された解析手法は、ショートリード(注2)と呼ばれる次世代シ ークエンサーが産出するデータの精度の高さを活かして、まず、大量の断片配列 内に存在する一塩基の違いをも区別できるグラフ構造(注3)に変換する(図 a)。 次に、そのグラフ構造をショートリード間のペア情報を用いて単純化することで、 より長く繋がったゲノム配列を再構築する(図 b)。相同染色体との対応付けを配 列の類似情報から行い(図 c)、エラー修正などを行った上で最終的な配列を導き 出す。
研究チームでは、この手法を「Platanus-allee」というプログラムに実装し、 ホームページで公開した(http://platanus.bio.titech.ac.jp/platanus2)。さらにこ の手法を実際に、線虫、シロオビアゲハ、ナメクジウオ、サクラ、ヒトなどの各 種生物に適用したところ、その実効性を証明できた。
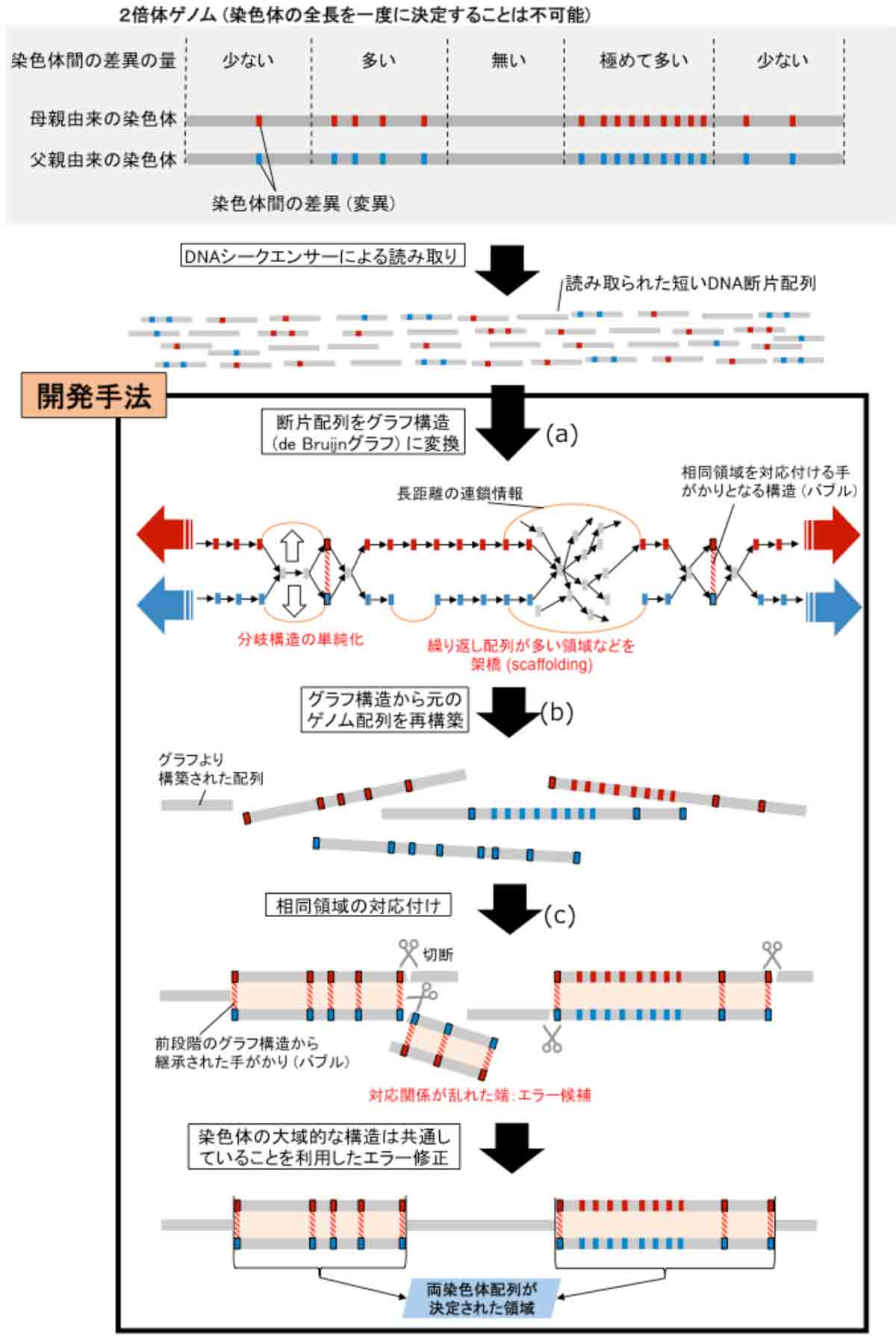 図:新たな情報解析プログラム「Platanus-allee」のアルゴリズムの模式図
図:新たな情報解析プログラム「Platanus-allee」のアルゴリズムの模式図
●今後の展開
研究開発された解析手法で、相同染色体間の複雑な変異情報が網羅的に収集可 能となる。これにより変異が蓄積したゲノム領域との関連が疑われている種分化、 多様性維持、免疫など重要な生命現象の解明が進むと考えられる。また、究極的 には、本研究成果を用いて、我々ヒトを含む“2 倍体生物が 2 セットの少し異な るゲノムを維持することで何を得たのか?”という根源的な問いに対する理解が 深化すると期待される。
【用語説明】
(注1) 次世代シークエンサー:
2004 年頃から登場した新しいタイプの塩基配列解読装置(シークエ ンサー)。最大の特徴は、それまでの機器(第一世代)と比べて圧倒 的に産出するデータ量が多い。その後も次々と新しいタイプのシー クエンサーが登場している。
(注2) ショートリード:
次世代シークエンサーの中で主流な機種が出力するタイプのデータ のこと。具体的には、ある程度の長さのゲノム断片の両端が 100~250 文字程度ずつの断片ゲノム配列(ショートリード)としてペアで読 まれる。最新の次世代シークエンサーからは、ショートリードが一 度に数億本(ペア)のレベルで産出される。
(注3) グラフ構造:
ノード(節)とエッジ(辺)で表現されるデータの集合体。ゲノム データでは、あるゲノム部分配列(ノード)が他のゲノム部分配列 (ノード)に繋がっているか(エッジ)の関係を記載したデータ集 合体。
本研究は、文部科学省科研費「新学術領域研究『学術研究支援基盤形成』」先進 ゲノム解析研究推進プラットフォーム(16H06279)および、16H04719, 15H0597 などの支援を受けて行われました。
【論文情報】
掲載誌:Nature Communications
論文タイトル:Platanus-allee is a de novo haplotype assembler enabling a comprehensive access to divergent heterozygous regions
著者:Rei Kajitani, Dai Yoshimura, Miki Okuno, Yohei Minakuchi, Hiroshi Kagoshima, Asao Fujiyama, Kaoru Kubokawa, Yuji Kohara, Atsushi Toyoda, and Takehiko Itoh
DOI:10.1038/s41467-019-09575-2
【問い合わせ先】
東京工業大学 生命理工学院 生命理工学系 教授 伊藤 武彦(いとう たけひこ)
【取材申し込み先】
東京工業大学 広報・社会連携本部 広報・地域連携部門
情報・システム研究機構 国立遺伝学研究所
リサーチ・アドミニストレーター室 報道担当