2023-06-23 量子科学技術研究開発機構
発表のポイント
- 遺伝子変異を「読み過ごす」作用を有する薬(アジスロマイシン)のがん予防効果を、家族性大腸腺腫症のモデルマウスを用いて評価
- アジスロマイシンの投与により、細胞増殖を抑制するタンパク質が正常に生成され、腸管ポリープの発生と悪性化を予防できることを解明
- 家族性大腸腺腫症の早期発生の予防法の開発に役立つことを期待
概要
国立研究開発法人量子科学技術研究開発機構(理事長 小安重夫)量子生命・医学部門放射線医学研究所放射線影響研究部の森岡孝満グループリーダーと柿沼志津子研究員らは、順天堂大学(学長 新井一)大学院医学研究科臨床遺伝学 新井正美教授、乳腺腫瘍学 齊藤光江教授、仙波遼子大学院生(大学院博士課程2023年3月時点)らとの共同研究で、遺伝子変異を「読み過ごす」薬で遺伝性の大腸がんを予防することに成功しました。
大腸がんは、日本におけるがん死亡原因の第2位で、そのうち5~10%は遺伝性の大腸がんです。特に家族性大腸腺腫症の患者さんの約42%は、がん抑制遺伝子APC(adenomatous polyposis coli)1)の一つに終止コドンを生じる点突然変異(ナンセンス変異)2)を生まれつき持っています。この変異があると、APCタンパク質の合成が途中で終了して、機能を持たない短いタンパク質が作られます。APCには、細胞増殖に関わるシグナルを抑制する機能があることから、正常なAPCタンパク質がなくなると細胞増殖を抑制できなくなります。家族性大腸腺腫症では、両親から受け継いだ2つのApc遺伝子のうち片方が生まれつき働かないため、正常な方の遺伝子が失われるという1回のイベントのみによって、機能するApc遺伝子をまったく持たない細胞が生まれます。これにより大腸全体に数百から数千の腺腫性ポリープが10歳代から発生します。標準的な治療法として「大腸全体の外科的切除」が選択されますが、生活の質(QOL:Quality of Life)を損なうため、新たな予防法の確立が求められています。
最近の研究で、タイロシン、エリスロマイシン、アジスロマイシンなどの特定のマクロライド系抗生物質は、終止コドンを「読み過ごす」作用(リードスルー効果)3)を有していることが細胞を用いた実験で示されました。特にアジスロマイシンは抗菌薬としてヒトに適用され低用量で効果があり副作用も少ないことから、我々は、アジスロマイシンがナンセンス変異を伴う家族性大腸腺腫症の予防薬として有望な候補と考えました。
そこで、アジスロマイシンのリードスルー効果が、遺伝性腫瘍の発生を予防しうるか(がん予防効果)を、Apc遺伝子にナンセンス変異を持ち家族性大腸腺腫症同様に腸管にポリープを発症するモデルマウスを用いて評価しました。その結果、アジスロマイシンはApc遺伝子のナンセンス変異部分を「読み過ごす」ことで正常なApcタンパク質の生成を促進し、腸管のポリープの発生と悪性化を予防することを初めて明らかにしました。今後、アジスロマイシンはナンセンス変異を有する家族性大腸腺腫症に対する予防薬として臨床応用の検討が期待されます。
本研究は、がんの予防薬や治療薬に関する論文が数多く発表されている国際誌「Biomedicine & Pharmacotherapy」に2023年6月3日にオンライン掲載されました。本研究は、JSPS科研費(JP20K07684、JP21H04932)の助成を一部受けています。
研究開発の背景と目的
アミノグリコシド系抗生剤の一部の薬剤は、抗菌作用に加えて、ナンセンス変異の終止コドンを「読み過ごす」ことで正常タンパク質の生成を促進する作用(リードスルー効果)を有していることが明らかになってきました。実際に、ナンセンス変異が原因で発症する嚢胞性線維症やデュシェンヌ型筋ジストロフィーの患者に対して、アミノグリコシド系抗生剤が予防薬として有用であることが臨床試験で示されました。その後、副作用の少ない合成化合物であるPTC124(アタルレン)が開発されて条件付きで承認され、長期的な経過観察データはまだ不足しているものの、これらの疾患に対する他の治療法が無いことから英国では使用が推奨されています。一方、リードスルー効果を持つ薬剤が遺伝性腫瘍に対する予防効果を持つかについては明らかにされていませんでした。
家族性大腸腺腫症は、ナンセンス変異が原因で生涯のうちに大腸がんを発症する遺伝性腫瘍症候群のひとつです。若年期から腺腫(ポリープ)を発生し、いずれほぼ100%ががんを発症します。このため、標準的な治療法として「大腸全体の外科的切除」が選択されますが生活の質(QOL:Quality of Life)が損なわれるため、画期的な予防法の確立が重要とされております。
最近の研究で、抗菌薬であるタイロシン、エリスロマイシン、アジスロマイシンなどの特定のマクロライド系抗生物質にもリードスルー効果があることが示されました。特にアジスロマイシンは抗菌薬としてヒトに適用され低用量で効果があり、副作用も少ないことから、アジスロマイシンが遺伝性腫瘍症候群を含むナンセンス変異を伴う遺伝性疾患の予防薬として有望な候補になると考えました。そこで、アジスロマイシンのリードスルー効果が遺伝性腫瘍の発生を予防しうるか(がん予防効果)を、Apc遺伝子にナンセンス変異を持ち家族性大腸腺腫症同様に腸管にポリープを発症するモデルマウス(C3B6F1 ApcMin/+ 4)、以下Minマウス)を用いて評価しました。
研究の手法と成果
本研究では、Apc遺伝子のナンセンス変異により自然に消化管にポリープが発生するMinマウスを用いました。このマウスは、浸潤癌に至る多段階発癌過程を病理学的に観察可能であるため、悪性化の予防試験に適しています。
Minマウスを4つの実験グループに分け、0(対照群として)、0.0125、0.05、または0.2 mg/mL のアジスロマイシン溶液を3週齢から継続して飲水投与しました(図1)。8週齢、12週齢、16週齢、20週齢で腸に発生したポリープの数、その病理学的特徴(良性・悪性)を調査しました。
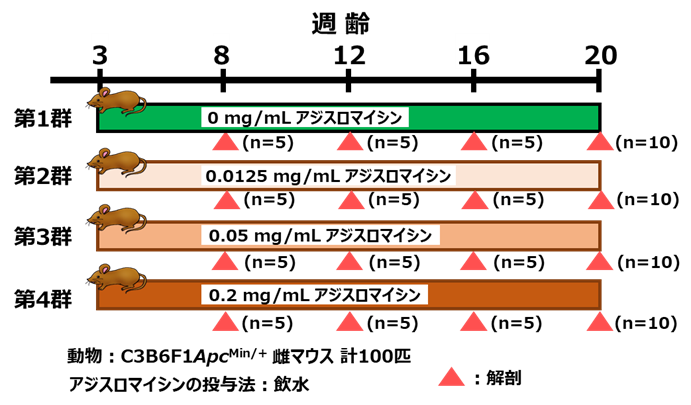
図1 実験群の設定
その結果、アジスロマイシン投与なしに比べて、投与グループではポリープの発生数が減少し、特に、16週齢では、0.0125 mg/mLのグループで有意に減少しました(図2)。また、病理組織的学的解析により、良性腫瘍と悪性腫瘍を識別して悪性腫瘍の割合の変化を比較したところ、投与なしのグループでは、悪性腫瘍の割合が時間と共に増加しましたが、アジスロマイシン投与の全てのグループでその割合が減少し、悪性化が抑制されたことが明らかになりました(図3)。
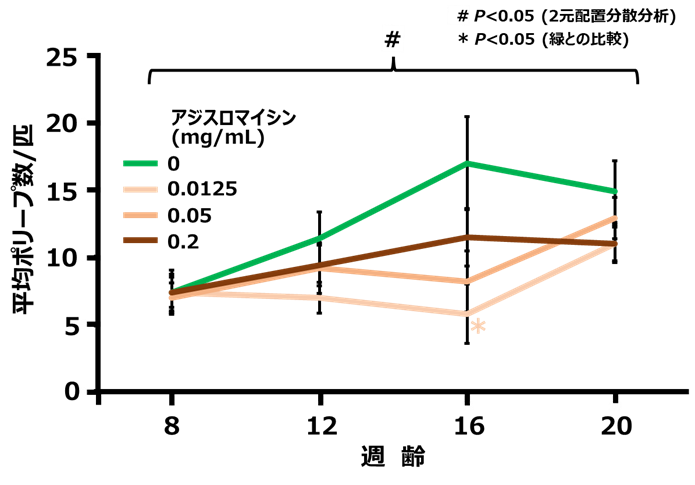
図2 アジスロマイシンによるポリープの抑制効果
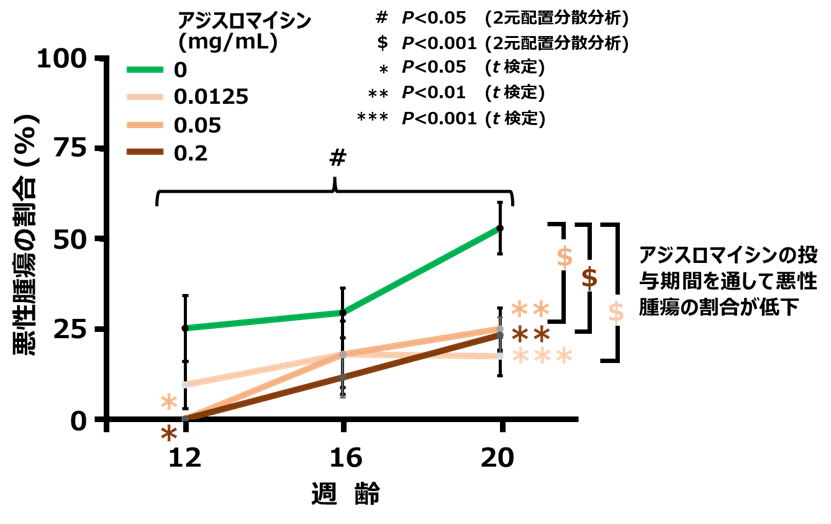
図3 アジスロマイシンによる悪性腫瘍の抑制効果
Apc遺伝子のナンセンス変異におけるアジスロマイシンのリードスルー効果を明らかにするため、抗体を用いて正常な小腸粘膜における正常APCタンパクの発現量を調べました。Minマウスは、2つあるApc遺伝子の片方にナンセンス変異があります。ナンセンス変異があると途中でタンパク質合成が終了してAPCタンパク質が短くなり、抗体は結合しません。正常な遺伝子または、リードスルー効果によりナンセンス変異が読み過ごされて合成が進めば、正常APCタンパク質が生成され、抗体が結合します(図4)。
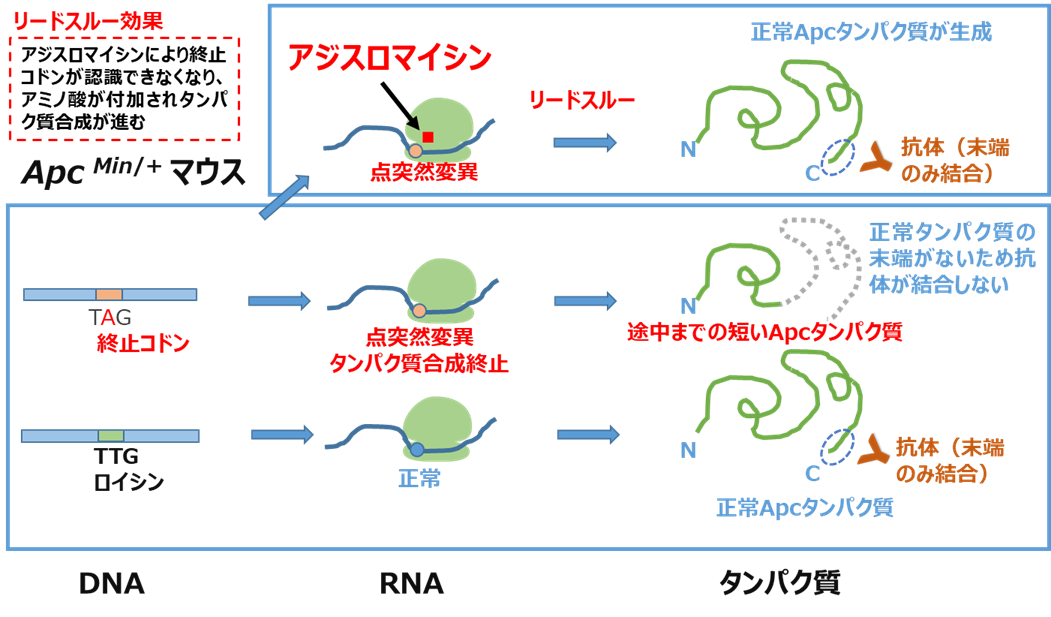
図4 Minマウスにおけるアジスロマイシンのリードスルー効果による正常タンパク質の生成機序
変異のないマウス(野生型マウス)の小腸粘膜に比べて、アジスロマイシンを投与していないMinマウスでは茶色が薄く抗体の結合量が少ないことから、細胞増殖を抑制する機能を持つ正常APCタンパク質の発現量が減少していますが、アジスロマイシンを投与すると茶色が濃くなり、その発現量が増加していることがわかりました(図5)。このことから、アジスロマイシンによってApc遺伝子のナンセンス変異がリードスルーされ、正常APCタンパク質の生成が促進されて、その量が増加して、がん化の進行を防いでいると考えられました。
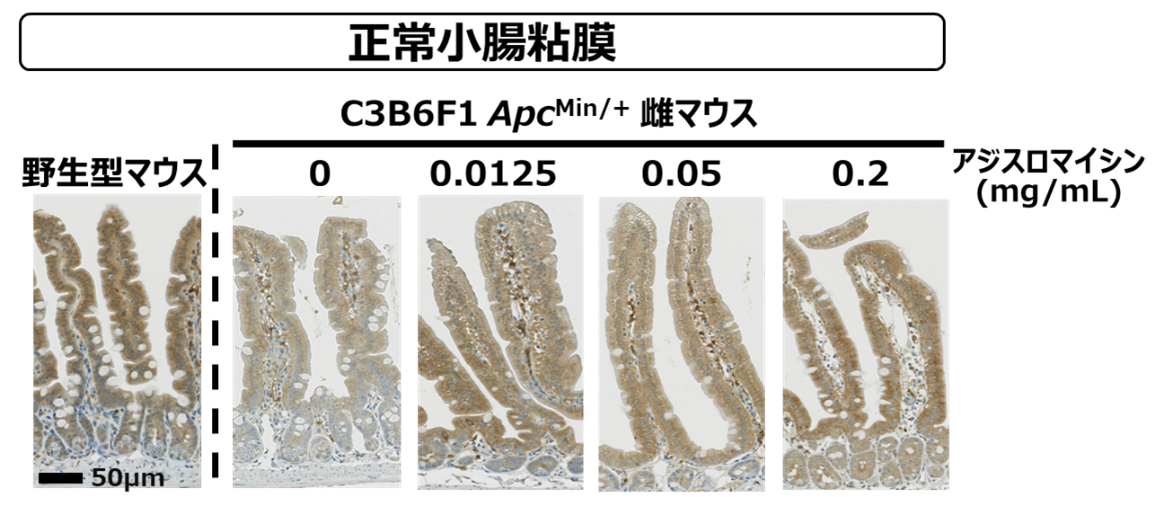
図5 アジスロマイシンによる正常APCタンパク質の増加効果
今後の展開
本研究により、Minマウスに、ナンセンス変異を読み過ごす作用(リードスルー)を有するアジスロマイシンを投与することで、正常なAPCタンパク質の生成を回復させ、ポリープの発生や悪性化を予防できることが初めて明らかになりました。同時に、今回の検討では、アジスロマイシンの濃度が高い場合は、強い抗菌作用により腸内細菌叢が乱れて、予防効果が低下する可能性も示唆されました。
今後、投与法の工夫や、抗菌作用を持たないリードスルー効果を有する薬剤を検討して、より効果的にポリープの発生を抑制し、外科的処置を必要としない予防法を構築することは、患者さんのQOLの向上にも寄与することが期待されます。更に、ナンセンス変異が原因の家族性大腸腺腫症以外の遺伝性腫瘍症候群にも応用が期待できます。
用語解説
1)がん抑制遺伝子APC(adenomatous polyposis coli)
細胞増殖や細胞分化などを誘導するWNTシグナル伝達を抑制する因子。APC遺伝子に異常があると、このシグナルが過剰に伝達され、細胞増殖が促進されます。
2)ナンセンス変異
DNAの塩基配列は3つの組合せ(コドン)で一つのアミノ酸を規定していますが、一部のコドンはその位置でタンパク質合成を終了させることを意味する終止コドンです。塩基の一つが突然変異により変化して終止コドンとなったものは、ナンセンス点突然変異と言われます。タンパク質をコードする塩基配列の途中でナンセンス変異が生じると、変異がない場合に比べてタンパク質の長さが短くなります。
3)リードスルー(read-through)効果
DNAの遺伝情報からタンパク質を合成する過程(翻訳)を終了する終止コドンが、遺伝情報の途中にある場合に、そのコドンを認識できなくする効果です。一部の薬剤がこの効果を持ち、薬剤の作用によって遺伝情報の途中にある終止コドンの認識ができなくなり、終止因子に代わってアミノ酸が付加されて最後まで翻訳が進み、正常にタンパク質が合成されて終了します。
4)C3B6F1 ApcMin/+マウス
家族性大腸腺腫症のモデルマウスは、Apc遺伝子のナンセンス変異をもちます。Apc遺伝子の2549番目のTがAに変異する事で850番目のアミノ酸ロイシン(TTG)が終止コドン(TAG)となりApcタンパク質の生成が途中で終了します。これまで多くの研究で用いられているC57BL/6J ApcMin/+マウスは、自然に消化管に多くのポリープを早期に発生するため、良性腫瘍の発生の解析に適しておりこれまで家族性大腸腺腫症のモデルマウスとして研究に利用されています。当研究部で開発したC57BL/6J ApcMin/+雄マウスとC3Hマウスの雌との第1世代(F1Min)であるC3B6F1 ApcMin/+マウスは、ポリープの数が6分の1に減少するため寿命が延長し、浸潤癌に至る多段階発癌過程を病理学的に観察可能であるため、悪性化の予防試験に適しています。(2021年3月5日プレス発表)
掲載論文
Ryoko Semba, Takamitsu Morioka, Hiromi Yanagihara, Kenshi Suzuki, Hirotaka Tachibana, Takahiro Hamoya, Yoshiya Horimoto, Tatsuhiko Imaoka, Mitsue Saito, Shizuko Kakinuma, Masami Arai.
Azithromycin induces read-through of the nonsense Apc allele and prevents intestinal tumorigenesis in C3B6F1 ApcMin/+ mice. Biomedicine & Pharmacotherapy, 164, 2023, https://doi.org/10.1016/j.biopha.2023.114968.