2026-04-23 京都大学iPS細胞研究所
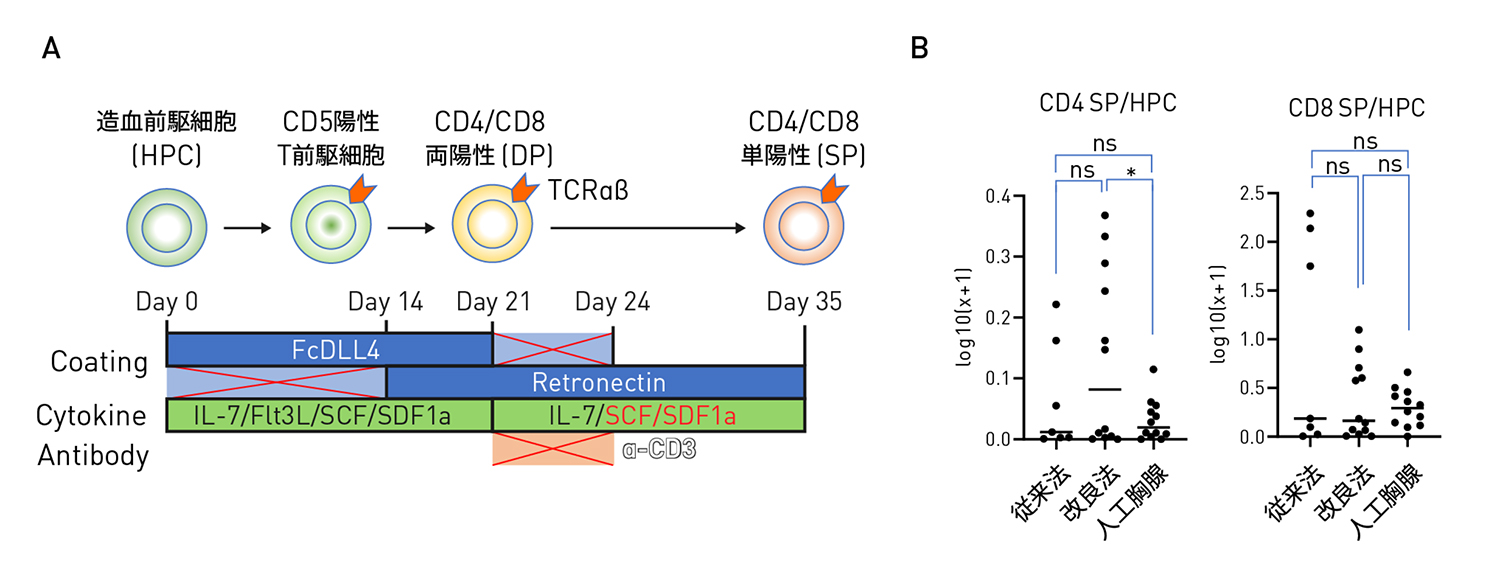
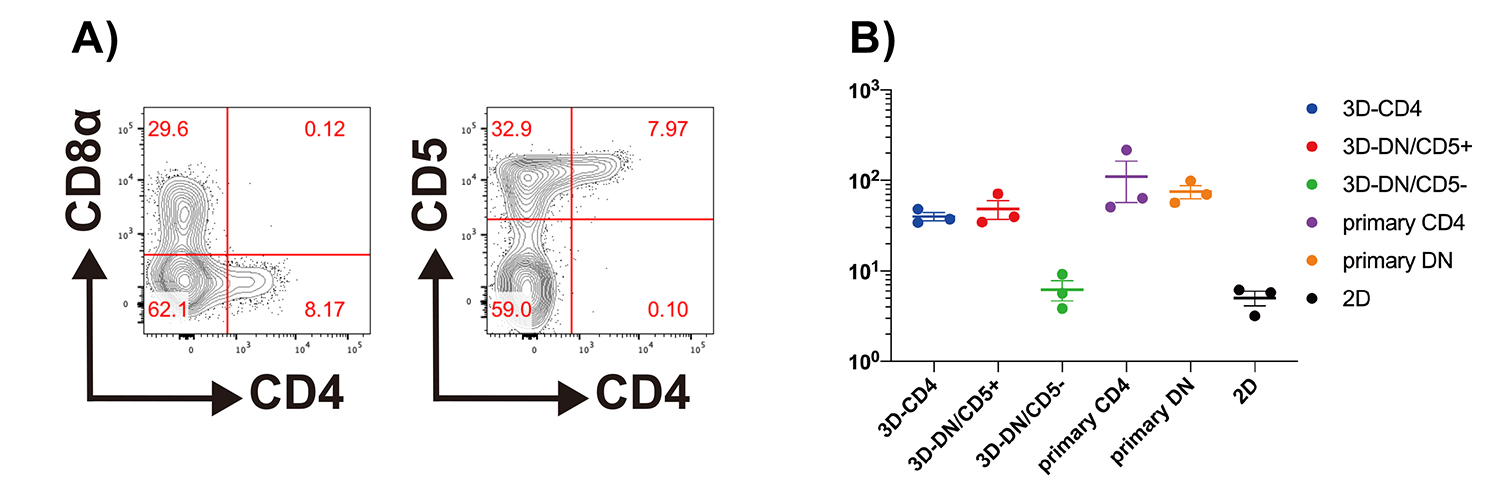
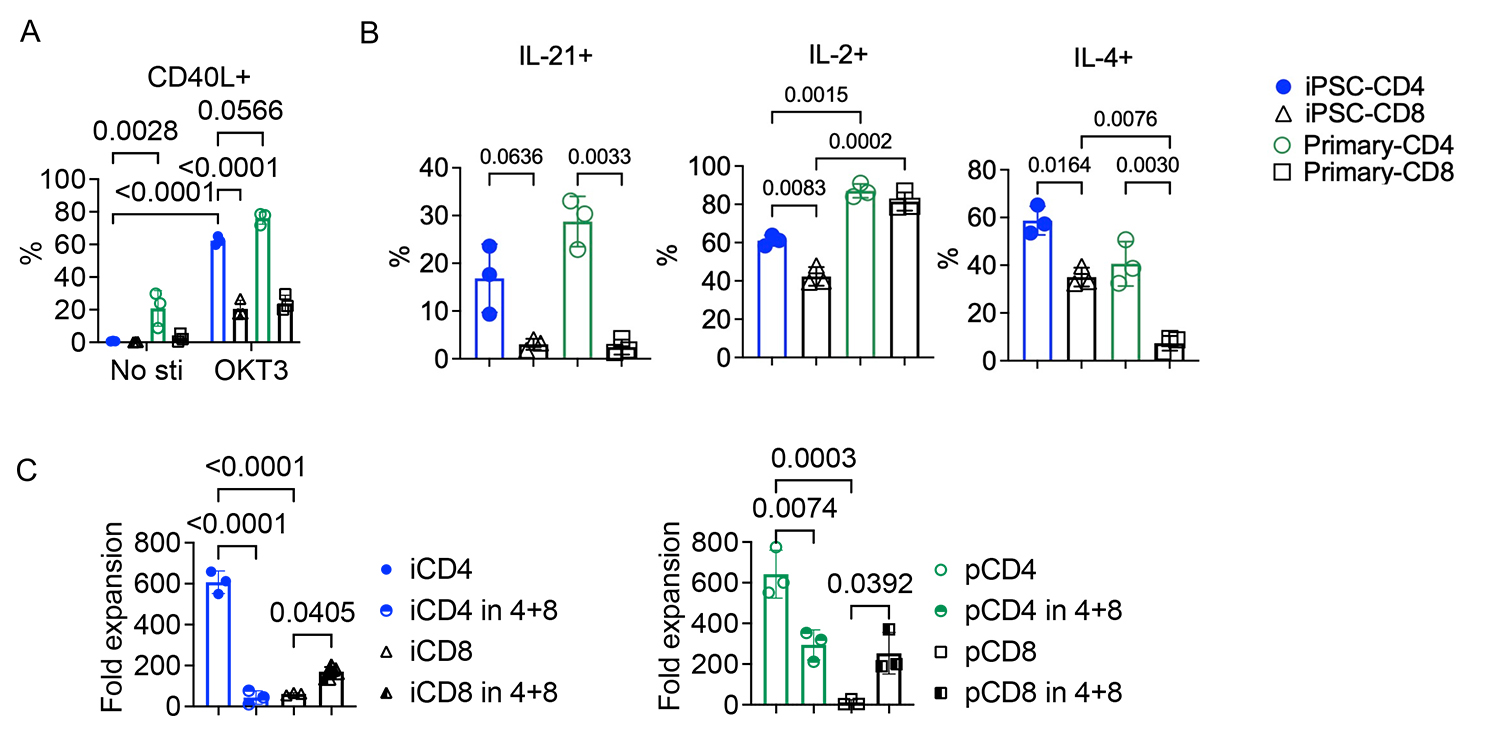
図1. CD4+T細胞の分化誘導法の開発
<関連情報>
- https://www.cira.kyoto-u.ac.jp/j/pressrelease/news/260423-130000.html
- https://www.cell.com/molecular-therapy-family/molecular-therapy/abstract/S1525-0016(26)00021-3
NotchおよびTCRシグナル伝達の段階特異的調節による、フィーダー細胞を用いないiPSC由来CD4単陽性ヘルパーT細胞の生成 Feeder-free generation of iPSC-derived CD4 single-positive helper T cells via stage-specific modulation of Notch and TCR signaling
Yohei Kawai ∙ Shin Kaneko
Molecular Therapy Published:January 20, 2026
DOI:https://doi.org/10.1016/j.ymthe.2026.01.020
Abstract
Induced pluripotent stem cell (iPSC)-derived T cells (iPS-T cells) represent a promising platform for adoptive immunotherapy, offering an unlimited source of T cells amenable to gene editing and rigorous quality control. While feeder-free in vitro redifferentiation systems have been successfully developed for CD8+ cytotoxic T cells, the generation of CD4+ helper T cells under similar conditions has remained elusive, despite their essential role in sustaining long-term immune responses. In this study, we established a feeder-free culture system for the generation of CD4 single-positive (SP) helper T cells from iPSCs under conditions that exclude TCR signaling, which otherwise biases differentiation toward the cytotoxic lineage. By precisely modulating Notch and integrin signaling in a stage-specific manner, we induced the differentiation of CD4 SP iPS-T cells expressing key helper-associated molecules, including CD40L and ThPOK, capable of promoting dendritic cell maturation. Notably, these cells also acquired cytotoxic activity upon repeated expansion while retaining robust proliferative capacity. Our findings provide a foundation for the scalable and consistent production of both CD4 SP helper and killer T cells from pluripotent stem cells, advancing the potential of iPSC-based immunotherapies.