2026-05-07 韓国基礎科学研究院(IBS)
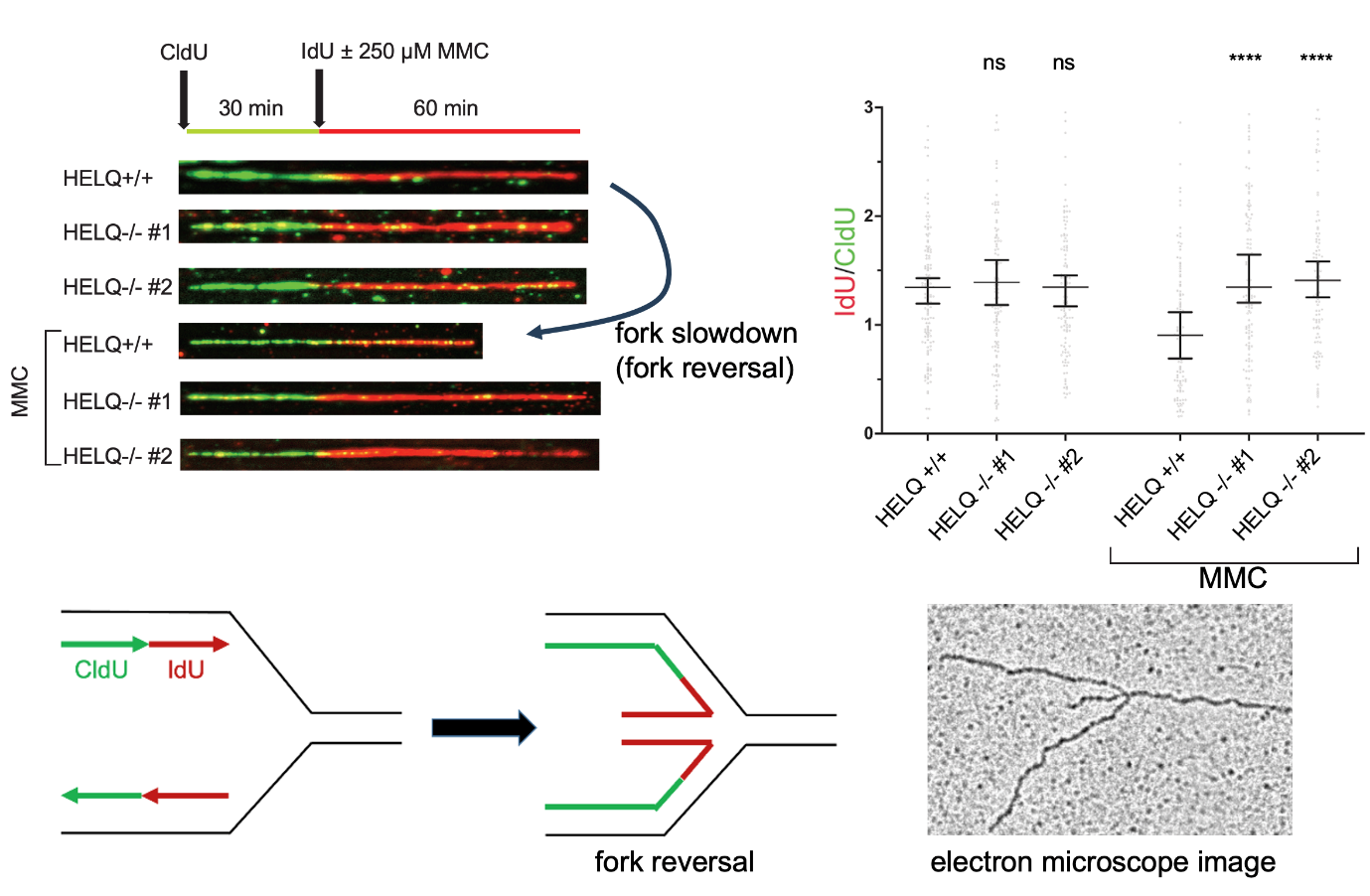
Figure 1. HELQ promotes fork slowdown (fork reversal) after treatment with a crosslinking agent
A representative figure showing that HELQ-deficient cells fail to undergo normal fork slowing after MMC (a crosslinking agent) treatment, consistent with defective fork reversal.
<関連情報>
- https://www.ibs.re.kr/cop/bbs/BBSMSTR_000000000738/selectBoardArticle.do?nttId=26673&pageIndex=1&searchCnd=&searchWrd=
- https://academic.oup.com/nar/article/54/8/gkag332/8664510
DNAヘリカーゼHELQは、BRCA2およびFANCD2を介した修復経路と協調して複製フォークの逆転を促進する The DNA helicase HELQ promotes replication fork reversal in coordination with BRCA2- and FANCD2-mediated repair pathways
Yerkin Dunbayev,Yen-Ju Chen,Lorenzo Sassi,Eun A Lee,Jae Sun Ra,Moonjung Choi,Anirban Mukherjee,Karen M Vasquez,Vincenzo Costanzo,Peter Chi,…
Nucleic Acids Research Published:29 April 2026
DOI:https://doi.org/10.1093/nar/gkag332
Abstract
HELQ is a 3′–5′ DNA helicase whose loss sensitizes cells to DNA-damaging agents, particularly DNA crosslinkers. HELQ interacts with the RAD51 paralog complex RAD51B–RAD51C–RAD51D–XRCC2 (BCDX2), a key mediator of replication fork reversal. Using DNA fiber assays, we show that HELQ and BCDX2 act epistatically to slow replication fork progression under replication stress. Because fork reversal transiently regresses nascent strands into a four-way junction and reduces net DNA synthesis, this fork slowing provides a functional readout of fork reversal. Directly supporting this model, electron microscopy reveals that reversed fork structures are reduced in HELQ-knockout cells. Consistent with a role in fork reversal, HELQ deletion suppresses nascent strand degradation when BRCA2- or FANCD2-dependent fork protection is lost. Mechanistically, biochemical reconstitution shows that HELQ is stimulated by RPA on fork substrates containing a leading strand gap, and these findings are consistent with the cell-based DNA fiber assays. Together, these results identify HELQ as a specialized regulator of replication fork remodeling that promotes fork reversal through the BCDX2 pathway.