3030-03-13 名古屋市立大学,生命創成探究センター,分子科学研究所, 基礎生物学研究所
名古屋市立大学薬学研究科の矢木宏和講師と自然科学研究機構生命創成探究センターの加藤晃一教授(分子科学研究所/名古屋市立大学兼任)らの研究グループらは、血液凝固因子の分泌の仕組みに着目して得られた知見に基づき、バイオ医薬品として用いられている糖タンパク質に、細胞内を移動する分子のパスポートを持たせることでその生産効率を大幅に高めることができることを示しました。本研究成果は、日本時間2020年3月13日午後7時に、自然科学のあらゆる領域を対象としたオープンアクセス学術誌「Nature Communications」に掲載されます。
【本研究成果のポイント】
抗体やエリスロポエチン[注1]などの糖タンパク質は広くバイオ医薬品[注2]として使われています。現在、これらの生物製剤のほとんどは、培養動物細胞を利用して生産されていますが、生産量を高めるために様々な方法が試みられています。本研究は、目的とする糖タンパク質にわずか10個のアミノ酸をつなげるだけで、その生産量を高められることを示したものです。本研究で見出された10アミノ酸からなる配列は、細胞内で作り出された糖タンパク質が細胞の外へと出荷されていく際の、輸送のパスポートとして働いています。
【背景】
これまで本研究グループは長年にわたり血液凝固因子[注3]が細胞の中から外へ分泌される仕組みについて調べてきました。特に、細胞の中で作り出された血液凝固第Ⅴ因子および第Ⅷ因子は糖タンパク質であり、それらが細胞の外へと向けて搬出されていく経路においてMCFD2[注4]とよばれるタンパク質が積荷の輸送体として関わっていることに着目しました。MCFD2の働きが損なわれると血液中の凝固因子が欠乏する疾患が引き起こされることから、MCFD2が積荷をどのように運んでいるのかという仕組みに興味が持たれていました。
【研究成果】
研究グループはまず、核磁気共鳴法[注5]を用いてMCFD2と血液凝固因子の分子の間の相互作用を詳しく調べました。その結果、MCFD2は第Ⅷ因子の中におけるアミノ酸10残基からなる特別な配列を認識していることがわかりました。この配列を取り除くと第Ⅷ因子の分泌量が著しく低下することから、この配列はMCFD2が第Ⅷ因子を積荷として見分けて効率的に運ぶための目印として働いていると考えられます。
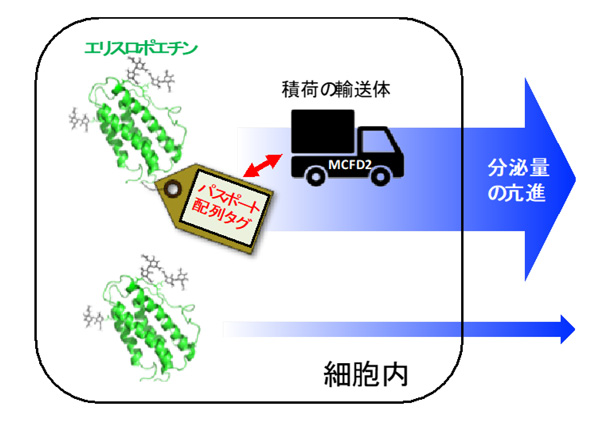
さらに興味深いことに、このアミノ酸10残基からなる配列をエリスロポエチンのような全く別の糖タンパク質に組み込んでみたところ、それらの糖タンパク質の細胞内の輸送効率が向上し、分泌量が2-3倍も上昇することがわかりました。この結果は、本研究で見出された特別な配列が、MCFD2が関わる細胞内の積荷糖タンパク質の輸送経路におけるパスポートとして働いていることを示しています。(図1)
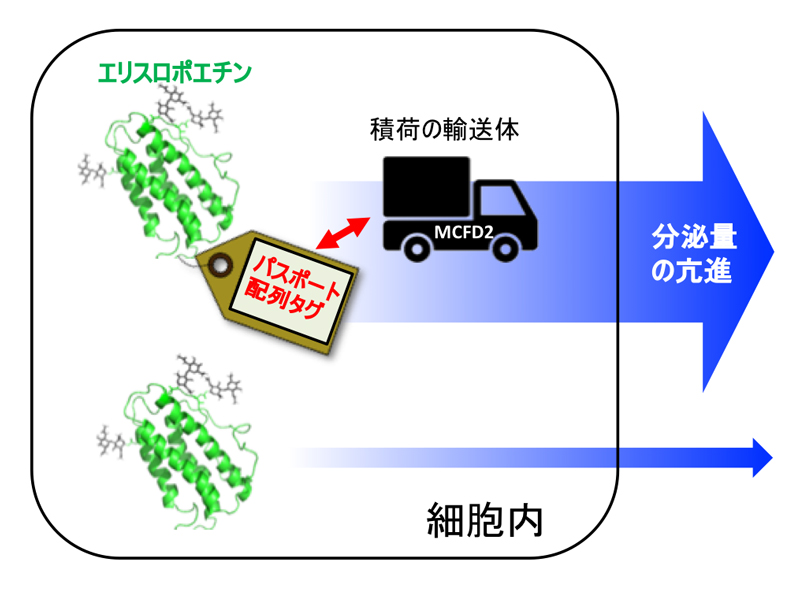
図1:エリスロポエチンに細胞内の物流を制御するパスポート配列を付けることで、分泌効率が上昇する。
【成果の意義および今後の展開】
本研究で用いたエリスロポエチンは、すでに医薬品として臨床で利用されています。こうした糖タンパク質に対して、わずか10残基のパスポート配列を付加することで分泌量が増加することは、バイオ医薬品の効率的な生産につながると期待されます。このことはバイオ医薬品の生産コストの面からも重要です。また、本研究の成果では、血液凝固因子の細胞内における輸送メカニズムも明らかにしていることから、血液凝固因子欠損症の発症の仕組みの理解を深めるとともに、血栓症のように血液凝固によって引き起こされる疾患の治療法の開発に貢献できる可能性があります。
[用語解説]
・エリスロポエチン [注1]:腎性貧血の治療に使われているバイオ医薬品。
・バイオ医薬品 [注2]:遺伝子組換え技術や細胞培養技術を用いて、細胞やバクテリアなどにより産生されるタンパク質を有効成分とする医薬品。
・血液凝固因子[注3]:血液の凝固を助け、出血を止めるために必要なタンパク質。血管が損傷し出血した際には、数多くの血液凝固因子が連鎖的に働いて止血が起こる。そのため、いずれの血液凝固因子が不足した場合においても、血液凝固反応が正常に起こらず、血友病のような出血性疾患が引き起こされる。一般に、血液凝固因子欠乏症の患者においては、血液凝固因子の遺伝子自体の変異が認められるが、血液凝固第V第VIII因子欠乏症の患者においては、血液凝固因子の遺伝子に対する変異は認められず、原因遺伝子産物の1つとしてMCFD2が同定されている。
・MCFD2[注4]:血液凝固第V第VIII因子欠乏症の原因遺伝子産物。血液凝固因子などの糖タンパク質を小胞体からゴルジ体に向けて輸送する。
・核磁気共鳴(NMR)法 [注5]:タンパク質などを磁場の中に入れてラジオ波を照射することで核スピンの共鳴現象を観測し、分子構造を原子レベルで解析することができる。
【研究グループ】
本研究は、名古屋市立大学、自然科学研究機構、産業技術総合研究所が参加した共同研究です。
【研究サポート】
本研究は、科学研究費補助金 基盤研究(JP19H03361, JP 24249002)および新学術領域研究(JP17H06414, JP25102008)等のサポートを受けて実施されました。
【掲載される論文の詳細】
掲載誌:Nature Communications
題目:Improved secretion of glycoproteins using an N-glycan-restricted passport sequence tag recognized by cargo receptor
著者:矢木宏和(名古屋市立大学)、矢木真穂(自然科学研究機構)、本田玲奈(名古屋市立大学、総合研究大学院大学)、太田裕作(自然科学研究機構)、齋藤泰輝(名古屋市立大学)、西尾美穂(名古屋市立大学)、蜷川 暁(自然科学研究機構)、鈴木康介(名古屋市立大学)、安西高廣(自然科学研究機構)、神谷由紀子(自然科学研究機構)、青木一洋(自然科学研究機構)、中西真人(産業技術総合研究所)、佐藤匡史(名古屋市立大学)、加藤晃一(名古屋市立大学、自然科学研究機構)
DOI:10.1038/s41467-020-15192-1
【問い合わせ先】
《研究全般に関するお問い合わせ先》
名古屋市立大学大学院薬学研究科
教授 加藤 晃一
自然科学研究機構 生命創成探究センター/分子科学研究所兼任
名古屋市立大学大学院薬学研究科
講師 矢木 宏和
《報道に関するお問い合わせ先》
名古屋市立大学 事務局企画広報課広報係
自然科学研究機構 生命創成探究センター広報担当
自然科学研究機構 分子科学研究所 研究力強化戦略室 広報担当
自然科学研究機構 基礎生物学研究所 広報室