2020-03-19 京都大学iPS細胞研究所
ポイント
- 希少難病CADASIL (cerebral autosomal dominant arteriopathy with subcortical infarcts and leukoencephalopathy) の病態メカニズムは未だに解明されておらず、治療法も存在しないのが現状です。
- 成熟した血管壁細胞注1)を患者さんのiPS細胞から分化誘導注2)する手法を確立しました。
- この手法で作製したCADASIL iPS細胞由来壁細胞には、患者さんの血管壁と同様の凝集体が観察されました。
- 患者さんのiPS細胞由来壁細胞の解析から、血管形成や構造の不安定化がCADASILで生じている可能性が示されました。
1. 要旨
山本由美研究員(現・国立循環器病研究センター病態代謝部、元・京都大学CiRA増殖分化機構研究部門)、井上治久教授(京都大学CiRA増殖分化機構研究部門/京都大学医学部附属病院臨床研究総合センター・理化学研究所)らの研究チームは、猪原匡史部長(国立循環器病研究センター脳神経内科)、曽根正勝特定准教授(京都大学糖尿病・内分泌・栄養内科)らの研究グループとともに、遺伝性脳小血管病CADASIL患者のiPS細胞から血管壁細胞を分化誘導し、その病態を試験管内で再現することに成功しました。この病態モデルの解析により、細胞の増殖や遊走に関係する血小板由来成長因子受容体β(PDGFRβ)注3)シグナルの異常が、病態を生じる可能性が見いだされました。
この研究成果は2020年3月19日午前10時にMolecular Brain誌でオンライン公開されました。
2. 研究の背景
希少難病CADASIL (cerebral autosomal dominant arteriopathy with subcortical infarcts and leukoencephalopathy)とは、血管壁細胞(ペリサイト、血管平滑筋細胞)に特異的に発現する一回膜貫通型受容体NOTCH3遺伝子の変異による優性遺伝性脳小血管病です。CADASIL患者は、毛細血管や細動脈などの小血管の狭窄や血管平滑筋細胞の変性などの病的変化により、脳梗塞や脳の深部の神経線維が障害される白質障害、さらには認知症を発症しますが、その病態メカニズムは未だに解明されておらず、治療法も存在しないのが現状です。これまでその頻度(有病率)は人口10万人あたり数名と言われていましたが、最近のゲノム解析では,CADASILを起こしうるNOTCH3遺伝子の変異を100人に1人が持つという発表もなされており、脳梗塞の治療薬開発のために病態を再現するモデルを用いた病態メカニズムの解明が強く望まれています。
3. 研究結果
研究グループは、まず既存の血管内皮細胞の分化誘導手法を改良し、成熟した血管壁細胞を患者さんのiPS細胞から分化誘導する手法を確立しました(図1)。この新たな手法により分化誘導したCADASIL iPS細胞由来壁細胞において、CADASILの病態としてこれまでに知られている、NOTCH3タンパク質の細胞外部分の凝集、細胞骨格アクチン繊維の構造異常、およびPDGFRβの増加が再現されていることが確認されました。また、CADASIL患者の血管壁に観察されるGOM (Granular osmiophilic material)注4)と呼ばれる凝集体が再現され、CADASILに見られるようにNOTCH3細胞外部分とHtrA1というタンパク質が含まれていました(図2)。これは、患者さんiPS細胞由来の壁細胞が、CADASILの病態モデルとして信頼できることを示しています。
さらに、健常コントロール群との比較の結果、CADASILの壁細胞において細胞遊走能が亢進しており、これに変異NOTCH3と過剰発現したPDGFRβが関わっていることが示唆されました。PDGFRβは、血管壁細胞の増殖と遊走の切り替えに関与することが知られています。CADASILの壁細胞では、PDGFRβが過剰発現することにより、血管新生の際の増殖と遊走の切り替えが正常に働かなくなり、結果として血管形成や構造の不安定化につながることでこの病気を引きおこすのではないかと考えられます。
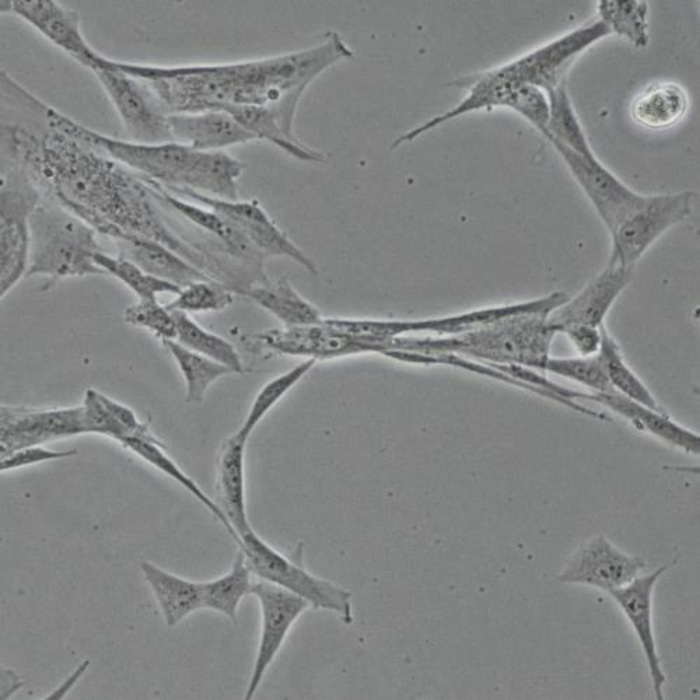
(図1)iPS細胞から分化誘導した血管壁細胞
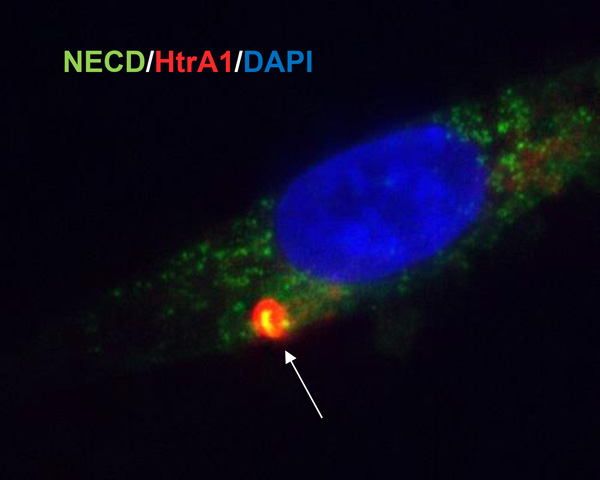
(図2)CADASIL iPS細胞由来壁細胞のGOM様沈着物
(矢印)
4. まとめ
今後、CADASILの病態モデルが、詳細な病態メカニズムの解明だけでなく、治療薬の探索に利用されることが期待されます。
5. 論文名と著者
- 論文名
Human iPS cell-derived mural cells as an in vitro model of hereditary cerebral small vessel disease - ジャーナル名
Molecular Brain - 著者
Yumi Yamamoto1,2, Katsutoshi Kojima3, Daisuke Taura3, Masakatsu Sone3, Kazuo Washida4,
Naohiro Egawa5,6,12, Takayuki Kondo5,6,7, Eiko N. Minakawa8, Kayoko Tsukita5,6, Takako Enami5,7, Hidekazu Tomimoto9, Toshiki Mizuno10, Raj N Kalaria11, Nobuya Inagaki3, Ryosuke Takahashi12, Mariko Harada-Shiba2, Masafumi Ihara4, Haruhisa Inoue5,6,7 - 著者の所属機関
- 日本学術振興会 特別研究員
- 国立循環器病研究センター病態代謝部
- 京都大学大学院医学研究科糖尿病・内分泌・栄養内科学
- 国立循環器病研究センター脳神経内科
- 京都大学iPS細胞研究所
- 理化学研究所バイオリソース研究センター(BRC)iPS創薬基盤開発チーム
- 理化学研究所革新知能統合研究センター(AIP)iPS細胞連携医学的リスク回避チーム
- 国立精神・神経医療研究センター神経研究所疾病研究第四部
- 三重大学大学院医学系研究科認知症医療学講座
- 京都府立医科大学神経内科学
- ニューカッスル大学神経科学研究所脳血管研究グループ
- 京都大学大学院医学研究科臨床神経学
6. 本研究への支援
本研究は、科学研究費助成事業(24.7954, 26830039, 16K18387, 18K07058)と日本医療研究開発機構(JP16ek0109130, JP18jm0210053, 20ek0210126s0102)により支援されました。
7. 用語説明
注1)血管壁細胞
周皮細胞(ペリサイト)や平滑筋細胞等から構成される。血管内腔を覆う内皮細胞を、基底側から裏打ちする細胞で、血管の構造および機能を司る。
注2)分化誘導
個体の発生に関わる分子を添加調整することにより、iPS細胞など多能性幹細胞から求める細胞種に変化させ作製すること
注3)血小板由来成長因子受容体β(Platelet-Derived Growth Factor receptor beta: PDGFRβ)
PDGFは、主に間葉系細胞(線維芽細胞、平滑筋細胞、グリア細胞等)の遊走および増殖などの調節を通じて血管新生に関与する増殖因子であり、血小板のみならず上皮細胞や内皮細胞など様々な細胞によって産生される。PDGFの受容体であるPDGFRには、alpha, betaのサブタイプがあり、PDGFRβは、血管新生に重要な役割を持ち、炎症や創傷治癒過程で発現が上昇する。
注4)Granular osmiophilic material(GOM)
主に電子顕微鏡下で観察されるオスミウム好性顆粒状物質で、CADASILに疾患特異的な病理学的所見であり、脳血管のみならず全身の血管壁で見られる。