2021-03-04 理化学研究所
理化学研究所(理研)生命機能科学研究センター染色体分配研究チームの北島智也チームリーダー、オーレリアン・クートワ研究員(研究当時)らの研究チームは、染色体分配装置である「紡錘体[1]」について解析し、卵子[2]がつくられる際の紡錘体の機能および形が動原体[3]と微小管[4]の接続を介して調整されていることを発見しました。
本研究成果は、卵子の染色体数異常[5]をもたらす原因の一つと考えられている紡錘体の異常を理解することに貢献すると期待できます。
卵子は、卵母細胞[2]が減数分裂[6]することでつくられます。遺伝情報が卵子に正しく伝えられるためには、減数分裂において染色体分配装置である紡錘体が正しく形成される必要があります。研究チームはこれまでに、卵母細胞の減数分裂における紡錘体形成には、染色体のくびれ部分にある構造(動原体)が重要であることを見いだしていました。動原体は、紡錘体を構成する微小管が染色体を捕捉するための接続点です。今回、研究チームは、哺乳類のモデルとしてマウスを用い、卵母細胞の減数分裂において動原体と微小管の接続を不安定化させる実験を行いました。この卵母細胞における紡錘体形成を解析したところ、紡錘体の極に集積するべき「微小管形成中心[4]」の配置が異常となり、また、紡錘体が過剰に伸びて正しい形をとれないことが明らかになりました。これらのことから、卵子が正しく染色体を分配するためには、動原体と微小管の接続を介して紡錘体が調整されることが重要であると考えられます。
本研究は、科学雑誌『EMBO Reports』オンライン版(3月3日付)に掲載されました。
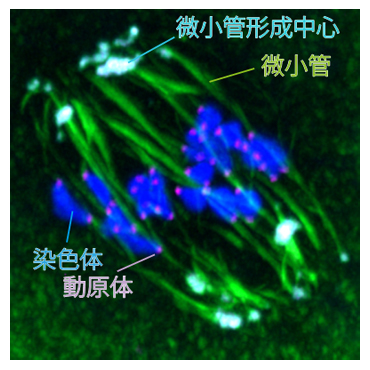
マウス卵母細胞における紡錘体
背景
母親の遺伝情報が正しく次世代に伝えられるためには、配偶子である卵子に染色体が正しく分配される必要があります。卵子に染色体を分配する過程が、卵母細胞の減数分裂です。ヒトを含む哺乳類の卵母細胞は卵巣の中に蓄えられており、排卵の前に減数分裂の分裂期へと進行します。
分裂期に入った卵母細胞は、まず、染色体を分配するための細胞内装置である「紡錘体」を形成します。紡錘体は二つの極を持ち、複製された染色体をそれぞれの極に向かって引っ張ることで、染色体を分配します。研究チームはこれまでの研究から、マウス卵母細胞において、紡錘体の二極性の獲得には「動原体」と呼ばれる染色体のくびれ部分の構造体が必要であることを見いだしてきました注1)。動原体は、微小管が染色体を捕捉するための接続点となる構造体ですが、紡錘体の二極化をどのように制御しているかは分かっていません。
今回、研究チームは、マウス卵母細胞を用いて、動原体と微小管の接続が紡錘体の機能と形成にどのように関わるのかを調べました。
注1)2020年5月27日プレスリリース「卵母細胞における染色体分配装置の形成機構を解明」
研究手法と成果
研究チームはまず、減数分裂における紡錘体形成の過程をライブイメージング[7]により高解像度で録画しました。得られた画像データから形成過程にある紡錘体を三次元で再構築し、その時間変化を定量的に解析した結果、紡錘体の二極性の獲得は三つのステップに分けて考えられることが分かりました(図1)。
第一のステップは、紡錘体の伸長です。減数分裂の分裂期に入ってすぐにつくられた球状の紡錘体が、両方向に伸長した形に変化していきます。この伸長とあわせ、多くの微小管形成中心が紡錘体の伸長方向(両極)へと移動していきます。第二のステップは、紡錘体の伸長の停止です。紡錘体は正しい長さまで伸長すると正確に伸長を停止させ、多くの微小管形成中心を両極にとどめます。第三のステップは、「微小管形成中心」の移動を完了させるプロセスです。

図1 紡錘体が二極性を獲得する三つのステップ
三次元再構築した画像で観察した紡錘体形成過程。紡錘体形成中心(緑)と染色体(マゼンタ)の位置を蛍光像で示す。第一のステップでは、減数分裂の分裂期に入った直後の球状の紡錘体(左端)が上下方向に伸長する。第二のステップでは、紡錘体が正しい長さで伸長を停止することで、多くの微小管形成中心が両極にとどめられる(右から2番目)。第三のステップで、紡錘体の中央に残った微小管形成中心(矢頭)の移動が完了する(右端)。スケールバーは10マイクロメートル(μm、1μmは1,000分の1mm)。
そして、紡錘体が伸長を停止したときには、多くの微小管形成中心が紡錘体の両極に位置しているものの、少数は紡錘体の中央に位置していることが分かりました(図2)。これら少数の微小管形成中心の動きを詳細に解析したところ、伸長を停止した紡錘体の両極の間を迷子のように行ったり来たりしながら、徐々に両極へと移動していくことが明らかになりました。これらの三つのステップのそれぞれが起こることで、紡錘体が正しい機能と形を獲得できると考えられました。
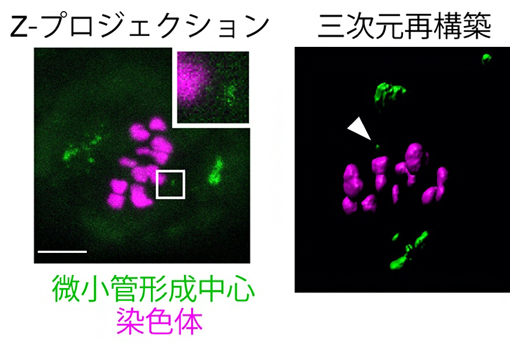
図2 紡錘体伸長後の微小管形成中心(緑)と染色体(マゼンタ)
紡錘体伸長後のZ-プロジェクション像(顕微鏡の焦点を変えて撮影した複数の画像を重ねたもの)と三次元再構築像。多くの微小管形成中心は紡錘体の両極に位置していたが、中央に位置するものが少数あった。四角で囲んだ部分と矢頭が中央にある微小管形成中心。スケールバーは10μm。
次に、紡錘体の微小管と動原体の接続が、三つのステップのいずれかを制御している可能性について調べました。この目的のために、微小管と動原体の接続を担うNdc80タンパク質[3]に点変異を導入することで、接続を不安定にする実験系を確立しました。
微小管と動原体の接続を不安定化させた卵母細胞における紡錘体形成をライブイメージングにより録画したところ、第二のステップである紡錘体の伸長停止以降に異常が起きることが分かりました。これらの卵母細胞では、紡錘体の伸長は正常なタイミングで開始するものの、停止できずに過剰に伸長してしまうことが明らかになりました。さらに、微小管形成中心を紡錘体の両極にとどめておくことができず、多くの微小管形成中心が中央部で迷子のように行ったり来たりを繰り返すことが分かりました(図3)。
これらの結果から、微小管と動原体の安定な接続が、紡錘体の伸長を停止させ、また、微小管形成中心の位置を紡錘体両極に限定することで、紡錘体の形および機能を調整するのに必要であることが分かりました。
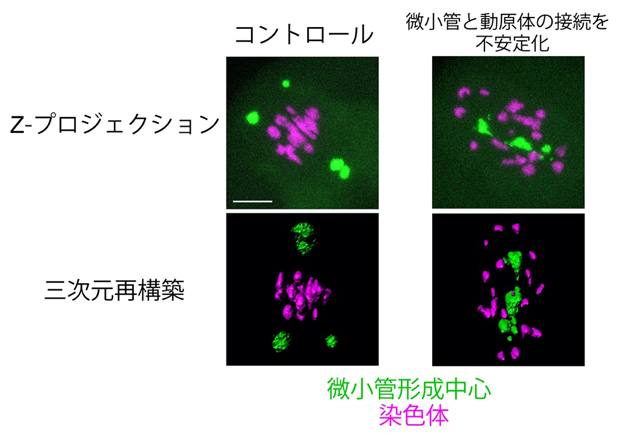
図3 紡錘体の形と機能を調整する微小管と動原体の接続
微小管と動原体の接続を人為的に不安定化させ、紡錘体伸長後の微小管形成中心(緑)の配置を比べた。微小管と動原体は本画像では表示していない。左のコントロールでは多くの微小管形成中心は紡錘体の両極に位置していたが、右の接続を不安定化したものでは多くが中央近傍に位置していた。スケールバーは10μm。
最後に、微小管と動原体の接続がどのように正しい紡錘体の形成機能を果たすのかを調べました。卵母細胞を固定し、微小管、動原体、微小管形成中心を同時に高解像度で観察したところ、動原体に接続した微小管の多くは、紡錘体両極に位置する微小管形成中心とも接続し、両者を橋渡しするかのように存在していることが分かりました。これらのことから、動原体に接続した安定な微小管の長さが、微小管形成中心の位置と、伸長が停止するべき紡錘体の長さを決定することに関わっている可能性が考えられました。
今後の期待
今回の研究から、紡錘体が正しく形成され、卵子に正常に染色体が分配されるためには、微小管と動原体の安定な接続が重要であることが明らかになりました。
ヒト卵子は染色体数異常の頻度が高いことで知られ、このことは流産やダウン症などの先天性疾患の主要な原因です。卵子の染色体数異常を引き起こす原因の一つとして、紡錘体形成の異常があることが報告されています。紡錘体の形および機能が調整される機構の一端が分かったことで、卵子の染色体数異常の原因となる紡錘体異常の理解につながると期待できます。
補足説明
1.紡錘体
細胞分裂の際に染色体を分配するための細胞内構造で、主に微小管から構成される。微小管については[4]参照。
2.卵子、卵母細胞
卵原細胞が増加した後、分化してできた雌性生殖細胞を卵母細胞と呼ぶ。卵母細胞は大きく成長した後、減数分裂を経て受精可能な卵子となる。
3.動原体、Ndc80タンパク質
動原体は染色体のくびれ部分上に形成されるタンパク質複合体で、Ndc80はその構成タンパク質の一つ。染色体分配の際に、微小管が染色体を動かすための牽引部位となる。体細胞分裂では姉妹染色分体のそれぞれに動原体が一つずつ形成され、減数第一分裂では相同染色体のそれぞれに動原体が一つずつ形成される。
4.微小管、微小管形成中心
「微小管」は細胞内で繊維状の構造をとる細胞骨格の一つである。αチューブリンとβチューブリンと呼ばれるタンパク質のヘテロ二量体が重合し、円筒状の繊維を形成したもので、重合・脱重合を可逆的に行うことで形態を変化させる。微小管には方向性があり、重合・脱重合が起きやすい末端をプラス端、反対側をマイナス端と呼ぶ。また、チューブリン重合の核となる構造を「微小管形成中心」と呼び、多くの動物の体細胞分裂では、主に中心体がその役割を果たすが、哺乳類の卵母細胞は中心体を持たない。哺乳類卵母細胞の紡錘体形成では、マイナス端が紡錘体の両極へ、プラス端が中央へ向かって配向し、これにより紡錘体は両極へ伸長した形をとり、微小管のマイナス端に存在する構造体である微小管形成中心は紡錘体の両極へ配置される。
5.染色体数異常
細胞が持つ染色体数が本来より多い、あるいは少ない異常のこと。染色体数異常の卵子が受精すると、染色体数が1本多いトリソミーや1本しかないモノソミーの受精卵が生じる原因となる。
6.減数分裂
真核生物の生殖器官(精巣や卵巣)にある生殖細胞で見られる、配偶子(精子や卵子)を作るための特別な様式の細胞分裂。途中でDNAが複製されることなく、2回の細胞分裂(減数第一分裂、減数第二分裂)が起こる。染色体セットの数が半分に減少して配偶子にもたらされるために、減数分裂と呼ぶ。
7.ライブイメージング
生きた細胞や組織、個体の生命活動を継時観察すること。特に、GFPなどの蛍光タンパク質を用いて特定のタンパク質や細胞を標識し、蛍光顕微鏡でその動きや変化を詳細に観察する手法は、生命科学の必須の手法となっている。
研究チーム
理化学研究所 生命機能科学研究センター 染色体分配研究チーム
チームリーダー 北島 智也(きたじま ともや)
研究員(研究当時) オーレリアン・クートワ(Aurelien Courtois)
上級研究員 吉田 周平(よしだ しゅうへい)
訪問研究員 竹之内 修(たけのうち おさむ)
(日本学術振興会 特別研究員)
研究パートタイマーI 浅井 皓平(あさい こうへい)
(京都大学大学院 生命科学研究科 大学院生)
研究支援
本研究は、日本学術振興会(JSPS)科学研究費助成事業新学術領域研究「配偶子インテグリティ(領域代表者:林克彦)」などによる支援を受けて行われました。
原論文情報
Aurelien Courtois, Shuhei Yoshida, Osamu Takenouchi, Kohei Asai, and Tomoya S. Kitajima, “Stable kinetochore-microtubule attachments restrict MTOC position and spindle elongation in oocytes”, EMBO Reports, 10.15252/embr.202051400
発表者
理化学研究所
生命機能科学研究センター 染色体分配研究チーム
チームリーダー 北島 智也(きたじま ともや)
研究員(研究当時) オーレリアン・クートワ(Aurelien Courtois)
報道担当
理化学研究所 広報室 報道担当